Science Advances:宋相容团队开发锰基LNP-mRNA疫苗,增强mRNA表达并提高免疫原性,更好预防新冠突变株
时间:2022-12-29 17:59:50 热度:37.1℃ 作者:网络
目前已有多种疫苗被批准用于预防COVID-19,其中包括两款mRNA疫苗,分别是辉瑞/BioNTech开发的Comirnty(BNT162b2),以及Moderna开发的Spikevax(mRNA-1273)。mRNA疫苗具有免疫原性高、生产速度快、成本低等独特优势,在抗击COVID-19大流行中发挥了极其有效的作用。
然而,层出不穷的SARS-CoV-2突变株,例如当前的主要流行株Omicron,它们的免疫逃逸对现有的mRNA疫苗构成了重大挑战。因此,开发更有效的针对新型新冠突变株的mRNA疫苗势在必行。
抗原呈递细胞(APCs),例如树突状细胞(DCs)的高效抗原呈递是mRNA疫苗高效发挥作用的前提,这需要足够的蛋白翻译和APCs成熟。此外,成熟DC上高表达的共刺激分子为未成熟T细胞的激活提供了次要信号,佐剂可促进DC成熟,上调DC共刺激分子表达。因此,佐剂的共递送是增强mRNA疫苗免疫效果的有效策略。
近日,四川大学华西医院生物治疗国家重点实验室宋相容团队在 Science 子刊 Science Advances 上发表了题为:Manganese-coordinated mRNA vaccines with enhanced mRNA expression and immunogenicity induce robust immune responses against SARS-CoV-2 variants 的研究论文。
该研究以新型可电离脂质(IC8)为基础,引入干扰素基因刺激因子(STING)的激动剂锰(2价Mn离子),构建了具有高免疫原性的新型mRNA递送系统——IC8/Mn-LNP。首次证实了Mn不仅能通过激活STING通路促进抗原呈递细胞(APC)的成熟,还能通过促进溶酶体逃逸来提高mRNA表达。
该研究还使用IC8/Mn-LNP递送了新冠突变株Delta或Omicron的全长刺突蛋白的mRNA序列,这两种mRNA疫苗均有到了针对Delta或Omicron的大量特异性IgG反应,还表现出较强的对新冠假病毒病毒的中和能力、Th1细胞偏向性免疫应答,且安全性较好。
这项研究表明,新型mRNA递送系统——IC8/Mn-LNP在开发Mn协同增强的mRNA疫苗方面具有很大潜力,具有较强的免疫原性和良好的安全性。

佐剂的共递送是增强mRNA疫苗免疫效果的有效策略。Toll样受体(TLRs)和干扰素基因刺激因子(STING)的激动剂,已经作为佐剂应用于mRNA疫苗。然而,TLR激动剂会引起严重的细胞因子风暴,这限制了其临床应用。STING激动剂作为佐剂使用时会诱导相对低水平的局部和全身炎症。
2019年9月,苗蕾等人在 Nature Biotechnology 期刊发表论文,开发了一个可电离脂质文库,作为mRNA递送载体,通过激活STING通路促进mRNA在体内的递送并增强抗肿瘤效果。
锰(Mn)是许多生理过程中必不可少的元素,能够通过直接激活cGAS来刺激STING通路,但Mn是否能增强mRNA疫苗的免疫效果尚不清楚。
递送系统能够保护mRNA免于被快速降解,并帮助其被细胞摄取并释放,这对于mRNA在体内的高效表达必不可少。脂质纳米颗粒(LNP)在目前唯二获批的mRNA新冠疫苗中表现出良好的疗效和安全性。
2022年7月,宋相容团队在 Advanced Functional Materials 期刊发表研究论文,发现LNP中的可电离脂质会显著影响mRNA表达,与Moderna公司的mRNA疫苗的LNP中使用的单一氮原子的可电离脂质相比,具有多个叔氨基氮原子的可电离脂质可显著增强mRNA疫苗的免疫原性,可引发了强大和持久的体液免疫反应。

在这篇发表于 Science Advances 的最新研究中,宋相容团队设计并构建了含有锰(Mn)和新型可电离脂质(IC8)的新型脂质纳米颗粒——IC8/Mn-LNP。
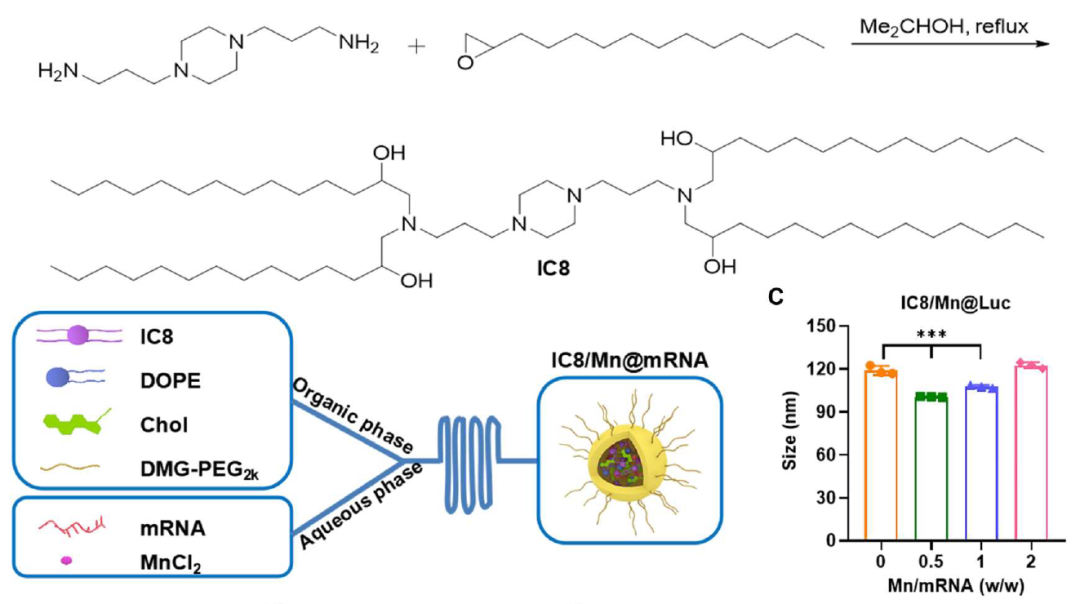
研究团队将IC8/Mn-LNP用于对mRNA的递送,然后评估其装载编码SARS-CoV-2突变株全长刺突蛋白(S蛋白)的mRNA(IC8/Mn@S)后的免疫原性,及其对SARS-CoV-2突变株的防护机制。
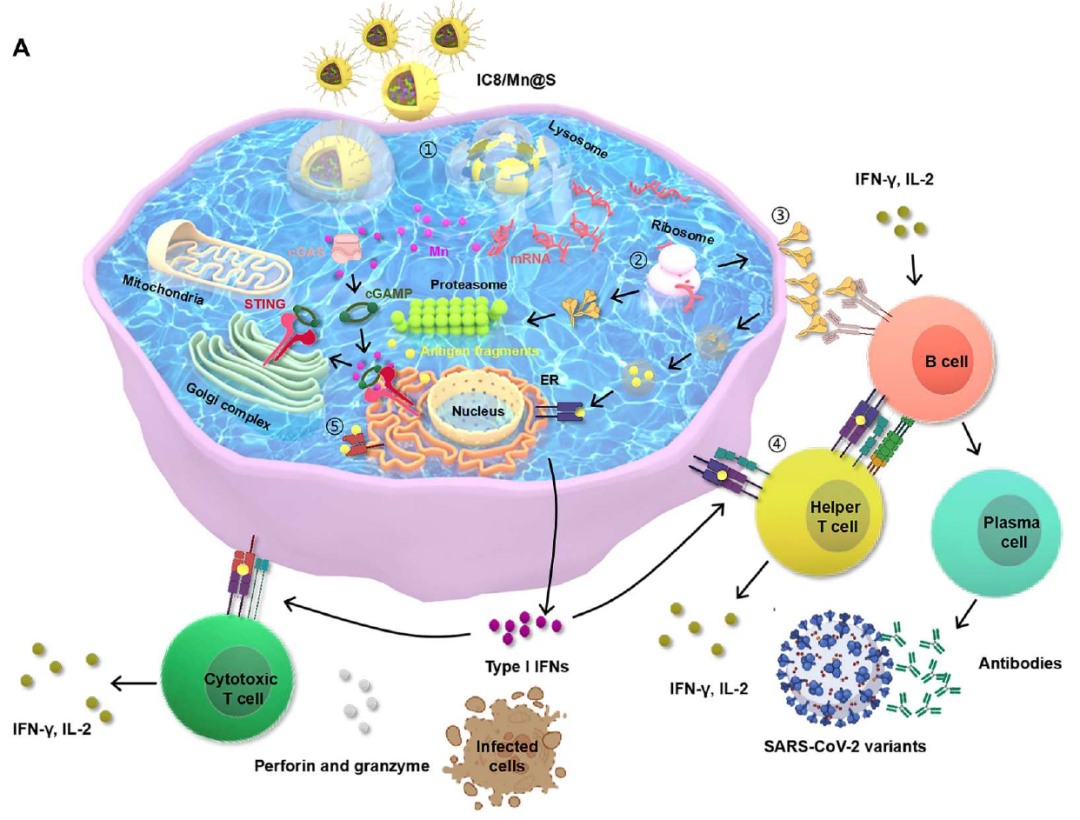
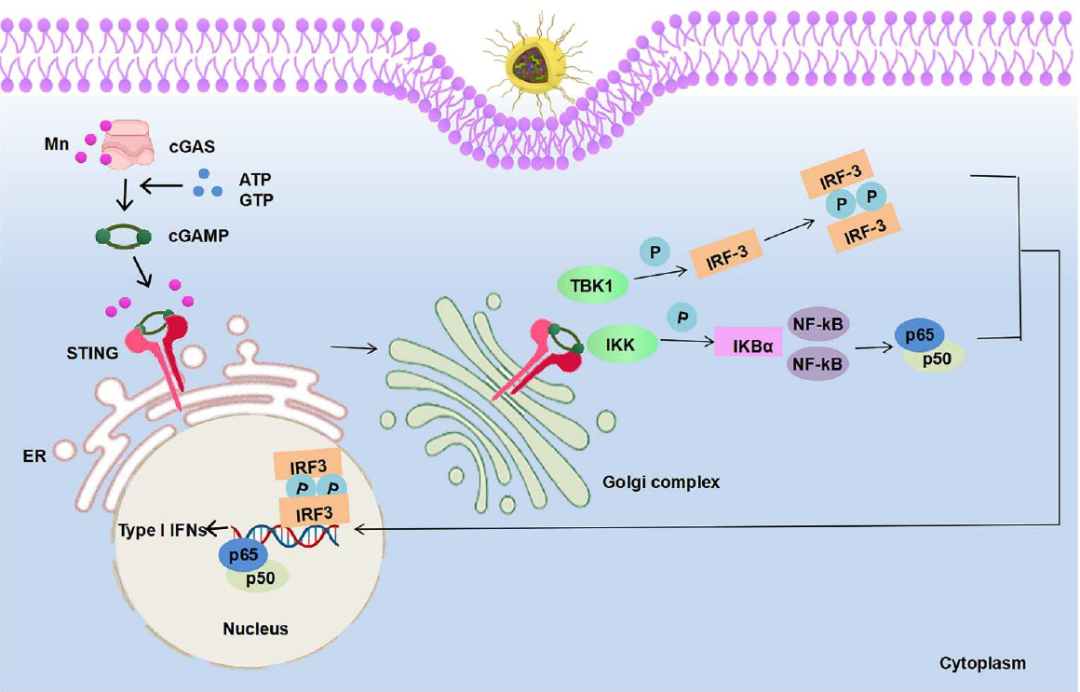
锰(Mn)通过促进溶酶体逃逸提高mRNA表达,并通过激活STING通路刺激抗原呈递细胞(APCs)成熟。此外,IC8/Mn@S在最佳剂量下 (Mn:mRNA=1:1)诱导出对新冠突变株Delta和Omicron的强效、持久的IgG抗体。
这项研究表明,新型mRNA递送系统——IC8/Mn-LNP在开发Mn协同增强的mRNA疫苗方面具有很大潜力,具有较强的免疫原性和良好的安全性,具有很好的临床应用前景。
论文链接:
1. https://www.science.org/doi/10.1126/sciadv.abq3500
2. https://www.nature.com/articles/s41587-019-0247-3
3. https://doi.org/10.1002/adfm.202204692


