2023 SG-BCC来了!特选5项中国学者研究壁报!先睹为快!
时间:2023-03-16 18:00:39 热度:37.1℃ 作者:网络
第十八届圣加伦国际乳腺癌大会(SG-BCC 2021)于欧洲中部时间(CET)2023年03月15日在奥地利维也纳正式召开!作为全球最具有影响力的有关早期乳腺癌诊断和治疗的国际研讨会,汇集全球各大合作组和中心的领先专家,共同探讨早期乳腺癌女性治疗的最新进展。SG-BCC官网公布入选摘要标题,梅斯医学精选5篇来自中国大陆的研究报告,让我们一睹为快!
摘要:P004
标题:Pyrotinib after trastuzumab-based adjuvant therapy in patients with HER2-positive breast cancer : a multicenter, open-label,phase 2 trial
吡咯替尼在HER2阳性乳腺癌患者曲妥珠单抗辅助治疗后的应用:一项多中心、开放、2期试验
目的:在这项研究中,我们旨在评估延伸佐剂吡咯替尼(一种针对HER1、HER2和HER4的口服不可逆泛HER受体酪氨酸激酶抑制剂)在曲妥珠单抗辅助治疗高危早期或局部晚期HER-2阳性乳腺癌患者中的有效性和安全性。
方法:这是一项多中心、开放的II期试验,在中国的23个中心进行。纳入高危早期或局部晚期HER-2阳性乳腺癌和已知的激素受体状态的妇女,在6个月内完成基于曲妥珠单抗的1年辅助治疗。
高危患者必须符合以下标准之一:N≥1;T≥2;新辅助治疗后未达到病理完全缓解;新辅助治疗后T≥5 cm或N≥2;T<2 cm但Ki67高、组织学分级3或有淋巴结微转移。
符合条件的患者被分配接受6个月或1年的口服吡咯替尼400 mg/d。主要终点是2年期IDFs率。
结果:2019年1月至2022年2月,141名符合条件的女性入选并接受吡咯替尼治疗。
11名患者没有进行疗效评估(因不良事件或其他原因在两周内撤回研究),因此130名患者进入完整分析集,其中94名患者接受1年的吡咯替尼治疗,36例接受6个月的治疗。完整分析集中患者的基线特征如表1所示。
表1 完整分析集合中患者的基线特征
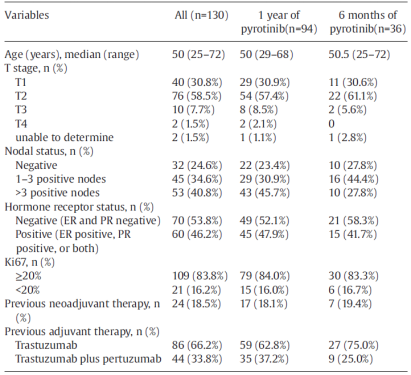
截至2022年10月10日,中位随访时间为24个月(IQR:18-34个月)。6名患者(4.6%)发生IDFS事件,其中3名(3.2%)服用吡咯替尼1年,3名(8.3%)服用6个月。
报告的最常见的不良事件是腹泻(79.4%),其中43名患者(30.3%)经历了3级腹泻(表2)。没有4级或更高级别的不良事件报告。
表2 至少10%的患者因治疗引发不良事件
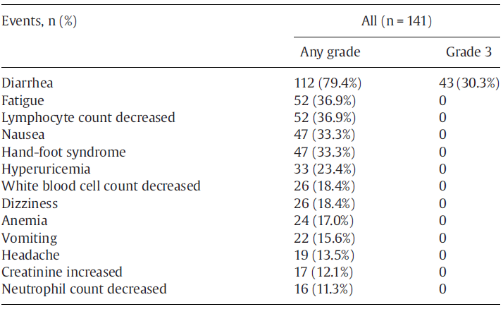
结论:曲妥珠单抗辅助治疗后应用扩展辅助剂吡咯替尼对高危早期或局部晚期HER-2阳性乳腺癌具有良好的耐受性和潜在疗效。后续研究正在进行中,以确定延长佐剂吡咯替尼的长期益处。
作者:温州医科大学附属第一医院王瓯晨教授等
摘要:P012
标题:Survival outcomes and toxicities of adjuvant docetaxel-cyclophosphamide for four cycles in node negative triple negative and HER2 positive Chinese breast cancer patients: A 10 year follow up study
多西紫杉醇-环磷酰胺辅助治疗结节阴性三阴性和HER2阳性中国乳腺癌患者的生存结果和毒副作用:一项10年随访研究
目的:结节阴性的三阴性乳腺癌(TNBC)和HER2阳性乳腺癌(HER2+BC)的最佳化疗方案还不确定。四个周期的多西他赛-环磷酰胺(DC4)(单独用于TNBC,与曲妥珠单抗同时用于HER2+BC)是一种需要较少周期的低强度选择。本研究调查了DC4的长期生存结果、预后因素和毒副作用。
方法:收集2007年至2013年接受DC4辅助治疗的结节阴性TNBC和HER2+BC(第一天D 75 mg /m2和C 600 mg/m2,21天为1周期)。排除pT4和HER2+但没有接受曲妥珠单抗的患者。使用KaplanMeier方法估计总生存率(OS)和侵入性无病生存率(iDFS)。生存结果的预后因素采用Cox比例危害模型进行评估。
结果:在符合纳入标准的111例患者中,62例(55.9%)为TNBC,49例(44.1%)为HER2+BC。中位年龄52岁(范围29-70岁)。60.4%的患者接受了乳房切除术。51.4%的患者pT2以上。超过三分之二的患者(67.6%)患有3级疾病。中位随访10年,TNBC组5年和10年OS率分别为88.7%和87.1%,HER2+BC组分别为95.9%和89.4%。TNBC组5年和10年IDFS率分别为83.9%和77.0%,HER2+BC分别为89.8%和85.6%。TNBC和HER2+BC的OS和IDFS差异无统计学意义。年龄、手术类型、T分期、肿瘤分级、淋巴血管侵犯和高Ki 67均不影响OS和IDF的预后。激素受体状态不能预测HER2+BC患者的预后(表1)。大多数患者(50.5%)的最大毒性分级为1级。
没有观察到与治疗相关的死亡。最常见的3级或4级毒性是中性粒细胞减少,发生率为34.2%。24.3%的患者出现发热性中性粒细胞减少症。预防性应用G-CSF的患者发热性中性粒细胞减少的发生率显著低于未预防性应用的患者(16.0%vs.70.6%,卡方检验P<0.001)。
表1 OS和iDFS的预后因素
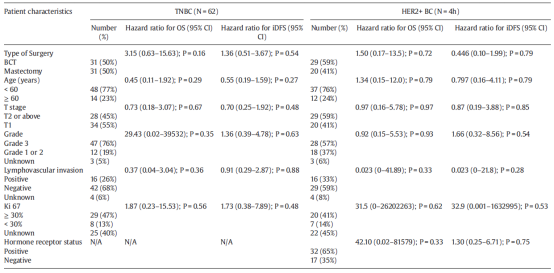
结论:DC4对TNBC阴性和HER2+ BC患者有很好的生存结果,这与文献中使用更强化方案的历史队列相当。强烈建议预防性使用G-CSF来降低中国患者发热性中性粒细胞减少症的风险。未来需要更大样本量的研究来确定强化治疗的患者亚组,以进一步改善治疗效果。
作者:香港荔枝角玛嘉烈医院肿瘤科郭崇华教授等
摘要:P035
标题:SLC26A9 promotes the development and stemness of triple-negative breast cancer via activating EGFR/PI3 K/AKT signaling pathway
SLC26A9通过激活EGFR/PI3K/AKT信号通路促进三阴性乳腺癌的发展和干化
目的:离子通道和转运蛋白的失调可以导致疾病的进展和发展,已经得到了广泛的研究。此前,我们首次报道了碳酸氢盐转运蛋白SLC26A9在胃癌发生发展中的作用。然而,SLC26A9在三阴性乳腺癌(TNBC)中的作用尚不清楚。
方法:利用组织芯片和TNBC细胞系检测SLC26A9的表达水平及其临床意义。利用器官的构建来研究TNBC的干性,通过改变SLC26A9在TNBC中的表达水平来探索SLC26A9在TNBC中的作用和分子机制。
结果:与癌旁正常乳腺组织(n=69)和MCF10A细胞相比,SLC26A9在乳腺癌组织(n=105,p<0.0001)和细胞系中的表达显著上调,且与患者的不良预后密切相关。在体外,SLC26A9基因敲除或沉默可阻断TNBC细胞的G2/M期,诱导细胞凋亡,并显著抑制其增殖、迁移和侵袭。此外,SLC26A9的缺失改变了上皮-间充质转化(EMT)标志物的丰度,从而将MDA-MB-231细胞的细长纺锤体表型改变为鹅卵石样上皮表型。在体内,SLC26A9显著促进了裸鼠TNBC肿瘤的生长。在干性方面,CD44+CD24-细胞中SLC26A9的表达水平高于CD44-CD24+细胞,剔除SLC26A9后,CD44和乙醛脱氢酶1B1(ALDH1B1)的丰度降低,而CD24的丰度增加,CD44+CD24-细胞的比例也降低。随后,SLC26A9的缺失抑制了肿瘤球状体的形成、癌细胞的自我更新和集落形成能力,包括TNBC原代组织细胞的大小和数量。同时,免疫荧光检测显示,基底样标志物K14和管腔标志物K8的表达受到了抑制,这表明SLC26A9与细胞的干性和分化显著相关。机制上,随着SLC26A9的缺失,EGFR/PI3K/AKT信号通路及其下游的增殖相关基因CCND1(CyClinD1)、cMyc受到明显抑制。
结论:SLC26A9的上调可能通过激活EGFR/PI3K/AKT信号通路促进TNBC的进展、发展和干化,有望为TNBC的治疗提供新的方向。
摘要:P186
标题:Confirmatory study of nanoparticle-assisted axillary staging in breast cancer patients who received neoadjuvant chemotherapy:expanded indication and reduced axillary intervention
对接受新辅助化疗的乳腺癌患者进行纳米颗粒辅助腋窝分期的验证性研究:扩大适应症,减少腋窝干预
目的:纳米颗粒辅助腋窝淋巴结分期(NAAS)结合了标准的双示踪剂(放射性同位素和蓝色染料)前哨淋巴结活检(SLNB),在接受新辅助化疗(NAC)前NAC阳性的乳腺癌患者中显示出良好的效果。这项研究旨在验证NAAS在更大人群中的准确性,探索SLNB适应症的扩展,并选择可能免除NAC后乳腺癌患者腋窝淋巴结清扫(ALND)的特定患者。
方法:研究对象为2020年11月至2022年7月接受NAAS和ALND治疗的浸润性乳腺癌患者。评价NAAS的检出率(DR)、假阴性率(FNR)、阴性预测值(NPV)和准确性。
结果:200例符合条件的患者顺利完成NAAS,其DR、NPV、准确性和FNR分别为97.09%、95.73%、97.5%和5.68%。值得注意的是,如果去除SLNs≥5,则NAAS的FNR降至0%。此外,NAAS还显示了95.38%的高准确率和8.57%的可接受的FNR,用于NAS治疗前N2-3乳腺癌患者。治疗前N1和N2-3乳腺癌患者的FNR、NPV和准确性没有统计学差异。此外,经NAAS在SLNS中分离出肿瘤细胞(ITCs)的患者在ALND中没有进一步的阳性病变。
结论:NAAS表现出优异和稳定的性能,FNR低,准确率高,表明在接受NAC的乳腺癌患者中具有较好的应用前景。如果NAAS显示阴性结节,NAC后N2-3期的患者也有机会避免ALND。此外,在SLNs中检测到ITCs的患者也可以免于ALND。
作者:四川大学华西医院杨俊杰教授等
精彩内容持续更新~敬请期待!


