【Blood】CAR-T联合伊布替尼治疗R/R MCL的2期TARMAC研究结果
时间:2023-11-06 15:44:16 热度:37.1℃ 作者:网络
伊布替尼联合CAR-T治疗MCL
CD19 CAR-T 细胞疗法在复发性或难治性套细胞淋巴瘤(R/R MCL)患者中获得了较高的缓解率,但也存在显著毒性,包括细胞因子释放综合征 (CRS) 和神经毒性,此外复发率也较高。临床前和临床数据支持伊布替尼对单采产物健康度(fitness)、CAR-T扩增和毒性的有益协同效应。
因此澳大利亚学者开展一项研究者发起的II 期 TARMAC 研究,在20例 MCL 患者中评价了时间限制性伊布替尼联合CAR-T 治疗的疗效和安全性,研究的II期结果近日发表于《Blood》。

关键点
1、CD19 CAR-T 细胞和时间限制性伊布替尼是复发难治性套细胞淋巴瘤的有效组合。
2、新型联合治疗可克服负面的临床和分子特征,包括 BTK抑制剂难治性和 TP53 突变。
研究方法
研究纳入既往接受≥1线治疗(可包括BTK抑制剂[BTKi])、放射学或组织学可检测病灶的R/R MCL 患者,关键排除标准包括既往异基因干细胞移植、既往 CAR-T 治疗或活动性中枢神经系统 (CNS) 淋巴瘤。
患者接受伊布替尼 560mg 每日给药,并因毒性适当降低剂量;进入研究时接受伊布替尼治疗的患者继续治疗。在单采前给予伊布替尼至少7天,并在 CAR-T 生产、清淋和 CAR-T 输注后持续给药。如果中心静脉置管且未停用伊布替尼则提供血小板输注。根据治疗医生的判断进行桥接治疗。所有患者均接受了清淋治疗,包括氟达拉滨 25 mg/m2和环磷酰胺250 mg/m2,每日一次,持续3天,2-5天后接受tisagenlecleuce单次给药,剂量为0.6-6.0 x 108 CAR阳性细胞。
主要终点为根据 Lugano 2014 版标准,研究者确定的输注后第4个月时的完全缓解率 (CRR)。次要终点包括不良事件的发生率和严重程度、客观缓解率(ORR)、第1、4、6、9和12个月时的 MRD 阴性率、无进展生存期 (PFS)、缓解持续时间 (DoR) 和总生存期 (OS)。
研究结果
患者特征和既往治疗
20例可评估患者 (100%) 均成功生产CAR-T,并接受单次输注,中位细胞剂量为3.0 x 108 CAR阳性细胞。从研究入组至 CAR-T 输注的中位时间为60天(,CAR-T生产(从订单至输注)的中位时间为49天。
研究入组时的基线特征总结见表1。中位年龄为66岁,75%为男性。既往中位治疗为2线。入组研究时,中位 TMTV 为166 cm3。19例患者 (95%) 既往暴露于利妥昔单抗和化疗,包括16例 (80%) 暴露于含阿糖胞苷的治疗方案和3例 (15%) 既往接受苯达莫司汀治疗。55%的患者既往接受过自体干细胞移植。10例患者 (50%) 既往暴露于BTKi;9例 BTKi 治疗难治 (45%),3例 (15%) 接受过一种以上BTKi。7例患者 (35%) 在研究入组时正在接受伊布替尼,所有其他患者均在入组时开始接受伊布替尼。单采前连续使用伊布替尼的中位时间为12天。既往未暴露于 BTKi 的患者(BTKi初治)的既往治疗线数(中位数1线)少于既往暴露于 BTKi 的患者(BTKi暴露)(中位数3线)。BTKi暴露患者中末线治疗难治患者更多。
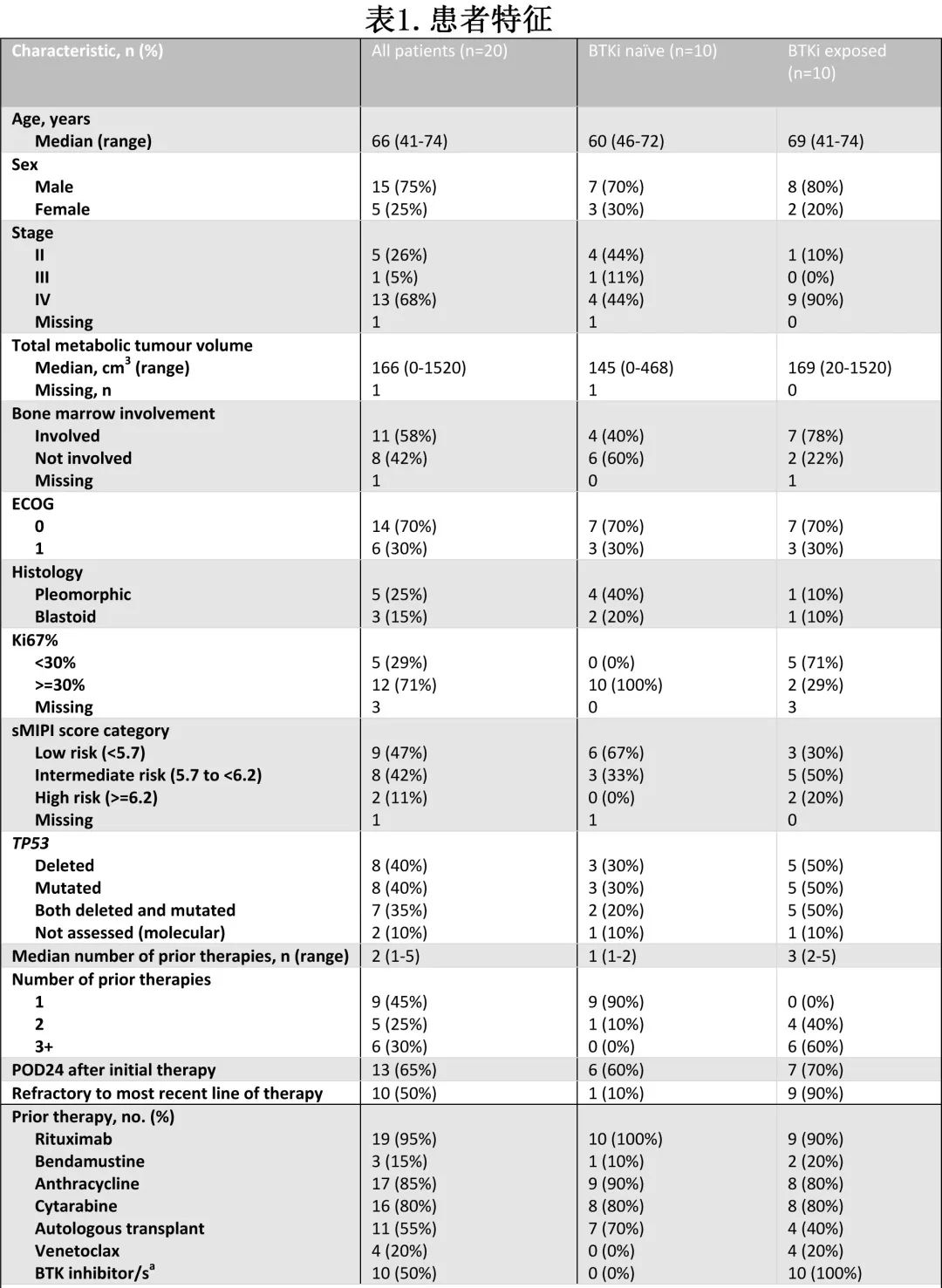
高危特征很常见:65%的患者在初始治疗后发生POD24,53%的患者入组时为MIPI 中危或高危,15%具有母细胞样形态。
基因特征
19例 (95%)MCL 经 FISH 证实为IGH::CCND1融合,1例根据免疫组化检测 cyclin D1 和 SOX11 表达确诊。18例患者 (90%) 可通过 NGS 进行基因组谱分析(图1)。常见异常包括CCND1(30%)、ATM(25%) 和 NOTCH2(25%) 突变。
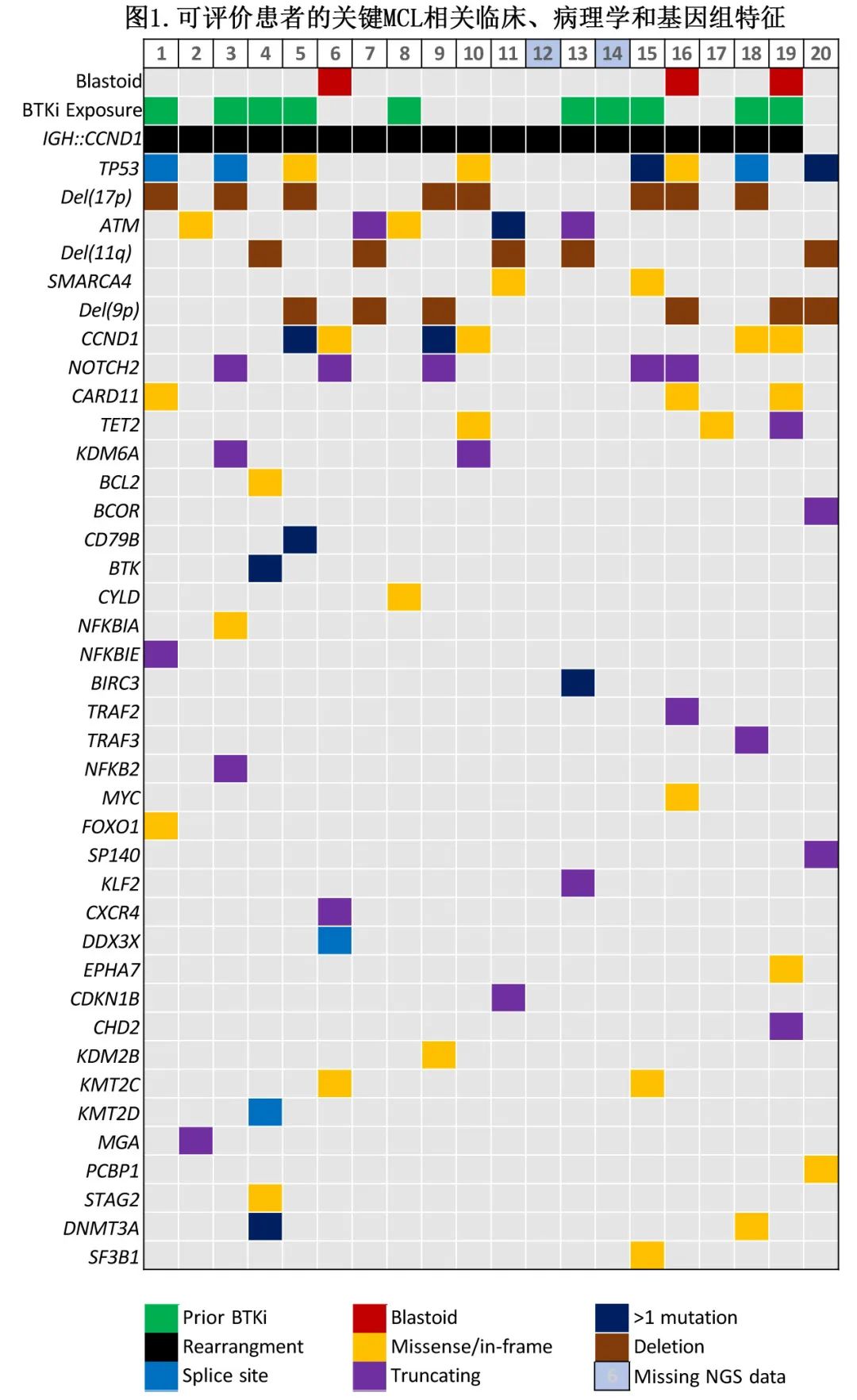
分别有20例 (100%) 和18例 (90%) 患者的 Del(17p) 和 TP53 突变状态已知,9例患者 (45%)存在TP53 畸变,1例(5%) del(17p)但无无突变,1例 (5%) TP53 多个突变但无缺失;其余7例患者 (35%)并发 del(17p) 和 TP53 突变。在8例 (40%) 中观察到 SWI/SNF 染色质重塑复合物的改变,2例发生 SMARCA4 突变 (10%),6例发生涉及 SMARCA2 的del(9p) (30%)。
治疗和缓解
从研究入组开始,所有20例可评估患者均接受伊布替尼治疗,5例患者在CAR-T细胞生产期间需要桥接治疗,包括1-2个周期的利妥昔单抗、吉西他滨和奥沙利铂 (n=4) 或维奈克拉(n=1) 治疗。11例 (55%) 在清淋前达到客观缓解(7例 PR 和4例CR),5例为SD,4例为PD(图2)。
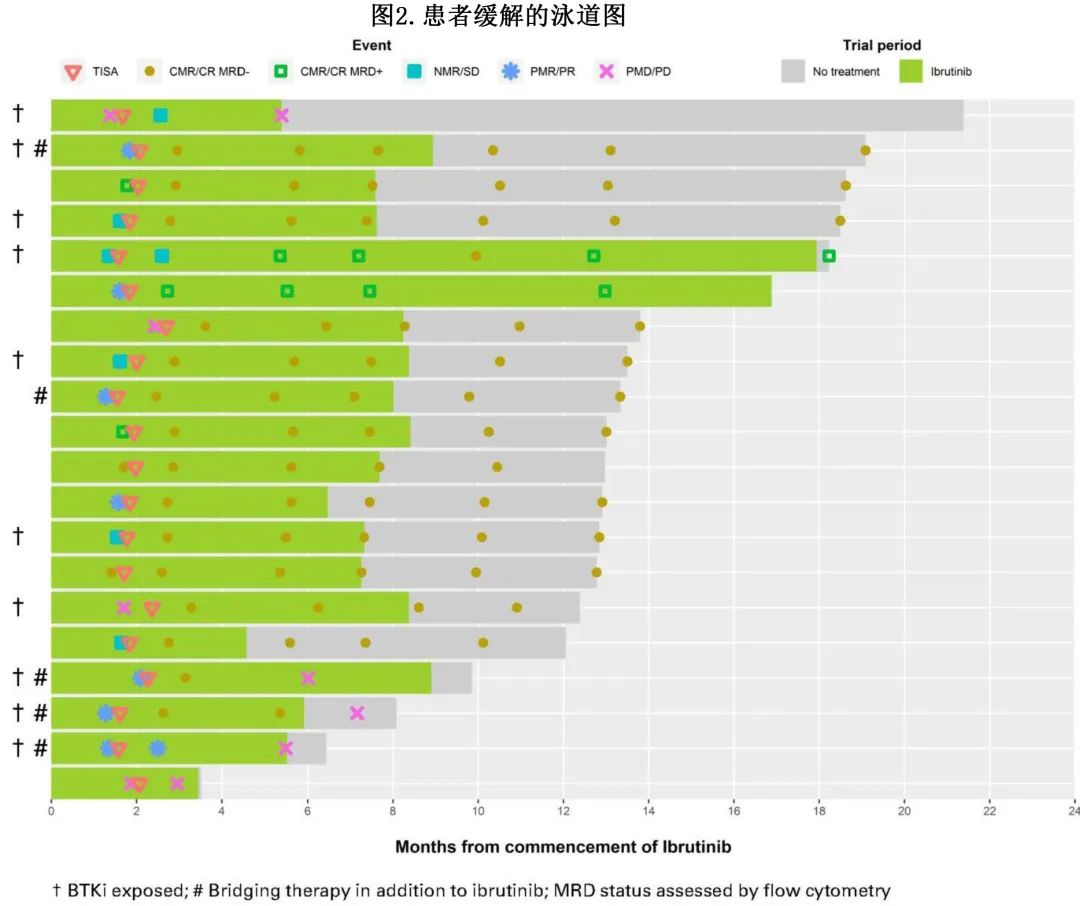
伊布替尼的中位剂量强度为100%;5例患者因CRS(n=2) 和皮疹 (n=1) 需要调整伊布替尼剂量,3例患者因 CRS 和皮疹 (n=1) 需要中断给药。患者在研究中接受伊布替尼的中位时间为7.3个月。
输注后所有20例患者均可评估缓解。输注后1个月,ORR为85% (80%CR),2例患者SD(10%),1例患者PD(5%)(图2)。
在输注后4个月的主要终点时,ORR和 CRR 均为80%(图3A)。1例患者在首次评估后缓解加深(SD至CR)。在第4个月达到 CR 的16例患者中,14例患者经流式细胞术检测为 MRD 阴性,因此主要终点时的总体 MRD 阴性率为70%(图3B)。所有14例流式 MRD 阴性患者均在6个月时间点停用伊布替尼。
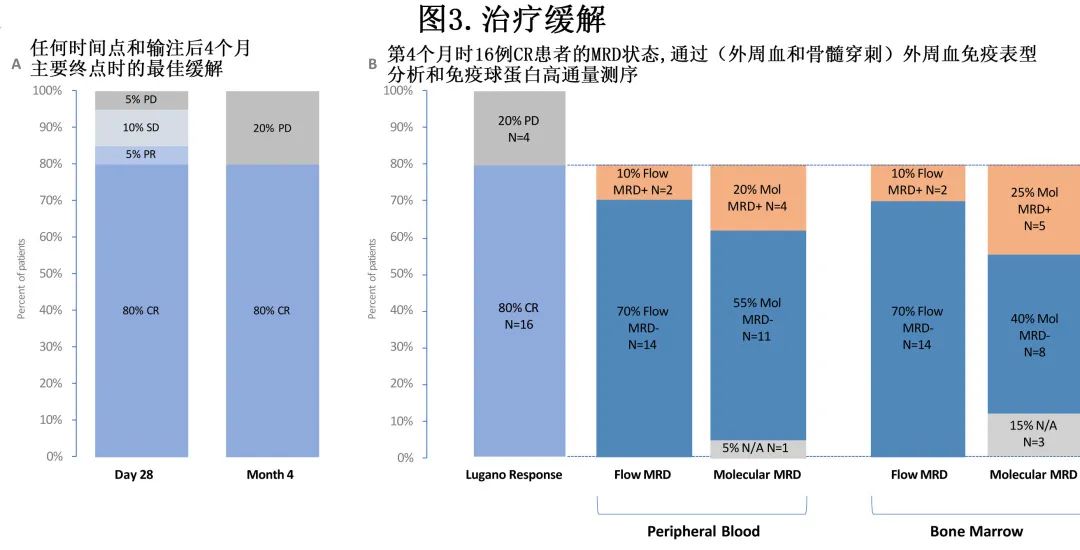
16例 CR 患者中,14例 BM 样本和15例 PB 样本的分子学 MRD 结果可用;共有5例患者显示骨髓分子 MRD 阳性(其中4例 PB 也为阳性),其中3例流式细胞仪检测为阴性。1例患者在基线时伴随浆细胞恶液质(意义不确定的单克隆丙种球蛋白病),因此分子阳性可能反映检测到克隆相关浆细胞肿瘤(同一样本的流式细胞术为阴性)。1例 BM 和 PB 中分子 MRD 阳性的患者在第6个月时出现疾病进展,2例仍接受伊布替尼治疗且无疾病进展(随访16.9个月和18.2个月),剩下一例患者尽管停止活性治疗,但在12.8个月观察后仍无疾病进展。
中位随访13个月,尚未达到中位PFS(图4)。12个月时估计的 PFS 和 OS 率分别为75%和100%。在数据截止日期无患者死亡。
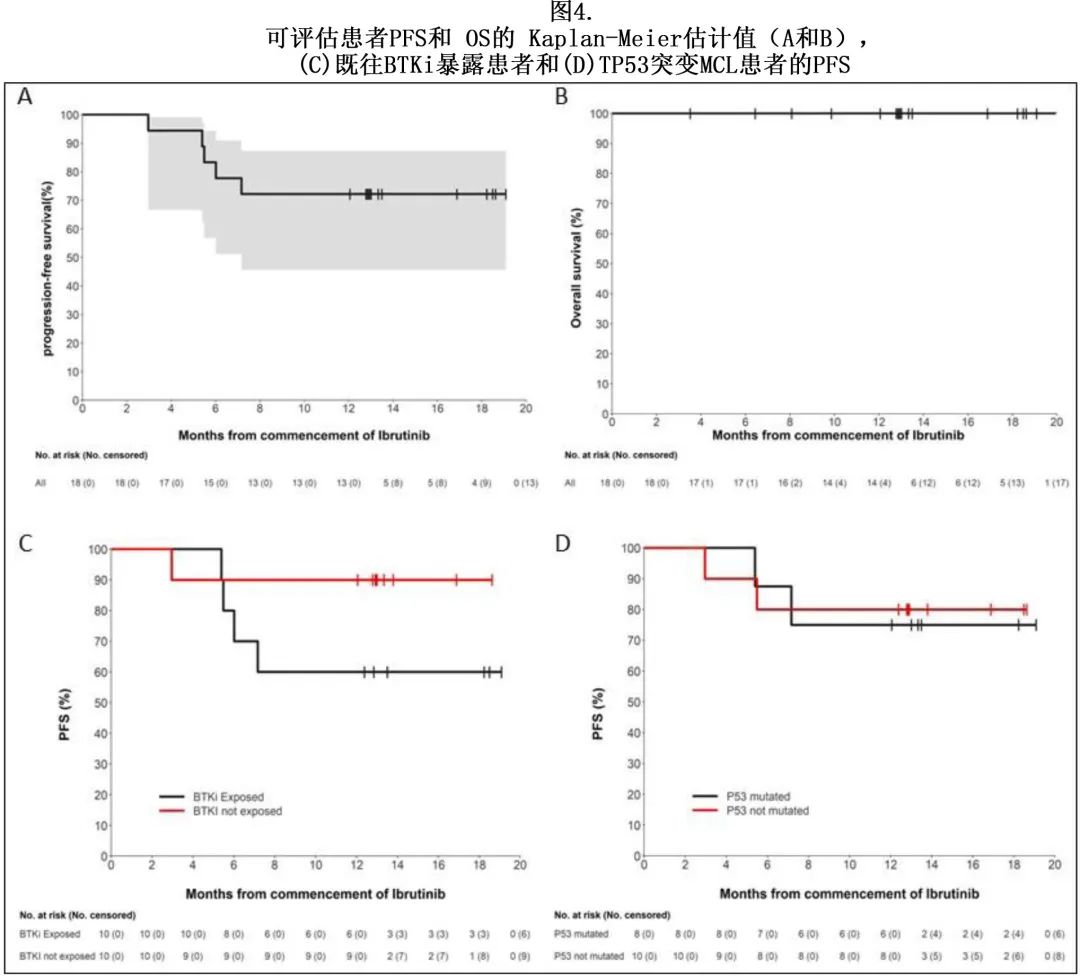
高危亚组中观察到深度和持久缓解
第4个月时的亚组分析显示,BTK初治和 BTK 暴露人群的 CRR 分别为90%和70%;8例 TP53 突变患者中的7例 (88%) 达到CR,6例可评估缓解患者中的4例 (67%) 显示分子学 MRD 阴性。无论既往 ASCT 状态、输注前缓解、母细胞样组织学或 Ki67% 如何,均观察到相似的 CR 率。应答者和非应答者之间的 TMTV 无显著差异,中位 TMTV 分别为123 cm3 vs 223 cm3 (p=0.6)。
深度缓解转化为持久PFS(图4C-D)。BTKi初治患者12个月时的 PFS 估计值为90%,而 BTKi 暴露患者为60%。有或无 TP53 突变或 SWI-SNF 畸变患者的12个月估计值相似(分别为 80% vs 75% 和88% vs 70%)。
3例苯达莫司汀暴露患者均未达到持久缓解,所有3例患者在主要终点时或之前均显示疾病进展。苯达莫司汀暴露患者年龄更大,表现出普遍高危的临床特征,包括 sMIPI 评分升高、既往治疗中位数增加和 POD24 率更高,但未观察到 TP53 畸变。
安全性
100%的患者记录了任何级别的不良事件,75%的患者发生3-4级事件。与研究治疗相关的最常见不良事件为任何级别的CRS (75%)、中性粒细胞减少 (50%)、腹泻 (30%)、皮疹 (20%) 和血小板减少(15%)。第28天有0%/15%/25%的患者 (n=20) 发生3-4级贫血、第90天无患者 发生中性粒细胞减少(n=19),第12个月0%/7%/0%的患者 (n=14)发生血小板减少。在输注后第一个月内,在总计4例患者 (20%) 中观察到8起感染发作,在该时间点后,在5例患者 (25%) 中再观察到8起感染发作,主要为1-2级;包括1例在随访期间发生症状性3级 COVID-19 感染的患者,其在4天后恢复。输注前发生了1起房颤事件,发生于脓毒症背景下;未观察到其他重大心律失常。
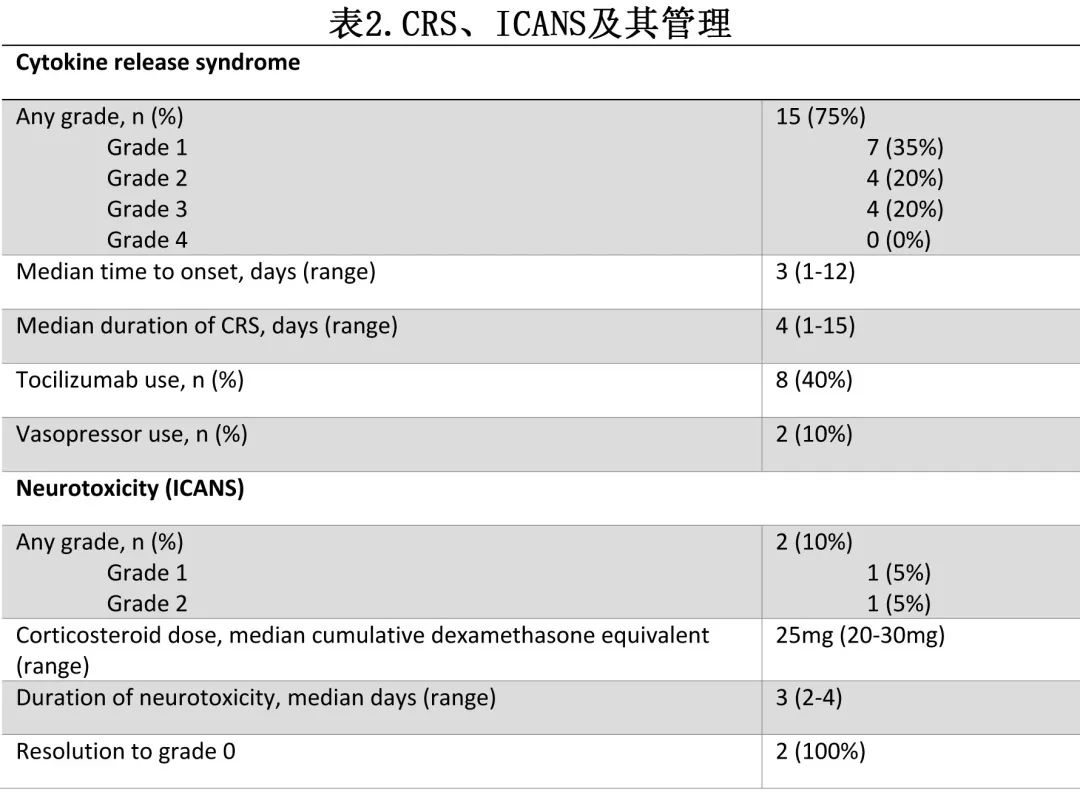
75%的患者发生CRS,55%为1-2级,20%为3级(表2)。无CRS(183cm3)、1-2级CRS(131cm3)和更高级别的≥3级CRS(145cm3)患者的基线中位 TMTV 相似。在发生3级 CRS 的4例患者中,所有患者在输注时均有可测量的疾病。对于所有患者,总体 CRS 的中位发作时间为第3天,中位持续时间为4天;未发生4级CRS。在2例患者中观察到免疫效应细胞相关神经毒性综合征 (ICANS)(1级,n=1;2级,n=1),持续2天和4天,并完全消退(表2)。9例患者 (45%) 接受托珠单抗给药(中位剂量2),7例患者 (35%) 接受地塞米松给药(中位剂量1),2例患者 (10%) 接受血管加压药。
输注后所有患者均存在外周血 B 细胞再生障碍性贫血,并在所有患者中持续至少6个月。基线时4例患者存在低丙种球蛋白血症,整个研究期间另外10例患者发生低丙种球蛋白血症;1例接受丙种球蛋白替代治疗。在中位9个月时,在6例患者中观察到 B 细胞恢复,定义为 PB B 细胞>总淋巴细胞的1%。
总结
该II期研究中,伊布替尼在白细胞单采之前开始给药,并持续至 CAR-T 生产和 CAR-T 给药后至少6个月。20例R/R MCL患者中位既往治疗线数为2,50%的患者既往暴露于BTKi。主要终点为输注后4个月的完全缓解率,次要终点包括安全性和基于 TP53 畸变的亚组分析。研究达到主要终点;80%的患者显示CR,通过流式细胞术和分子学方法分别有70%和40%的患者显示MRD阴性。在中位随访13个月时,估计12个月 PFS 为75%,OS为100%。15例 (75%) 发生细胞因子释放综合征,1-2级12例 (55%),3级3例 (20%)。在2例患者 (10%) 中观察到可逆性1-2级神经毒性。无论既往 BTKi 暴露或 TP53 突变如何均保持疗效。深度应答与稳健的 CAR-T 扩增和较少耗尽的基线 T 细胞表型相关。
总体而言,BTKi和 T 细胞重定向免疫治疗联合治疗的安全性和疗效似乎很有前景,值得进一步探索。
参考文献:
Minson AG,et al. CAR T-cells and Time-Limited Ibrutinib as Treatment for Relapsed/Refractory Mantle Cell Lymphoma: Phase II TARMAC Study.Blood . 2023 Oct 26:blood.2023021306. doi: 10.1182/blood.2023021306.


