《自然》子刊: ω-3 脂肪酸或有助于减少抑郁症
时间:2021-06-17 19:02:09 热度:37.1℃ 作者:网络
6月16日,美国国立卫生研究院 (NIHR) 莫兹利生物医学研究中心的研究人员发表在nature子刊上的研究,评估了高剂量 EPA 和 DHA 对实验室培养的神经元和抑郁症患者的影响,以帮助阐明这些物质是如何减少炎症和预防抑郁的。科学家们或许能够确定一种重要的分子机制,帮助抑郁症患者开发 ω-3 脂肪酸的潜在新疗法。

Alessandra Borsini et al.Omega-3 polyunsaturated fatty acids protect against inflammation through production of LOX and CYP450 lipid mediators: relevance for major depression and for human hippocampal neurogenesis.molecular psychiatry.DOI: 10.1038/s41380-021-01160-8
该研究评估了 22 名重度抑郁症患者,他们每天服用 3 克 EPA 或 1.4 克 DHA,持续 12 周。在 ω-3 PUFAs 治疗前后,他们在患者的血液中测量了 EPA 和 DHA 的脂质代谢物,并进行抑郁症状评分。
在两组患者中,EPA 或 DHA 治疗组都与其代谢物的增加和抑郁症状的显着改善相关,EPA 和 DHA 组的抑郁症状评分平均分别降低了 64% 和 71%。此外,在体外实验中鉴定出相同代谢物水平较高与抑郁症状水平较低相关。
实验室的临床研究表明,富含n-3多不饱和脂肪酸(ω-3 PUFAs)的饮食,如EPA和DHA,具有抗炎和抗抑郁的作用,深海鱼能够提练出EPA及DHA。此外,研究人员已经证明了IL1β(白细胞介素-1β)、IL6和干扰素-α(IFN-α)能够通过激活下游炎症信号通路、信号转导与转录激活因子 1(STAT1)和核因子激活的B细胞的κ-轻链增强(NF-kB),从而导致细胞增殖、神经形成减少、细胞凋亡增多。
在免疫失调的重度抑郁症患者中,不饱和脂肪酸(PUFAs)保护神经元免受炎症伤害。炎症反应之所以能够被激活,是因为白细胞介素-1β和IL6在脑脊液中分泌增加,这些炎症细胞因子导致了抑郁症状。以前的研究也证明过,通过EPA和DHA可以阻止IL1β细胞因子引起的神经形成减少。
多不饱和脂肪酸被环氧化酶(COX)、脂肪氧化酶(LOX)和细胞色素P450(CYP450)酶代谢成一系列脂质介质,表现出强大的免疫调节活性(见图a)。在神经元细胞中,EPA和DHA被代谢为LOX、CYP450羟化酶和COX脂质介质,这些脂质介质能阻止神经形成减少、神经元凋亡增多。在接受EPA或DHA治疗的抑郁症患者的血浆中,这些脂质代谢物会增加,它们支持多不饱和脂肪酸的抗抑郁、抗炎和神经保护作用。
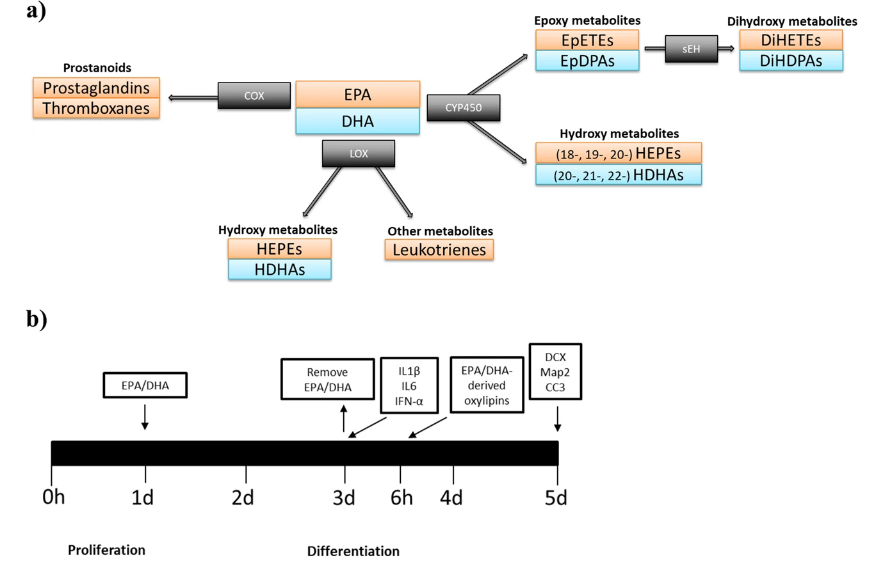
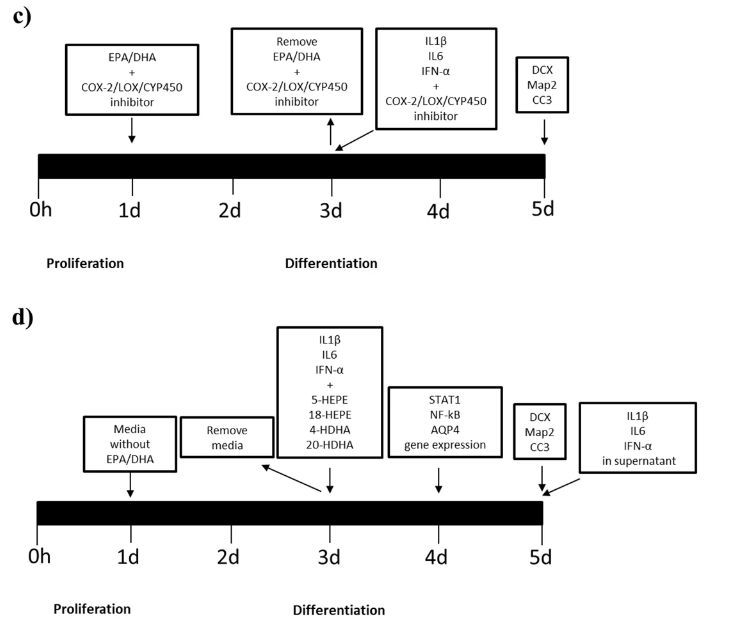
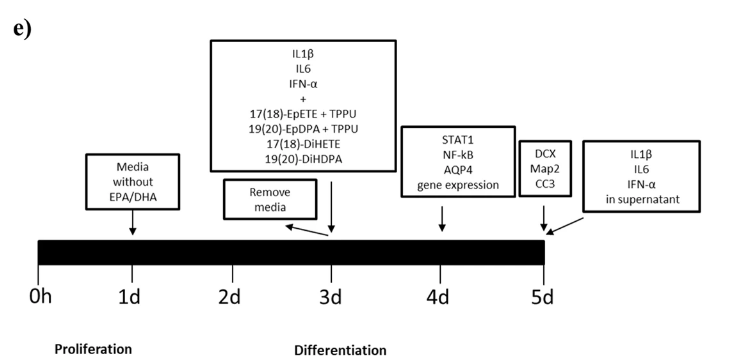
ω-3 PUFAs酶的合成途径以及ω-3 PUFAs和衍生脂质媒介物的实验时间表
具体来说,EPA在IL1β和IFN-α炎症细胞因子存在的情况下,阻止神经形成的减少(Map2+细胞),而DHA在三种炎症细胞因子存在的情况下都对神经起作用。此外,EPA阻止了IL1β和IL6引起的细胞凋亡的增多(CC3+细胞),而DHA在IL1β和IFN-α存在的情况下对细胞凋亡起作用。
EPA作为一种抗炎剂,能够抑制与先天免疫反应有关的机制,从而发挥其抗细胞凋亡的特性。DHA具有更多的神经保护作用,用DHA疗法可以阻止由IL1β炎症细胞因子引起的神经形成减少。
EPA和DHA的功能存储在细胞膜上,换句话说,ω-3 PUFAs通常储存在细胞膜中,是膜复合体的基本结构成分。在炎症或应激刺激的情况下,ω-3 PUFAs可以改变表面受体的表达,调节膜基细胞反应。LOX、CYP450羟化酶和环氧酶脂质介质是EPA或DHA存在的情况下,通过IL1β、IL6或IFN-α炎症细胞因子刺激下产生的,但在单独使用EPA或DHA预处理过程中不产生。
总之,研究证实并扩展了关于EPA和DHA的抗抑郁、抗炎和神经保护能力的证据,并确定LOX衍生的5-HEPE和4-HDHA以及CYP450衍生的18-HEPE、20-HDHA、17(18)-EpETE和19(20)-EpDPA是ω-3 PUFAs效应的媒介,进一步证实这些代谢物在接受EPA或DHA治疗抑郁症患者血浆中增加(同时抑郁症状得到改善)。
本研究中使用的EPA和DHA水平很可能是饮食消耗的鱼类(ω-3 PUFA的丰富来源)无法达到的浓度,需要治疗性补充剂补充。
原文出处:
https://www.nature.com/articles/s41380-021-01160-8


