瑞基仑赛(Relma-cel)对于R/R DLBCL患者表现出突破性疗效
时间:2021-07-27 23:25:16 热度:37.1℃ 作者:网络
 2021 CAR-T细胞治疗大会专题讲座——从CAR-T工艺开发到临床获益看瑞基仑赛(Relma-cel)于3月5日下午正式在江苏徐州召开,国内顶级血液肿瘤大咖通过线上线下联动共同予会。本场专题会由徐州医科大学血液病研究所徐开林教授的主持,浙江大学医学院附属第一医院胡永仙教授进行详尽的汇报。
2021 CAR-T细胞治疗大会专题讲座——从CAR-T工艺开发到临床获益看瑞基仑赛(Relma-cel)于3月5日下午正式在江苏徐州召开,国内顶级血液肿瘤大咖通过线上线下联动共同予会。本场专题会由徐州医科大学血液病研究所徐开林教授的主持,浙江大学医学院附属第一医院胡永仙教授进行详尽的汇报。

徐州医科大学血液病研究所徐开林教授
R-CHOP方案是DLBCL治疗的“金标准”,但35%~40%患者对传统R-CHOP耐药或复发[1],R/R DLBCL患者预后不佳[2],可选择的治疗方案十分受限。CAR-T细胞疗法对传统治疗束手无策的R/R DLBCL患者表现出了突破性的疗效,为DLBCL患者带来了新的希望。
胡永仙教授在汇报中表示,CAR-T细胞疗法已成为肿瘤治疗领域研究的重点。由于受工艺稳健性和一致性以及小批量多批次的生产模式的严格限制,CAR-T细胞疗法的产业化规模一直受到挑战。另外,中国虽然是CAR-T研发大国,但国内长期以来欠缺上市的CAR-T产品。

浙江大学医学院附属第一医院胡永仙教授
瑞基奥仑赛(Relma-cel):先进的产品及工艺设计
瑞基奥仑塞(Relma-cel)是在美国JUNO公司Liso-cel(JCAR017 )工艺平台基础上,自主研发的一款靶向CD19的自体CAR-T细胞产品。本次汇报中,胡永仙教授从产品设计、工艺平台和整体控制系统的优势以及当前临床研究结果等方面详细解读了瑞基奥仑塞的应用价值及前景。
瑞基奥仑赛使用4-1BB作为共刺激域。在一些体内外研究中,4-1BB共刺激域显示出了更好的安全性和有效性,相较于CD28共刺激域,基于4-1BB共刺激域的CAR-T细胞在体内续存时间更长[3,4]。
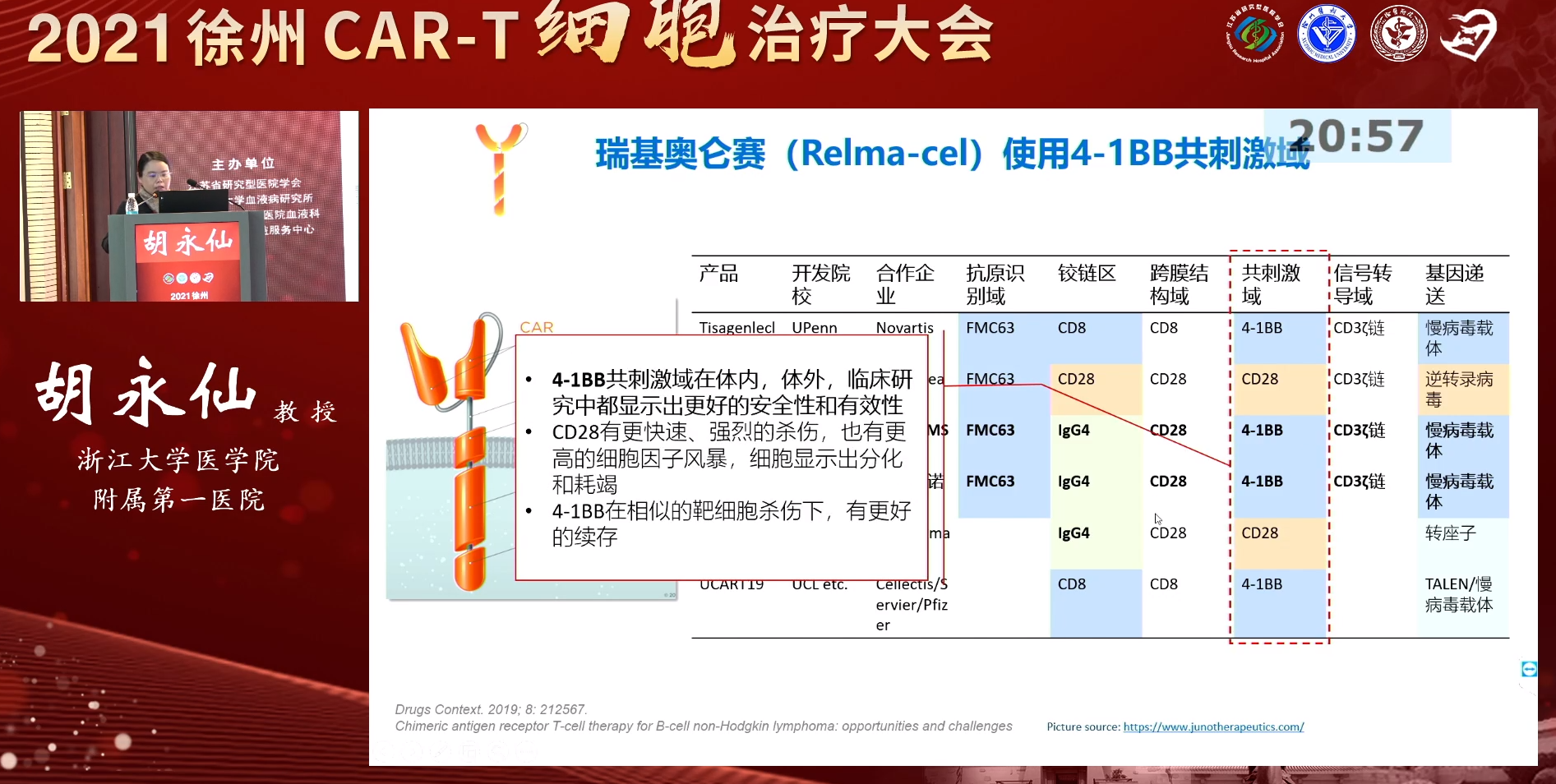 此外,瑞基奥仑赛采用T细胞纯化、冻存、慢病毒载体、动态扩增等先进且成熟的生产工艺和技术,确保工艺的稳健性和生产成功率;面对自体细胞产品生产的挑战,瑞基奥仑赛采用全程自动化、封闭的生产工艺,且在整体化的工艺和质量控制策略方面,保证了产品生产的可控性和质量的一致性,实现规模化生产。
此外,瑞基奥仑赛采用T细胞纯化、冻存、慢病毒载体、动态扩增等先进且成熟的生产工艺和技术,确保工艺的稳健性和生产成功率;面对自体细胞产品生产的挑战,瑞基奥仑赛采用全程自动化、封闭的生产工艺,且在整体化的工艺和质量控制策略方面,保证了产品生产的可控性和质量的一致性,实现规模化生产。

瑞基奥仑赛(Relma-cel):RELIANCE试验,为R/R DLBCL患者带来新选择
瑞基奥仑赛关键性临床试验(RELIANCE)II期结果已于2020年ASH大会公布[5],试验对69例患者进行了筛选,其中59例R/R DLBCL患者成功入组并接受了瑞基奥仑赛治疗,中位年龄为56.0岁(18~75)。患者随机接受两种不同剂量瑞基奥仑赛治疗(分别为100×106或150×106CAR-T细胞)。主要终点为研究者评估的3个月ORR,次要终点为研究者评估的最佳缓解率(BOR)、研究者评估的3个月完全缓解率(CRR)、不良事件(AE)、疾病控制率(DOR)、总生存(OS)等。
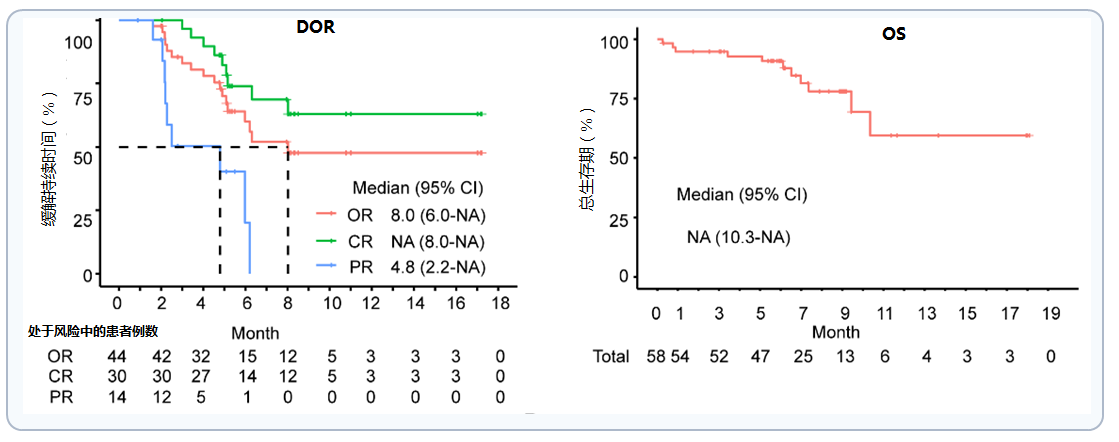
 数据截至2020年6月17日,在58例可评估有效性的患者中,最佳ORR为75.9%(95% CI,62.8 ~ 86.1),最佳CR为51.7%(95% CI,38.2 ~ 65.1)。3个月时ORR(主要终点)为60.3%(95%CI:46.6%,73%),CR率44.8% (95%CI:31.74%,58.46%)。
数据截至2020年6月17日,在58例可评估有效性的患者中,最佳ORR为75.9%(95% CI,62.8 ~ 86.1),最佳CR为51.7%(95% CI,38.2 ~ 65.1)。3个月时ORR(主要终点)为60.3%(95%CI:46.6%,73%),CR率44.8% (95%CI:31.74%,58.46%)。

患者首次达CR的中位时间为0.95个月,中位随访时间8.9个月,未达到中位OS,中位PFS和DOR分别为7.0个月(95%CI:5.5~NA)和8.0个月(95%CI: 5.09~NA)。
瑞基奥仑赛(Relma-cel):安全性表现优异
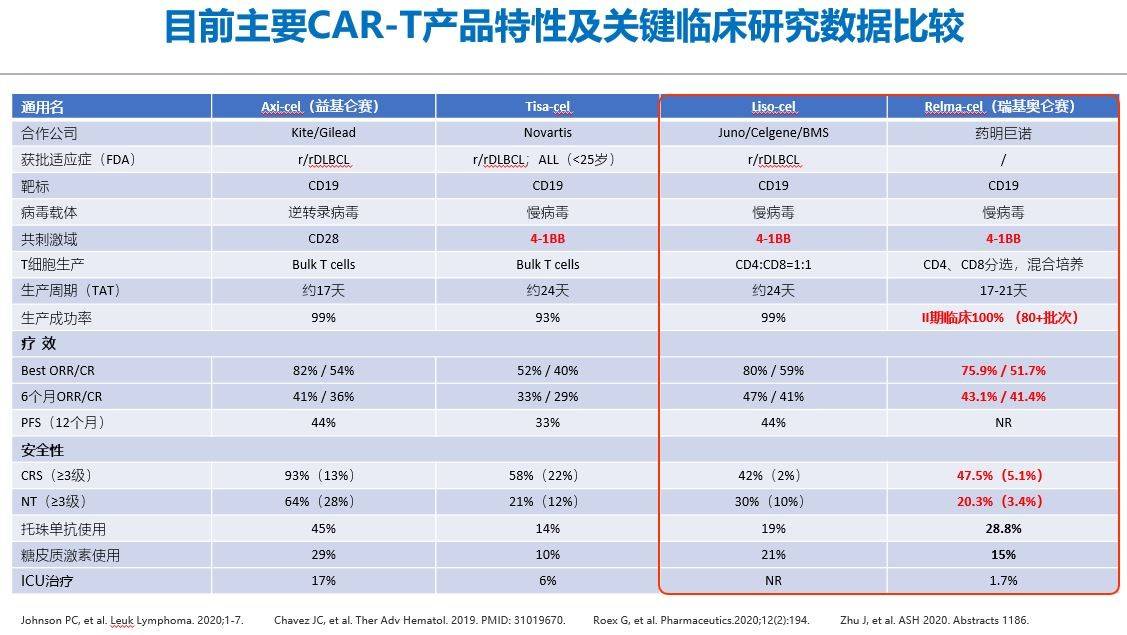
安全性分析显示,在59例接受治疗的患者中,28例患者(47.5%)出现了不同等级的细胞因子释放综合征(CRS),12例患者(20.3%)出现了神经系统毒性(NT),≥3级CRS和NT发生率仅为5.1%和3.4%。
RELIANCE试验是首个使用中国制造的,符合临床试验生产标准的CAR-T产品,并用于中国复发/难治性(r/r)大B细胞淋巴瘤(LBCL)患者的临床研究。与在美国和欧盟获批的其他特异性CD19 CAR-T药物相比,瑞基奥仑赛显示了类似的初步缓解率,且在接受既往重度治疗且风险较高的r/r LBCL患者中的安全性可能会更好。
在随后的讨论环节,徐州医科大学附属医院黄一虹教授针对RELIANCE研究数据以及瑞基奥仑赛的应用优势等话题与胡永仙教授展开热烈讨论,进一步加深了大家对这一CAR-T产品的认识。
鉴于瑞基奥仑赛靶向CD19 CAR-T成熟的生产工艺技术,以及2020年ASH大会公布的优秀临床数据,相信瑞基奥仑赛日后必将为我国R/R DLBCL带来新的治疗选择。作为获得中国首个以CD19为靶点的临床研究批件 并获国家重大新药创制专项支持的CAR-T细胞产品,瑞基奥仑赛于2020年9月被国家药品监督管理局授予新药申请优先审查资格,现已进入最后审评阶段。我们期待瑞基奥仑赛能早日获批,尽早解决患者“燃眉之急”,同时也期待能有更多临床研究数据公布,瑞基奥仑赛能获批更多适应证,为更多患者带来获益。
参考文献[1]. Sarkozy Clémentine, Sehn LH, et al. Ann Lymphoma 2019;3:10.
[2]. Crump M, Neelapu SS, et al. Blood 2017;130(16):1800-8.
[3]. Kawalekar OU, et al. Immunity. 2016;44(2):380-390.
[4]. Long AH, et al. Nat Med.2015;21(5):581-590.
[5]. Zhu J, et al. ASH 2020. Abstracts 1186


