Antioxidants:GLP-1类似物利拉鲁肽通过减少氧化应激和炎症改善脓毒血症影响的血管功能
时间:2021-11-11 17:02:18 热度:37.1℃ 作者:网络

背景及目的:利拉鲁肽是一种长效胰高血糖素样肽-1 (GLP-1)的类似物,在食物摄取后释放,参与葡萄糖的调节。天然GLP-1及其类似物(如利拉鲁肽、司美格鲁肽和阿必鲁肽)刺激胰腺β细胞释放胰岛素,但由于GLP-1受体(GLP-1R)不仅在胰腺中表达,它们也对其他器官/组织产生影响。旨在测试GLP-1类似物新型抗糖尿病药物心血管安全性的临床试验令人惊讶地发现,与标准治疗相比,长效GLP-1类似物治疗2型糖尿病可减少心血管事件。其机制尚不完全清楚,但一些临床和临床前研究表明GLP-1类似物有抑制炎症的作用。脓毒血症可导致感染性休克的高死亡率。Leader和其他试验揭示了胰高血糖素样肽-1(GLP-1)类似物如利拉鲁肽(LIRA)的心脏保护和抗炎特性。我们先前证明,通过抑制GLP-1的降解,可以改善脂多糖(LPS)诱导的内毒素中的存活率。在此,我们研究了LIRA在盲肠结扎穿孔(CLP)脓毒血症模型中的作用。
方法:实验采用三组小鼠:对照组(B6J)、盲肠结扎穿刺脓毒血症小鼠(CLP)和利拉谷肽治疗组(CLP+Lira)。在CLP治疗前一天开始腹腔注射利拉鲁肽(100µ/kg)或生理盐水(对照剂,对B6J和CLP组足够的体积),并持续至安乐死,每天两次,每12小时一次。CLP诱导脓毒血症后共48小时。麻醉后用氯胺酮/氧拉嗪(氯胺酮120 mg/kg和氧拉嗪16 mg/kg, 0.9% NaCl)穿刺心脏处死动物。心脏,主动脉和血液都被采集。使用罗氏公司(Basel, Schweiz)的ACCU-CHEK传感器系统评估全血葡萄糖水平。在治疗和安乐死之前,研究人员称了这些老鼠的体重,并用红外温度计测量了它们的体温。红外温度计用于测量来自法国维罗勒斯的小型啮齿动物(如图1所示)。
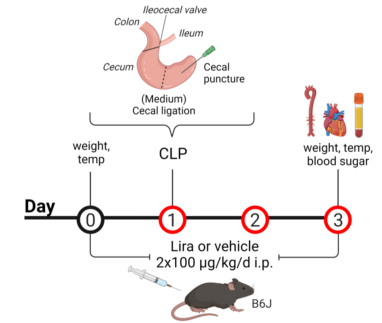
图1 治疗方案和盲肠结扎穿孔(CLP)手术。雄性C57BL/6J小鼠腹腔注射利拉鲁肽(Lira)或溶媒(生理盐水),每天2次,每12小时1次,连续3天。利拉的剂量为2×100µg/kg/d或足够的体积。首次给药后一天,在回盲瓣下方的中间位置结扎盲肠,然后进行盲肠穿孔(穿孔),造成中度脓毒血症。
为了研究血管反应性,从小鼠的主动脉中解剖并清除血管周围脂肪。切开4 mm的胸主动脉段,安装在器官浴腔内的力传感器上。这些环受到80 mm的KCl团注,清洗,并进行收缩曲线,以响应浓度增加的去极化KCl。为了测试血管对内皮依赖性血管扩张剂乙酰胆碱(ACh)和非内皮依赖性血管扩张剂硝酸甘油(NTG)的反应,用2µM前列腺素F2α收缩血管,使其产生约70-80%的最大张力,并记录浓度-弛张曲线
综上所述,C57BL/6J小鼠腹腔注射Lira(200µg/kg/d,3d),经GLP-1类似物处理1d后,用CLP诱导脓毒血症。监测存活率和体温。检测主动脉血管功能(等长张力记录)、蛋白表达(免疫组化和斑点杂交)和基因表达(qRT-PCR)。
结果:脓毒血症小鼠CLP损害了主动脉的内皮依赖性舒张,并与炎症标志物(如白细胞介素-6和诱导型一氧化氮合酶)相关,氧化应激(如3-硝基酪氨酸)升高,但经Lira治疗后几乎完全恢复正常。我们证明GLP-1类似物LIRA通过减少血管炎症和氧化应激来改善脓毒血症引起的内皮功能障碍。
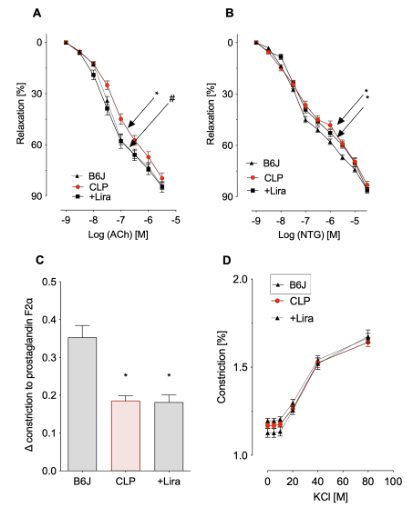
图2 用GLP-1受体激动剂利拉鲁肽治疗可预防CLP诱导的脓毒血症小鼠的内皮功能障碍。在等长张力记录中测定胸主动脉环(A,B)内皮依赖性(乙酰胆碱,ACh)和非内皮依赖性(硝酸甘油,NTG)舒张功能。(C,D)2-μ-M-前列腺素F2-α和增加KCl浓度引起的血管收缩反应。数据是22-34(A)、21-35(B)或26-36(C、D)独立测量的平均值±SEM。*p<0.05 vs.b6j;#p<0.05 vs.CLP。图2.用GLP-1受体激动剂利拉鲁肽治疗可预防CLP诱导的多菌脓毒症小鼠的内皮功能障碍。在等长张力记录中测定胸主动脉环(A,B)内皮依赖性(乙酰胆碱,ACh)和非内皮依赖性(硝酸甘油,NTG)舒张功能。(C,D)由2µM前列腺素F2α和增加KCl浓度引起的血管收缩反应。数据是22-34(A)、21-35(B)或26-36(C、D)独立测量的平均值±SEM。*p<0.05 vs.b6j;#p<0.05 vs.CLP
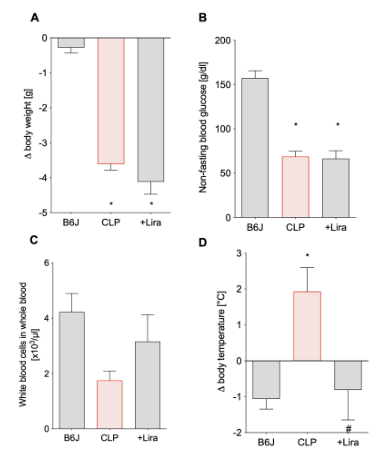
图3 用GLP-1受体激动剂利拉鲁肽治疗,可以在不改变脓毒血症小鼠血糖水平的情况下,预防CLP引起的白细胞减少和体温升高的并发症。(A,D)分别于第0天和第3天称重,测体温,测定Δ体重和Δ体温。(B,C)在脓毒血症诱导后2天检测非空腹血糖水平和全血白细胞计数。数据是来自单个动物或6个单个血液样本(每个样本由3到4只小鼠混合)的22-26(A)、19-22(B)和16-24(D)测量的平均值±SEM(C)。*p<0.05 vs.b6j;#p<0.05 vs.CLP。图3.用GLP-1受体激动剂利拉鲁肽治疗多菌性脓毒症小鼠,可在不改变血糖水平的情况下预防CLP引起的白细胞减少和高热并发症。(A,D)分别于第0天和第3天称重,测体温,测定∆体重和∆体温。(B,C)在脓毒血症诱导后2天检测非空腹血糖水平和全血白细胞计数。数据是来自单个动物或6个单个血液样本(每个样本由3到4只小鼠混合)的22-26(A)、19-22(B)和16-24(D)测量的平均值±SEM(C)。*p<0.05 vs.b6j;#p<0.05 vs.CLP

表1 血液参数。数据是5-7个个体血液样本的平均值±SEM(每个样本来自3 - 4只小鼠)。*p< 0.05 vs. B6J。
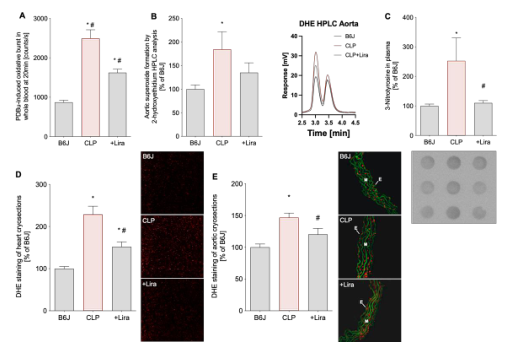
图4 用GLP-1受体激动剂利拉鲁肽治疗可降低CLP诱导的脓毒血症小鼠的血管、心脏和全身氧化应激。(A)用化学发光法测定佛波酯(PDBu)刺激后的全血氧化爆发(L-012)。(B)超氧化物特异的DHE产物2-羟乙基在主动脉组织中被定量,并以B6J对照组的百分比表示。除了定量外,还显示了具有代表性的色谱图。(C)用斑点印迹法检测过氧亚硝酸根形成后血浆中3-硝基酪氨酸(3-NT)阳性蛋白的含量。在密度量化图下面显示了一幅代表性的图像。(d,E)心脏和主动脉冰冻切片用二氢乙锭染色,显示ROS的形成为红色荧光,主动脉板层的自身荧光为绿色。在密度分析旁边显示了具有代表性的显微照片。E为内皮细胞,M为中层细胞。数据是6个单独的血液样本(每个从3到4只小鼠混合)(A)、6-8个(B)和4个(D,E)的个体血液样本或4个单独的血浆样本(每个从3到4个小鼠混合)的平均值扫描电镜(C)。*p<0.05 vs.b6j;#p<0.05 vs.CLP。

图5.用GLP-1受体激动剂利拉鲁肽治疗脓毒血症小鼠可抑制CLP诱导的血管炎症。定量RTPCR检测主动脉组织中白细胞介素6(IL6)、诱导型一氧化氮合酶(INOS)、肿瘤坏死因子α(TNFα)和细胞间黏附分子1(IMAM 1)的基因表达水平。免疫组织化学方法检测主动脉(E,F)3-NT阳性蛋白丰度和NOX2蛋白表达。有代表性的免疫组织化学图像显示在密度定量的旁边。放大倍数为40倍,刻度条为50µm。数据为3个个体样本(A-D)或3个个体动物(E,F)的平均值±扫描电镜(每个样本由3至4只小鼠组成)。*p<0.05 vs.b6j;#p<0.05 vs.CLP
结论:GLP-1类似物的抗氧化和抗炎作用可能是保护心血管系统免受脓毒血症时失衡炎症反应的一种有价值的工具。
原文出处:
Helmstädter J, Keppeler K, Aust F,et al.GLP-1 Analog Liraglutide Improves Vascular Function in Polymicrobial Sepsis by Reduction of Oxidative Stress and Inflammation.Antioxidants (Basel) 2021 Jul 23;10(8)


