Cell:中科院刘光慧教授揭示早衰的关键驱动信号
时间:2021-11-16 23:07:40 热度:37.1℃ 作者:网络
来自中国科学院生物物理研究所刘光慧研究员、美国国立卫生研究院的研究人员细胞生物学家Tom Misteli博士,开发出了一种基于细胞的高通量、高内涵成像小干扰RNA(siRNA)筛选方法,利用这一系统确定了抗氧化NRF2信号通路是早年衰老综合症(Hutchinson-Gilford progeria syndrome,HGPS)的一个驱动机制。这项重要的研究发布在6月2日的《细胞》(Cell)杂志上。同期Cell配有评论。
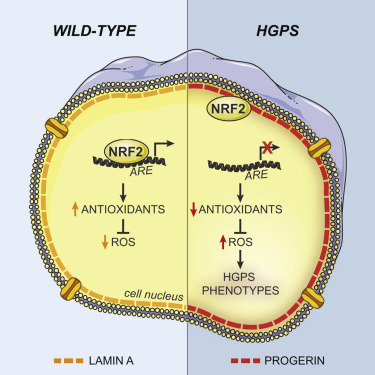
衰老是与许多常见疾病,包括癌症和心血管疾病相关的一个基本的生物学过程。自然发生的人类早衰疾病HGPS是研究人类衰老的一个强大工具。HGPS患者患者患有动脉粥样硬化,显示出多种早衰症状,寿命严重缩短。在细胞水平上,HGPS细胞显示异常的核结构、基因组失稳定以及氧化还原稳态改变。
在HPGS中,核结构蛋白lamin A和C的编码基因LMNA发生新生突变,激活了一个选择性前体mRNA (pre-mRNA)剪接位点,导致表达一种缺失50个氨基酸的lamin A突变体——progerin,其累积于核膜上。有研究发现Progerin在野生型的衰老细胞中累积,表明它有可能也与正常衰老相关联。
Progerin以一种显性方式发挥作用,可导致多种细胞缺陷,损害核结构的完整性、异染色质维持、DNA修复和氧化还原稳态,这被归因为降低了这些信号通路中一些关键蛋白质的水平。而Progerin功能多效应使得鉴别出HGPS的治疗靶点变得复杂。
在这篇Cell文章中,研究人员采用高通量的siRNA筛查方法,确定了NRF2抗氧化信号通路是HGPS中的一个驱动机制。Progerin隔绝NRF2,由此使得它亚核错误定位,导致了NRF2转录活性受损,由此提高了长期氧化压力。抑制NRF2活性或提高氧化压力足以重演HGPS老化缺陷,而在HGPS患者中重新激活NRF2活性可逆转progerin相关的核老化缺陷,恢复动物模型中间充质干细胞(MSCs)体内活力。
这些研究结果确定了抑制NRF2介导的抗氧化反应是早衰表型的一个关键促进因素。
这些研究结果不仅有助于加深人们对于人类衰老的认识,而且为延缓衰老及防治衰老相关疾病提供了新的靶标和策略。Cell杂志同期发表的Leading Edge Previews,题目为Dangerous Entrapment for NRF2,指出,“确立progerin和NRF2的功能联系将有益于通过靶向激活NRF2通路以改善儿童早衰症的治疗。例如,激活NRF2能通过降低活性氧和炎症反应以降低血管动脉粥样硬化(儿童早衰症的主要死因)的发生,激活NRF2也可能通过改善间充质干细胞中的氧化还原稳态以提高细胞的基因组稳定性,从而防止干细胞在体内的加速耗竭”。
奥替普拉(Oltipraz)作为一种NRF2激动剂(原本是一种古老的抗血吸虫药物),已经被FDA批准应用于治疗脂肪肝和肝纤维化的三期临床试验。研究人员发现这种小分子可以逆转儿童早衰症间充质干细胞加速衰老的表型,并能延缓其在体内的耗竭速度。这一方面使得Oltipraz可能存在新的用途可能。
该工作由中国科学院生物物理研究所、中国科学院动物研究所以及美国NIH等科研机构合作完成。生物物理所研究员刘光慧和美国国家癌症研究所教授Tom Misteli为论文的共同通讯作者。动物所研究员曲静和生物物理所副研究员张维绮为论文的共同高级作者(co-senior author)。生物物理所博士研究生王丽霞和杨济平参与了研究工作。该研究受到国家自然科学基金委、科技部“973”项目、中科院先导项目以及中科院生物大分子科教融合卓越创新中心的资助。
刘光慧研究员的主要研究方向包括基于人多能干细胞的人类疾病模型和药物筛选系统,疾病特异iPSCs的基因纠正,人类衰老和长寿的分子机理以及细胞核结构、染色体组织和人类疾病。近年在Nature、Science等国际权威杂志上发表了多项重要的研究成果。
2012年,刘光慧和美国索尔克生物研究所的Juan Carlos Izpisua Belmonte教授合作,利用人类干细胞证实细胞核缺陷有可能在帕金森氏病中发挥重要作用,指出了治疗这一疾病的新途径。相关论文发表在Nature杂志上(Nature:帕金森病衰老机制首次被揭示)。
在2015年4月Science杂志上的一项研究中,刘光慧研究员、北京大学生命科学学院的汤富酬研究员以及Salk生物科学研究所的Juan Carlos Izpisua Belmonte教授,将衰老过程与紧密包装的细胞DNA束解体联系到了一起,这有可能促成一些方法预防及治疗如癌症、糖尿病和阿尔茨海默氏症等年龄相关的疾病(Science:中国学者采用成年早衰症干细胞模型揭示衰老的分子机制)。
原始出处:
Repression of the Antioxidant NRF2 Pathway in Premature Aging.
Kubben N, Zhang W, Wang L, Voss TC, Yang J, Qu J, Liu GH, Misteli T.
Cell. 2016 Jun 2;165(6):1361-74.
关于刘光慧 研究员 
简历 & 研究组工作摘要
1997-2002 北京大学医学部,药理学学士
2002-2007 中国科学院生物物理研究所,理学博士
2007-2009 美国斯科利普斯(Scripps)研究所 Research associate
2009-2011 美国索尔克(Salk)生物学研究所 Research associate
2011-2018 中科院生物物理研究所,研究员,博士生导师
2019- 中科院动物研究所,研究员,博士生导师
学术任职
中国老年医学学会基础与转化医学分会副会长
中国老年学会衰老与抗衰老科学委员会副主任委员
中国细胞生物学学会干细胞生物学分会委员
中国医促会出生缺陷精准医学分会委员
中国生物物理学会理事
Protein & Cell杂志副主编
代表性论文
1. Liu GH, Barkho BZ, Ruiz S, Diep D, Qu J, Yang SL, Panopoulos AD, Suzuki K, Kurian L, Walsh C, Thompson J, Boue S, Fung HL, Sancho-Martinez I, Zhang K, III JY, Belmonte JC. Recapitulation of premature ageing with iPSCs from Hutchinson-Gilford progeriasyndrome. Nature. 2011; 14;472: 221-5.
Highlighted by “Faculty of 1000” (http://f1000.com/13411976)
2. Liu GH*, Suzuki K*, Qu J*, Sancho-Martinez I, Yi F, Li M, Kumar S, Nivet E, Kim J, Soligalla RD, Dubova I, Goebl A, Plongthongkum N, Fung HL, Zhang K, LoringJ,Laurent L, and Belmonte JC. Targeted gene correction of laminopathy-associated LMNA mutations in patient-specific iPSCs.Cell Stem Cell. 2011; 8(6):688-94. (*equal contribution)
Highlighted by Nature (Nature 474,8. doi:10.1038/474008c)
Highlighted by Cell Stem Cell (Cell Stem Cell 9, 2: 93-94)
3. Li M*, Liu GH*, Belmonte JC. Navigating the epigenetic landscape of pluripotent stem cells. Nat Rev Mol Cell Biol.2012; 13:524-35. (*equal contribution)
4. Liu GH#, Qu J, Suzuki K, Nivet E, Li M, Montserrat N, Yi F, Xu X, Ruiz S, Zhang W, Ren B, Wagner U, Kim A, Li Y, Goebl A, Kim J, Soligalla R, Dubova I, Thompson J, Yates J III, Esteban C, Sancho-Martinez I, Belmonte JC#. Progressive degeneration of human neural stem cells caused by pathogenic LRRK2. Nature. 2012; 491:603-7. (#Corresponding author)
Highlighted by Nature Reviews Neurology (doi:10.1038/nrneurol.2012.230)
5. Liu GH#, Ding Z, Izpisua Belmonte JC#. iPSC technology to study human aging and aging-related disorders. CurrOpin Cell Biol. 2012; 24:765-74. (#Corresponding author)
6. Giorgetti A, Marchetto MC, Li M, Yu D, Fazzina R, Mu Y, Adamo A, Paramonov I, Cardoso JC, Monasterio MB, Bardy C, Cassiani-Ingoni R, Liu GH, Gage FH, Izpisua Belmonte JC. Cord blood-derived neuronal cells by ectopic expression of Sox2 and c-Myc. ProcNatlAcadSci U S A. 2012; 109(31):12556-61.
7. Xu X, Duan S, Yi F, Ocampo A, Liu GH#, Belmonte JC#. Mitochondrial regulation in pluripotent stemcells. Cell Metab. 2013. Sep 3;18(3):325-32. (#Corresponding author)
8. Zhang WQ, Qu J, Suzuki K, Liu GH#, Belmonte JC#.Concealing cellular defects in pluripotent stem cells. Trends Cell Biol. 2013. 23(12):587-92. (#Corresponding author)
9. Pan H, Cai N, Li M, Liu GH#, Izpisua Belmonte JC#. Autophagic control of cell stemness. EMBO Mol. Med. 2013. 5:327-31. (#Corresponding author)
10. Guan D, Zhang W, Zhang W, Liu GH#, Belmonte JC#. Switching cell fate, ncRNAs coming to play. Cell Death Dis. 2013. 4:e464.(#Corresponding author)
11. Yang J, Cai N, Yi F, Liu GH#, Qu J#, Belmonte JC#. Gating pluripotency via nuclear pores. Trends Mol Med. 2014. Jan; 20(1):1-7.(#Corresponding author)
Cover story in Trends Mol Med (CELL PRESS) 2014, issue 1
12. Wu K, Ren R, Su W, Wen Bo, Zhang Yuying, Yi Fei, Qiao X, Yuan T, Wang J, Liu L, Belmonte JC#, Liu GH#, Chen C#. A novel suppressive effect of alcohol dehydrogenase 5 in neuronal differentiation. J Biol Chem. 2014. 289(29):20193-9. (#Corresponding author)
13. Liu GH#, Suzuki K, Li M, Qu J, Montserrat N, Tarantino C, Gu Y, Yi F, Xu X, Zhang W, Ruiz S, Plongthongkum N, Zhang K, Masuda S, Nivet E, Tsunekawa Y, Soligalla R, Goebl A, Aizawa E, Kim N, Kim J, Dubova I, Li Y, Ren R, Benner C, del Sol A, Bueren J, Trujillo J, Surralles J, Esteban C, Izpisua Belmonte JC#. Modeling Fanconi Anemia pathogenesis and therapeutics using integration-free patient iPSCs.Nat Commun. 2014. 7;5:4330. (#Corresponding author)
14. Suzuki K, Yu C, Qu J, Li M, Yao X, Yuan T, Goebl A, Tang S, Ren R, Aizawa E, Zhang F, Xu X, Soligalla R, Chen F, Kim J, Kim NY, Liao HK, Benner C, Esteban CR, Jin Y, Liu GH#, Li Y#, Belmonte JC#. Targeted gene correction in human disease-specific induced pluripotent stem cells minimally impacts whole-genome mutational load. Cell Stem Cell. 2014; 15, 31–36. (#Corresponding author)
Highlighted by Nature (Naturedoi:10.1038/nature.2015.17110)
Highlighted by Nature (Nature515,S11–S13(13 November 2014)doi:10.1038/515S11a)
Highlighted by Cell Stem Cell (Cell Stem Cell, July 3 (2014), doi: 10.1016/j.stem.2014.06.017)
Highlighted by Nature Methods (Nature Methods, 11, 894 (2014) doi:10.1038/nmeth.3090)
15. Reddy P, Ocampo A, Suzuki K, Luo J, Bacman SR, Williams SL, Sugawara A, Okamura D, Tsunekawa Y, Wu J, Lam D, Xiong X, Montserrat N, Esteban CR, Liu GH, Sancho-Martinez I, Manau D, Civico S, Cardellach F, Del Mar O'Callaghan M, Campistol J, Zhao H, Campistol JM, Moraes CT, Izpisua Belmonte JC.Selective Elimination of Mitochondrial Mutations in the Germline by Genome Editing. Cell. 2015; 161:459-469
Highlighted by Nature (Nature|doi:10.1038/nature.2015.17379)
Highlighted by Cell Stem Cell (Cell Stem Cell | doi:10.1016/j.stem.2015.04.012)
Highlightedby The Scientist
16. Zhang W, Li J, Suzuki K, Qu J, Wang P, Zhou J, Liu X, Ren R, Xu X, Ocampo A, Yuan T, Yang J, Li Y, Shi L, Guan D, Pan H, Duan S, Ding Z, Li M, Yi F, Bai R, Wang Y, Chen C, Yang F, Li X, Wang Z, Aizawa E, Goebl A, Soligalla RD, Reddy P, Esteban CR, Tang F#, Liu GH#, Belmonte JC#. A Werner syndrome stem cell model unveils heterochromatin alterations as a driver of human aging. Science. 2015; 348(6239):1160-3.(#Corresponding author)
Highlighted by Science (Science|5 JUNE 2015 VOL 348 ISSUE 6239)
Highlighted by Science (Science| DOI: 10.1126/science.aab2575)
Highlighted by TIME, Washington Post, Science News
Nature Reviews Genetics16,318(2015)doi:10.1038/nrg3958
17. Duan S, Yuan G, Liu X, Ren R, Li J, Zhang W, Wu J,Xu X, Fu L, Li Y, Yang J, Zhang W, Bai R, Yi F, Suzuki K, Gao H, Esteban CR, Zhang C, Belmonte JC, Chen Z, Wang X,Jiang T, Qu J#,Tang F#, Liu GH#. PTENdeficiency reprograms human neuralstem cells towards a glioblastoma stem cell-like phenotype. Nat Commun. 2015. 6:10068. (#Corresponding author)
18. Pan H, Guan D, Liu X, Li J, Wang L, Wu J, Zhou J, Zhang W, Ren R, Zhang W, Li Y, Yang J, Hao Y, Yuan T, Yuan G, Wang H, Ju Z, Mao Z, Li J, Qu J#,Tang F#, Liu GH#. SIRT6 safeguards human mesenchymal stem cells from oxidative stress by coactivating NRF2. Cell Res.2016.26(2):190-205. (#Corresponding author)
Highlighted by Cell (DOI: http://dx.doi.org/10.1016/j.cell.2016.05.061)
Highlighted by Cell Res (Cell Res|doi: 10.1038/cr.2016.8)
19.Guo J, Fang W, Sun L, Lu Y, Dou L, Huang X, Sun M, Qu J#, Liu GH#, Li J#. Reduced miR-200b and miR-200c expression contributes to abnormal hepatic lipid accumulation by stimulating JUN expression and activating the transcription of srebp1. Oncotarget. 2016. doi: 10.18632/oncotarget.9183. (#Corresponding author)
20. Wang H, Diao D, Shi Z, Zhu X, Gao Y, Gao S, Liu X, Wu Y, Rudolph KL, Liu GH, Li T, Ju Z.SIRT6 Controls Hematopoietic Stem Cell Homeostasis through Epigenetic Regulation of Wnt Signaling. Cell Stem Cell. 2016. 7;18(4):495-507.
21. Kubben N, Zhang W, Wang L, Voss T, Yang J, Qu J, Liu GH#, Misteli T#, Repression of the antioxidant NRF2 pathway in premature aging.Cell. 2016. 165,1361-1374 (#Corresponding author)
Highlighted by Cell (DOI: http://dx.doi.org/10.1016/j.cell.2016.05.061)
Book chapter:
Liu GH#, Yang J, Ding Z, Ocampo A, Qu J, Suzuki K, Izpisua Belmonte JC#. Chapter: iPSC disease modeling of laminopathies. Human iPS Cells in Disease Modeling (Springer), 2016, pp 53-67 (#Corresponding author)


