BioDrugs:AVT02 VS. 原研药阿达木单抗在中重度慢性斑块状银屑病患者中的疗效、安全性和免疫原性
时间:2022-01-08 19:03:45 热度:37.1℃ 作者:网络
AVT02(阿达木单抗)是一种拟议的Humira®生物仿制药。AVT02的生产浓度为100毫克/毫升,采用不含柠檬酸盐的配方。近日,发表于BioDrugs的一项研究比较了AVT02与Humira®在中度至重度慢性斑块状银屑病患者中的疗效、安全性和免疫原性。

这项针对成人受试者的双盲、随机、平行组、主动对照研究,比较了AVT02与原研药阿达木单抗在第1周皮下注射80毫克,然后每隔一周注射40毫克的情况(按1:1的比例)。在第16周,接受原研药阿达木单抗的受试者按1:1的比例重新随机选择继续接受原研药阿达木单抗,或改用AVT02,每隔一周一次,直到第48周,最终疗效终点为第50周。最初接受AVT02的受试者从第16周到第48周继续接受AVT02。主要终点是第16周时银屑病面积和严重程度指数(PASI)评分的改善百分比。次要疗效终点包括在其他时间点PASI评分的改善百分比,皮肤病生活质量指数(DLQI)评分相对基线的变化,以及达到sPGA"清晰"或"几乎清晰"反应的受试者数量和百分比。其他次要终点包括比较不良事件概况、抗药性抗体和中和抗体,以及稳定状态下阿达木单抗的血清谷值水平。
结果,共有413名受试者接受随机分配(205名接受AVT02,208名接受原研者)。AVT02治疗的受试者在第16周的PASI评分改善百分比为91.6%,原研药阿达木单抗为89.6%。主要终点的90%置信区间在预定的±10%等值范围内(90% CI - 0.76至5.29;95% CI - 1.34至5.88),第16周DLQI评分(AVT02治疗组和原研药阿达木单抗治疗组分别改善11.4分和10.6分)和sPGA(两组都有90.5%的患者达到"清晰"或"几乎清晰")的可比模式支持该评估。所有治疗组,包括从原研药阿达木单抗转为AVT02的治疗组,在PASI评分、生活质量评估和sPGA的改善百分比方面,其疗效一直持续到研究的第50周。AVT02和原研药阿达木单抗的安全性、耐受性和免疫原性在第16周时相似,这种情况在转换组和继续组中一直持续到第50周。
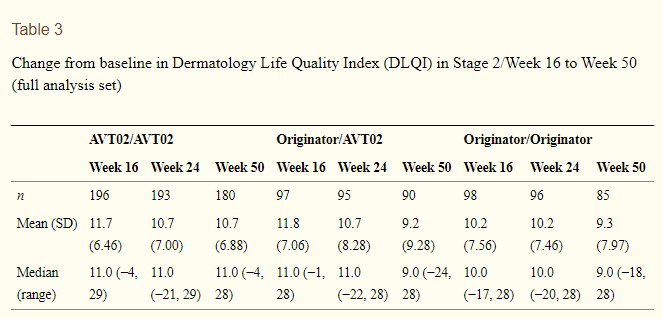
综上所述,该研究结果表明,客观和主观的疗效指标支持AVT02和原研药阿达木单抗在第16周和50周之前的生物相似性评价,在转换和继续治疗组中都是如此。AVT02的安全性和耐受性良好,其安全性和免疫原性与原研药阿达木单抗观察到的相似,两者之间没有临床意义上的差异。
原始出处:
Steven R Feldman, et al., Efficacy, Safety and Immunogenicity of AVT02 Versus Originator Adalimumab in Subjects with Moderate to Severe Chronic Plaque Psoriasis: A Multicentre, Double-Blind, Randomised, Parallel Group, Active Control, Phase III Study. BioDrugs. 2021 Nov;35(6):735-748. doi: 10.1007/s40259-021-00502-w.