控制情绪、影响神经,如何让肠道菌群重塑“心声”?
时间:2022-01-21 18:17:31 热度:37.1℃ 作者:网络

中枢神经系统获取周围世界信息的唯一方法是利用感官,尤其是充满数百万细菌的肠道。
肠道和大脑一直通过不同的渠道相互交流,它们也相互影响,比如紧张情绪通常会导致肠道不适感,同样,如果你没有很好地对待肠道菌群群,没有给它们提供茁壮成长和快乐生活所需的营养,你也会感到情绪低落。
所以可以认为,人的情绪和至少在某种程度上取决于肠道菌群,并且在某种程度上它们控制着大脑,这听起来可能有点儿可怕。但事实上,这种关系在20年前就被发现了,从那时起,它就成为了一个高产的研究领域,“肠-脑轴”有趣新闻一直未曾间断过。
近些年的研究表明,肠道菌群与大脑相互作用的途径有多种,要么通过细菌产生的代谢物,要么直接与神经相互作用。对于许多精神、神经性疾病的人,我们没有治愈方法,也不完全了解潜在的致病机制。而肠道菌群可能为这些疾病的治疗提供新见解。
同时,我们也已经开始查明可能对大脑产生积极或消极影响的肠道细菌有哪些。
什么是“菌群-肠-脑轴”
肠道菌群的代谢物直接影响肠道的免疫、内分泌和神经,肠道神经与大脑神经相连,三者互相交叉影响,并且这一影响是从胎儿时期就开始,贯穿一生的过程,不同年龄阶段有不同的表现。母亲的身体健康及肠道菌群状态会影响胎儿神经发育、脑免疫及血脑屏障功能发育。
婴儿出生后建立自己的肠道菌群,菌群继续影响大脑发育,且会持续至成年。肠道菌群通过消化食物,产生的短链脂肪酸、修饰胆汁酸等代谢物,可以通过肠上皮细胞或肠内分泌细胞向神经传递信号;还会产生多种神经递质如5-羟色胺、色氨酸、多巴胺等,神经递质经过体液循环进入大脑,直接影响大脑信号;肠道菌群影响下丘脑-垂体-肾上腺(HPA)轴控制的皮质酮生成,可以促进社交互动活动。
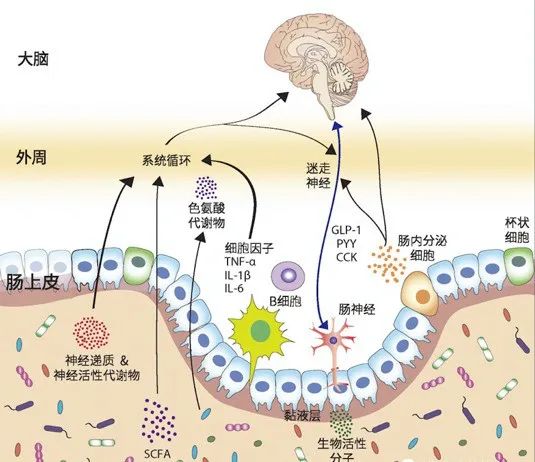
肠道菌群失调时,会释放大量炎症因子导致大脑及肠道的症状;中枢神经控制迷走神经和脊髓传出的神经信号到达肠道后,调节肠道菌群稳态和肠道内多种细胞的空间分布。因此形成了肠道菌群-肠-神经互相作用的复杂系统。
肠道菌群与肠、大脑的交流涉及到免疫调节、肝胆代谢、神经支配、肠内分泌、微生物代谢信号等,是一个非常复杂的过程,不断有新的研究被发现来完善其机制。
与菌群-肠-脑轴干预有关的神经性行为障碍
目前,很多研究发现,孤独症、抑郁症、焦虑症、精神分裂症、阿尔茨海默病等精神和神经系统疾病与菌群-肠-脑轴相关。例如,
孤独症
孤独症(ASD)是在一定遗传因素作用下,受多种环境刺激导致的中枢神经系统发育障碍性疾病,在2岁即可确诊,会有社交障碍、言语交流障碍、兴趣狭窄、刻板重复行为等明显的临床表现,部分患者会在音乐、机械记忆等方面有超常表现。
ASD患者常见有胃肠道并发症,许多研究发现ASD患者肠道菌群组成及代谢产物有显著变化,肠道菌群丰度降低,肠道内与抗体相关的菌群毒力因子增加。如果将孤独症患者的肠道菌群移植给无菌小鼠,会引起小鼠产生相似的孤独症症状。肠道菌群通过短链脂肪酸、色氨酸、胆汁酸等调节神经递质的产生,直接影响患者行为。在临床试验中,摄入益生菌会改善患者症状,将健康人菌群移植给患者也有症状改善。因此益生菌也逐渐被纳入孤独症治疗中。
抑郁症
对抑郁症患者与健康人的肠道菌群分析发现有显著差异,菌群多样性降低,抗炎细菌减少,有促进炎症的菌属增加,且菌群类型的变化幅度与抑郁症状的严重程度相关。炎症因子增多、神经递质调节失衡,进一步影响抑郁症的发生发展。改善饮食,摄入益生菌,对缓解抑郁症有积极作用。
双相情感障碍
双相情感障碍(BD)也是常见的精神障碍类型。浙大胡少华团队,通过对 BD 患者与健康人肠道菌群多样性及差异,以及治疗前后的肠道菌群变化进行分析,发现BD患者肠道菌群多样性降低,产丁酸菌属丰度下降,且不同菌种丰度与患者抑郁程度相关。因此对患者肠道菌群进行改善,可能会对病情产生积极作用。有抑郁症状的患者,选择富含膳食纤维的食物,定期补充益生菌,会十分有利于身体健康。
阿尔茨海默病
肠道菌群通过菌群-肠-脑轴对人体的调节贯穿一生。阿尔茨海默病(AD)是多发于老年人的神经系统退行性疾病,有失忆、失语、失去空间感等表现。威斯康辛大学的研究发现,AD患者肠道菌群多样性降低,双歧杆菌属减少,且菌种丰度差异与 AD 的病情相关。路易斯安娜州立大学的一项研究发现,AD 患者的脑中存在大量来源于肠道菌群的促炎症信号 LPS,说明随着衰老,毒素分子从肠道中进入血液循环,进入大脑,影响神经系统。
此外,多项研究还发现菌群失调引起的肠道及血脑屏障通透性升高会增加 AD 发病风险,益生菌干预可降低患 AD 风险。因此老年人定期服用益生菌有助于降低 AD 发病风险。
可能对大脑产生积极影响的细菌
通过对菌群-肠-脑轴的了解不断加深,通过调“肠”来控“脑”将会逐步成为现实。目前在脑肠轴领域的有深度研究的菌株包括:
长双歧杆菌SINE 001
长双歧杆菌SINE 001是我国首个经权威机构认定的益生菌标准菌株,在投入临床使用已经超过20年之久,具有超过1500篇的科学循证支撑,并且在众多疾病领域具有临床干预效果验证,尤其是消化、过敏、认知方面。
2020年中南大学湘雅三医院团队发表的一项临床试验(IF:7.324)表明,对于非心外科手术的老年患者,围手术期补充口服益生菌药物(含长双歧杆菌SINE 001、嗜酸乳杆菌、粪肠球菌),可能通过限制外周炎症和压力反应,减少术后认知损伤的发生,这为益生菌预防术后神经认知损失提供了新的可能性。
罗伊氏乳杆菌SINE 003
罗伊氏乳杆菌是近年来用于神经性疾病研究的大热菌株,超20篇精神健康相关高分文献循证证据表明,其可以干预神经递质合成分泌、影响迷走神经系统,缓解焦虑、提高认知、改善社会行为缺陷。
2021年《NeuroscienceResearch》发表研究表明:口服黄体酮或罗伊氏乳杆菌SINE003改善去卵巢小鼠肠道微生物群,抑制其抑郁和焦虑样行为。

植物乳杆菌P-8、SINE 002
植物乳杆菌 P-8 是科拓生物的专利菌株,拥有11项专利, 60多篇文献验证。科拓生物是中国益生菌行业首家上市企业,是中国益生菌第一股,具有近20年益生菌深耕经验。
内蒙古农业大学的张和平教授团队随机选取103名成年人进行心理、压力以及焦虑缓解的试验,发现植物乳杆菌P-8具有显著舒缓压力及焦虑,改善认知能力的作用。相比于安慰剂组,12周后益生菌组的压力、焦虑症状有明显改善,IFN-γ、TNF-α 等促炎因子的水平显著降低,同时记忆及认知能力也有提升。
植物乳杆菌SINE 002作为信谊3000多株菌种库中的明星菌株,已在微生态制剂使用30余年,安全可靠,目前多项临床研究正在开展中。
长双歧杆菌婴儿亚种R6
长双歧杆菌婴儿亚种R6分离自婴儿肠道原籍菌,可以充分利用双歧因子,并具有高效代谢母乳低聚糖(HMO)能力。
经过全基因组数据和安全性评价,该类菌株已有近1000篇文献支撑,发现其代谢产物能促进神经系统细胞发育,稳定营养平衡,增强免疫力。
总之,平衡的肠道菌群对精神、神经健康至关重要。我们需要了解更多关于肠道细菌如何影响我们的中枢神经系统的信息,去尝试寻找靶向肠道菌群改善或治疗精神神经系统疾病症状的方法。
※需要注意,对于精神神经性系统疾病的治疗还是需要谨遵医嘱。
参考文献
1. KaraG. Margolis, John F. Cryan, Emeran A. MayerThe Microbiota-Gut-Brain Axis: FromMotility to Mood. J Gastro.2020.160 (5):1486-1501.
2. LewL C , Hor Y Y et al. Probiotic Lactobacillus plantarum P8 alleviated stress andanxiety while enhancing memory and cognition in stressed adults: A randomised,double-blind, placebo-controlled study. Clin Nutr. 2019. 38(5):2053-2064.
3. Li N,Wang Q, Wang Y et al. Oral Probiotics Ameliorate the BehavioralDeficits Induced by Chronic Mild Stress in Mice via the GutMicrobiota-Inflammation Axis. Front Behav Neurosci. 2018; 12: 266.
4. AsmaKazemi, Ahmad Ali Noorbala, Kamal Azam et al. Effect of prebiotic andprobiotic supplementation on circulating pro-inflammatory cytokines and urinarycortisol levels in patients with major depressive disorder: A double-blind,placebo-controlled randomized clinical trial.J Funct Foods. 2019(52):596-602.
5. PingzhuWang,Xinlin Yin, Gong Chen et al. Perioperative probiotic treatment decreasedthe incidence of postoperative cognitive impairment in elderly patientsfollowing non-cardiac surgery: A randomised double-blind and placebo-controlledtrial. 2020.40(1):64-71.
6.Agirman G , Hsiao E Y . SnapShot: The microbiota-gut-brain axis[J]. 2021.
7.Jameson K G , Olson C A , Kazmi S A , et al. Toward UnderstandingMicrobiome-Neuronal Signaling[J]. Molecular Cell, 2020, 78(4).
8.Coretti L , Paparo L , Riccio M P , et al. Gut Microbiota Features inYoung Children With Autism Spectrum Disorders[J]. Frontiers in Microbiology,2018, 9.
9.Svoboda E . Could the gut microbiome be linked to autism?[J]. Nature, 2020,577(7792):S14-S15.
10.Rtl A , Rn B , Aes C , et al. Reductions in anti-inflammatory gutbacteria are associated with depression in a sample of young adults -ScienceDirect[J]. Brain, Behavior, and Immunity, 2020, 88:308-324.
11.Da Niels J K , Koopman M , Aidy S E . Depressed gut? Themicrobiota-diet-inflammation trialogue in depression[J]. Current opinion inPsychiatry, 2017:369.
12.Hu S , Li A , Huang T , et al. Gut Microbiota Changes in Patientswith Bipolar Depression[J]. Advanced Science, 2019, 6(14).
13.Vogt N M , Kerby R L , Dill-Mcfarland K A , et al. Gut microbiomealterations in Alzheimer's disease[J]. Scientific Reports, 2017, 7(1):P563.
14.Zhao Y , Cong L , Vivian J , et al. Microbiome-DerivedLipopolysaccharide Enriched in the Perinuclear Region of Alzheimer's DiseaseBrain[J]. Frontiers in Immunology, 2017, 8:1064-.
15.Xu H , Tao W , Feng J . Alzheimer's disease and gut microbiota[J].Science China(Life Sciences), 2016, 59(10):1006-1023.
16.Lew L C , Hor Y Y et al. Probiotic Lactobacillus plantarum P8 alleviated stressand anxiety while enhancing memory and cognition in stressed adults: Arandomised, double-blind, placebo-controlled study. Clin Nutr. 2019.38(5):2053-2064.


