Lancet Oncology:背靠背!吴一龙/周彩存团队发现舒格利单抗可治疗转移性/不可切除性非小细胞肺癌
时间:2022-01-31 17:18:20 热度:37.1℃ 作者:网络
肺癌是全球第二大最常诊断的癌症和癌症死亡的主要原因,每年占新发癌症的 11·4%和癌症死亡的18%。大约 80-90% 的原发性肺癌是非小细胞肺癌 (NSCLC),通常被诊断为转移性疾病,该阶段与预后不良相关。鳞状细胞癌占 NSCLC的20-30%,并且由于其独特的生物学和疾病特征,与非鳞状 NSCLC 相比,其生存期甚至更短。
几个 3 期试验表明抗 PD-1 或抗 PD-L1 抗体联合化疗作为一线治疗晚期鳞状或非鳞状NSCLC 患者的无进展生存期、总生存期或两者均显示出不同程度的益处。KEYNOTE-1895 和 KEYNOTE-4076 报告称,在化疗中加入抗 PD-1 抗体 pembrolizumab 与安慰剂加化疗相比,在未经治疗的非鳞状细胞癌的全身治疗中,总生存期和无进展生存期在统计学上显着延长非鳞状和鳞状非小细胞肺癌。


相反,抗 PD-L1 抗体 atezolizumab 在几项 3 期试验中显示出不确定的 NSCLC 生存获益。在 IMpower131 中,atezolizumab 联合卡铂-紫杉醇或卡铂-nab-紫杉醇作为鳞状 NSCLC 患者的一线治疗仅达到了一个共同主要终点(无进展生存期),并且总生存期没有改善。同样,在 IMpower132 试验中,atezolizumab 加卡铂-培美曲塞或顺铂-培美曲塞作为非鳞状 NSCLC 患者的一线治疗并未提高总生存期。POSEIDON 试验达到了其主要终点,显示 durvalumab 加化疗与单独化疗相比,无进展生存期有统计学意义的改善,但总生存期没有改善。因此,PD-L1抑制剂联合化疗作为晚期非鳞状和鳞状NSCLC一线治疗的疗效值得进一步评估和验证。
Sugemalimab(舒格利单抗,原名 CS1001)是一种靶向 PD-L1 的全长、全人免疫球蛋白 G4(IgG4、s228p)单克隆抗体。临床前研究表明,舒格利单抗保留与 Fcγ 受体 I 结构域的结合亲和力,这可以通过在肿瘤微环境中将表达 PD-L1 的肿瘤细胞与巨噬细胞交联来诱导抗体依赖性细胞吞噬作用,并可能进一步增强肿瘤抗原呈递。舒格利单抗的 1a/1b 期研究表明,单一疗法或与铂类化学疗法联合使用,在包括非鳞状和鳞状 NSCLC 在内的一系列肿瘤中产生了有希望的抗肿瘤活性。
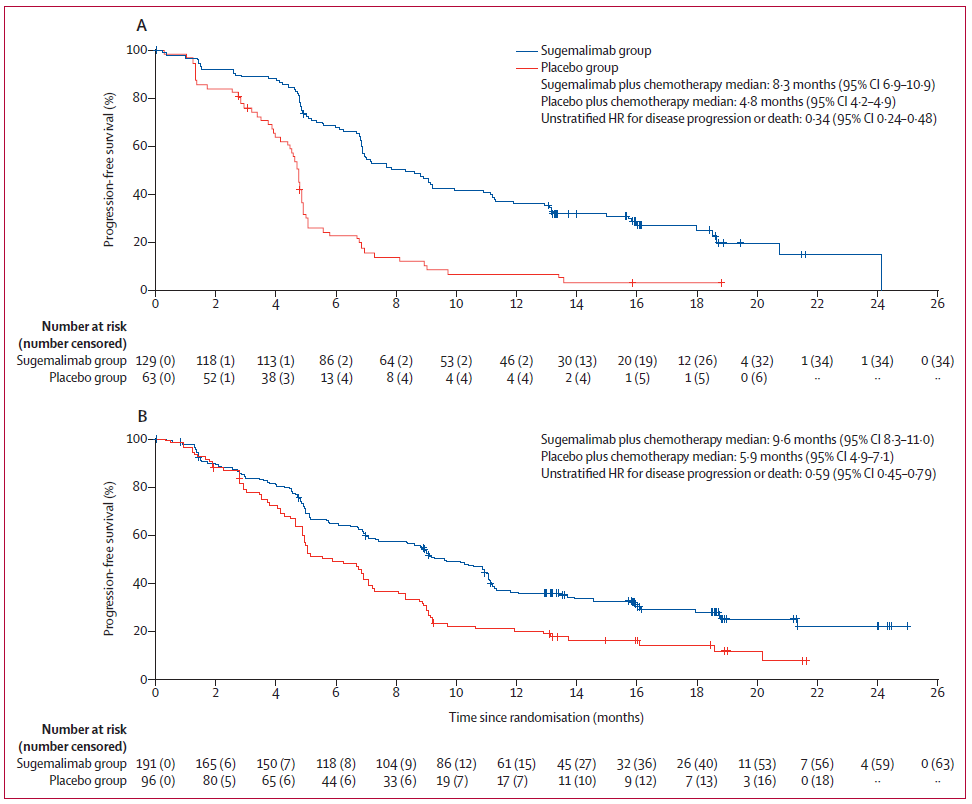
研究者评估的按肿瘤病理类型划分的患者无进展生存期的 Kaplan-Meier 图(图源自Lancet Oncology )
在这里,该研究报告了 GEMSTONE-302 试验的结果,包括预先设定的无进展生存期中期分析和最终无进展生存时间点,旨在进一步评估在非鳞状或鳞状转移性非小细胞肺癌患者一线铂类化疗中加入舒格利单抗的疗效和安全性。
这项随机、双盲、3 期试验在中国 35 家医院和学术研究中心进行。符合条件的患者年龄在 18-75 岁之间,经组织学或细胞学证实为 IV 期鳞状或非鳞状 NSCLC,没有已知的 EGFR 致敏突变、ALK、ROS1 或 RET 融合,既往无转移性疾病的全身治疗,以及东部肿瘤协作组(ECOG) 体能状态为 0 或 1。
患者被随机分配 (2:1) 接受舒格利单抗(1200 mg,静脉内,每 3 周一次)加铂类化疗(卡铂 [曲线下面积 (AUC) 5 mg/mL/min,静脉内] 和紫杉醇 [175 mg/m2,静脉内] 用于鳞状 NSCLC,或卡铂 [AUC 5 mg/mL/min,静脉内] 和培美曲塞 [500 mg/m2,静脉内] 用于非鳞状 NSCLC(舒美利单抗组)或安慰剂加与舒格利单抗组相同的铂类鳞状或非鳞状 NSCLC 化疗方案(安慰剂组),最多四个周期,随后对鳞状 NSCLC 使用舒格利单抗或安慰剂进行维持治疗,对非鳞状 NSCLC 使用 500 mg/m2 静脉注射舒格利单抗或匹配的安慰剂加培美曲塞。
随机化由交互式语音-网络响应系统通过置换块(块大小为 3 和 6 的混合,每个层内的随机顺序)完成,并按 ECOG 表现状态、PD-L1 表达和肿瘤病理学分层。研究人员、患者和申办者对治疗分配不知情。主要终点是意向治疗人群中研究者评估的无进展生存期。在接受至少一剂治疗的所有患者中分析了安全性。报告的结果来自预设的中期分析(即研究达到主要终点时)和更新的分析(预设的无进展生存期最终分析),随访时间更长。该研究已在 ClinicalTrials.gov (NCT03789604) 注册,不对新参与者开放,后续工作正在进行中。
在 2018 年 12 月 13 日至 2020 年 5 月 15 日期间,对 846 名患者进行了资格评估;367 名不合格,其余 479 名患者被随机分配到舒格利单抗组 (n=320) 或安慰剂组 (n=159)。在预先计划的中期分析中(数据截止日期为 2020 年 6 月 8 日;中位随访时间为 8·6 个月 [IQR 6·1-11·4]),GEMSTONE-302 达到了其主要终点,在舒格利单抗组与安慰剂组相比(中位 7·8 个月 [95% CI 6·9-9·0] vs 4·9 个月 [4·7-5·0];分层风险比 [HR] 0·50 [ 95% CI 0·39–0·64],p<0·0001])。在最终分析中(2021 年 3 月 15 日),中位随访时间为 17·8 个月(IQR 15·1-20·9),无进展生存期的改善得以维持(中位 9·0 个月 [95% CI 7·4–10·8] vs 4·9 个月 [4·8–5·1];分层 HR 0·48 [95% CI 0·39–0·60],p<0·0001)。
总生存期的 Kaplan-Meier 图(图源自Lancet Oncology )
最常见的 3 级或 4 级任何治疗相关不良事件是中性粒细胞计数减少(舒格利单抗组 320 例中的 104 例 [33%] 与安慰剂组 159 例中的 52 例 [33%]),白细胞计数减少(45 [14%]与 27 [17%])、贫血 (43 [13%] vs 18 [11%])、血小板计数减少 (33 [10%] vs 15 [9%]) 和中性粒细胞减少 (12 [4%] vs 7 [4%])。舒格利单抗组 73 名 (23%) 患者和安慰剂组 31 名 (20%) 患者发生了任何与治疗相关的严重不良事件。舒格利单抗组组 10 例 (3%) 患者报告了任何与治疗相关的死亡(1 例肺炎伴呼吸衰竭;1 例骨髓抑制伴感染性休克;2 例肺炎;呼吸衰竭、腹痛、心力衰竭和免疫介导性肺炎各有一名患者;另外两名死亡原因不明)和安慰剂组的2名(1%)患者(肺炎和多器官功能障碍综合征)。
总之,该研究发现无论PD-L1表达如何,与安慰剂加化疗相比,舒格利单抗加化疗显示出具有统计学意义和临床意义的无进展生存期改善,这可能是一种新的一线治疗选择适用于鳞状和非鳞状转移性非小细胞肺癌。
该研究由基石药业资助。该研究是临床试验,具体请谨遵医嘱。
参考消息:
https://www.cell.com/cancer-cell/fulltext/S1535-6108(21)00382-2
https://www.thelancet.com/journals/lanonc/article/PIIS1470-2045(21)00650-1/fulltext#%20


