一文读懂 | 二尖瓣钳夹术的前世今生
时间:2023-08-24 13:42:10 热度:37.1℃ 作者:网络
二尖瓣反流(MR)是常见的心脏瓣膜疾病之一,长期未纠正的MR会影响心功能,引发心力衰竭及其他更差的临床结局。对于老年人或有多种合并症的患者,外科手术修复或置换的风险过高。因此,临床上有近一半的重度MR患者未接受手术治疗。MitraClip是一种用于治疗MR的经导管二尖瓣修复系统,模仿Alfieri缘到缘技术进行二尖瓣修复,于20世纪90年代后期开发。在临床试验证明其安全性和有效性后,获得了临床使用批准,特别是在欧洲、美国和日本用于不耐受外科手术的患者。最新一代 MitraClip 系统可以提高手术成功率,即使在二尖瓣解剖结构复杂的患者中也是如此。通过本文,回顾MitraClip临床试验和RCT的证据,并展望MitraClip的患者选择和未来前景。
二尖瓣反流
二尖瓣反流是常见的瓣膜性心脏病,其患病率随着年龄的增长而迅速增加。据报告,每10例75岁以上患者中就有1人患有中度或重度MR。未经手术治疗的严重退行性MR(DMR)患者的预后较差。同时,伴随着人口结构不断老龄化,越来越多的心力衰竭(HF)患者已成为一个全球性问题。功能性MR(FMR)常继发于心衰患者,其机制涉及左心室(LV)重塑、乳头肌移位和(或)长期持续性心房颤动(AF)造成的左心房(LA)扩张。即使使用了指南指导药物治疗(GDMT),FMR的预后仍较差。FMR与HF症状、生活质量下降以及HF导致的再住院和死亡率增加有关,FMR合并收缩期HF的患者在5年内死亡率为62%。FMR的手术治疗仍然存在争议和挑战。二尖瓣环成形术是FMR的标准手术技术。但它没有直接解决左心室畸形和二尖瓣瓣叶栓系。因此,在无须冠状动脉旁路移植术的FMR患者中并不推荐。有近一半的重度症状性MR,因为合并症较多,行开放手术治疗的风险太高,而没有进行手术治疗。
发展历史和初始临床试验
1996年,意大利心脏外科医生Ottavio Alfieri提出,只需要一条缝合线就可以闭合MV。这种技术于1997年提交了使用导管放置单个U形夹的MitraClip的专利申请。MitraClip设备于2008年获得欧洲市场的CE标志,并于2013年获得美国FDA的批准在美国上市。MitraClip系统是首个经皮二尖瓣修复系统,该技术被称为“二尖瓣经导管边缘到边缘修复 (TEER)”。
2011年,新英格兰杂志发表了2005~2008年在北美开展的具有里程碑意义的EVEREST II随机对照试验。入选患者随机分配到MitraClip或手术组(75例FMR患者,204例DMR患者),评估MitraClip对符合手术条件的MR患者的安全性和有效性。安全性终点包括术后30天的不良事件,疗效终点包括全因死亡率、MR严重程度为3+或更高以及避免12个月时再次进行MV手术。分析表明,MitraClip组的不良事件明显较少,表现出更高的安全性。但MV再次手术在MitraClip组(20%)比在手术组(2%)更频繁。2015年,发表了5年的随访结果。术后6个月时组间差异无统计学意义。与手术组相比,心功能(NYHA分级)和左心室功能在MitraClip组中也有所改善。
2013年发表的欧洲ACCESS-EU两阶段多中心注册研究,评估了2009年至2011年间MitraClip在14个欧洲中心的高风险手术患者(393例FMR,117例DMR)中的临床疗效和安全性。即刻手术成功率(APS)为91.2%,无围手术期死亡,30d死亡率为3.4%,1年生存率为81.8%。在这些患者中,71.4%的患者在12个月时改善为NYHA Ⅰ或Ⅱ,6分钟步行距离和明尼苏达心力衰竭生活质量评分显著改善,证明了MitraClip的安全性和有效性。因此,MitraClip最终被纳入2012年欧洲心脏病学会(ESC)指南,表明经皮边缘到边缘手术可能适用于心脏直视手术高风险且符合资格解剖学标准的MR患者。
两项结果相互矛盾的FMR随机对照试验
2018年公布了两项针对FMR和HF患者的MitraClip随机对照试验,并报告了不同的结果。在这些研究发表之前,没有关于MitraClip在FMR患者中疗效的RCT。因此,他们引起了全世界的关注。
2018年8月,在慕尼黑举行的2018年ESC大会上发表了MITRA-FR多中心研究结论。该试验覆盖法国37个中心,入组时间2013年12月至2017年3月,纳入标准为有症状的重度FMR[有效反流口面积 (EROA) > 0.20 cm2或反流量>30 ml],LVEF为15%~40%且正在接受最佳药物治疗同时不耐受外科手术。患者被随机分配到MitraClip治疗组(n=152)或药物治疗组(n=152)。分析显示,设备植入的成功率为96%,无急诊手术病例,无围手术期死亡,但两组间在1年全因死亡率或HF相关住院治疗的主要终点方面无显著差异(MitraClip组为54.6%,药物治疗组为51.3%;HR 1.16;95%CI 0.73~1.84)。全因死亡率分别为24.3%和22.4%,HF相关住院率分别为48.7%和47.4%。该研究证明了MitraClip的安全性,但不能证明其预后疗效。此外,2019年9月在巴黎举行的2019年ESC大会上公布了2年随访数据,全因死亡率和HF相关住院率仍然无显著差异(HR 1.04;95%CI 0.76~1.42),MitraClip组为64.2%,药物治疗组为68.6%。
另一项RCT,即COAPT试验,在圣地亚哥举办的TCT2018上公布。纳入2012年12月至2017年6月,北美78个中心共614例接受了最大量的GDMT后仍有症状的3+或4+FMR患者,随机分配接受MitraClip + GDMT(302例患者)或单独接受GDMT(312例患者),以研究MitraClip的安全性和有效性。患者平均年龄约为72.2岁,平均STS评分为8.2%,平均LVEF为31.3%。分析显示,MitraClip + GDMT组在24个月内HF相关住院的主要终点显著降低(MitraClip + GDMT组35.8%/人年,单独GDMT组67.9%/人年;HR 0.53;95% CI 0.40~0.70)。12个月内无MitraClip相关并发症的比例为96.6%,表明MitraClip的安全性。MitraClip + GDMT组在30天、6、12和24个月时NYHA分级和MR等级明显更好,而单独使用GDMT组24个月时的NYHA Ⅰ/ Ⅱ HF相关住院率显著更高。此外,2019年9月在旧金山举行的TCT 2019上公布了3年随访数据。MitraClip + GDMT组36个月内HF相关住院率的主要终点为35.5%/人年,单独GDMT组为68.8%/人年(HR 0.49;95%CI 0.24~0.40),进一步扩大了组间差异。
COAPT和MITRA-FR试验几乎同时发表在著名的《新英格兰医学杂志》上,显示出截然不同的结果,震惊了全世界的临床医生并引起了很大的争议。造成这种情况的主要原因是COAPT试验的MR严重程度较高(平均EROA,0.41 cm2 vs 0.31 cm2),COAPT试验的继发性左心室重塑不如MITRA-FR试验[左心室收缩末期容积(LVEDV)指数,101 ml/m2 vs 135 ml/m2]。此外,COAPT试验受试者严格使用GDMT进行管理,而MITRAFR试验参与者可以根据他们在临床环境中的情况调整他们的药物。最后,与MITRA-FR试验受试者相比,COAPT试验受试者在随访期间的手术并发症更少,APS率更高,MR降低幅度更大。
关于MR严重程度和左室重塑的进展,最近提出了“严重和不成比例的MR”“严重和成比例的MR”和“轻至中度MR”的概念。图1清晰地表示了左心室重塑的进展与MR程度。因此,在视觉上可以理解的是,MITRA-FR试验受试者具有严重且成比例的MR,而COAPT试验受试者具有严重且不成比例的MR。因此,在图表上绘制这两个指数之间的关系可用于确定患者是否患有 MitraClip有效的FMR。
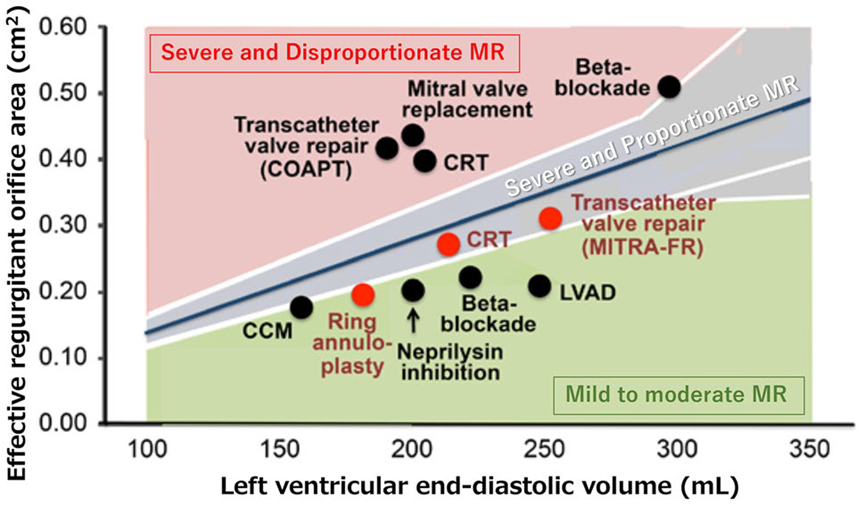
图1 成比例和不成比例MR的疗效比较。图中粉色区域表示严重和不成比例的MR,灰色区域表示严重和成比例的MR,绿色区域代表轻度至中度的MR。纵轴为EROA,横轴为LVEDV。每个点表示一种药物或干预措施对成比例和不成比例MR的影响。黑点表示降低了死亡或心衰住院风险的治疗方法,红点代表无效的治疗方法。
当前指南中关于 MitraClip用于FMR 的建议
基于对MITRA-FR和COAPT试验之间差异的讨论,2020 年美国心脏病学会 (ACC)/美国心脏协会(AHA)瓣膜性心脏病(VHD)指南建议对以下患者使用MitraClip:接受 GDMT 治疗心衰(D期)后仍有持续症状(NYHA Ⅱ~Ⅳ)的、与LVEF降低(20%~50%)相关的严重FMR患者,需要同时具备适合 MitraClip 的解剖结构、左心室收缩末期直径(ESD)≤70 mm和肺动脉收缩压≤70 mmHg 。这类患者使用MitraClip被视为Ⅱa类推荐。
2021年,欧洲心胸外科协会(EACTS)VHD指南建议,对于伴有冠状动脉或其他需要治疗的心脏病的有症状FMR患者,或被心脏团队判断为不适合进行心脏直视手术的患者,或接受经皮冠状动脉介入治疗(PCI)和(或)经导管主动脉瓣植入(TAVI)等有创心导管治疗的患者,将MitraClip视为Ⅱa类推荐。同时,对于未合并其他需要侵入性治疗的心脏病的FMR患者,如果满足COAPT标准:中重度或重度FMR(MR≥3+),优化GDMT治疗后仍有症状、LVEF为20%~50%,LVESD ≤ 70 mm,前一年内至少一次因心衰住院、脑利钠肽水平升高或解剖结构判断适合MitraClip治疗,MitraClip植入应被视为Ⅱa类推荐。
当前指南中对MitraClip用于DMR的建议以及适合使用MitraClip的形态
在2020年ACC/AHA指南中,针对有症状的严重DMR合并高手术风险的患者(NYHA Ⅲ级或Ⅳ级),如果MV解剖结构有利于MitraClip修复并且患者的预期寿命至少为1年,则MitraClip被视为Ⅱa类推荐。在2021年ESC/EACTS指南中,对于符合超声心动图标准且无法手术或被心脏团队判定为高手术风险的有症状患者,MitraClip 治疗被认为是Ⅱb类推荐。
根据这些指南,通过超声心动图评估的MV的解剖学特征是MitraClip成功的关键。术前 TEE可以通过评估其特征,例如基线MR严重程度、MV面积和传导压力梯度,并排除心内血栓来确定 MitraClip 植入的适用性。术中和 MitraClip 植入后应重复超声心动图评估,以评估操作成功与否。在使用MitraClip的早期,MitraClip植入通常仅限于符合EVEREST试验中使用的解剖学合格标准(称为EVEREST标准)的患者。然而,随着超声心动图成像技术的进步、手术专业知识和设备的进步使得这些解剖学标准的扩展成为可能。
国内实践
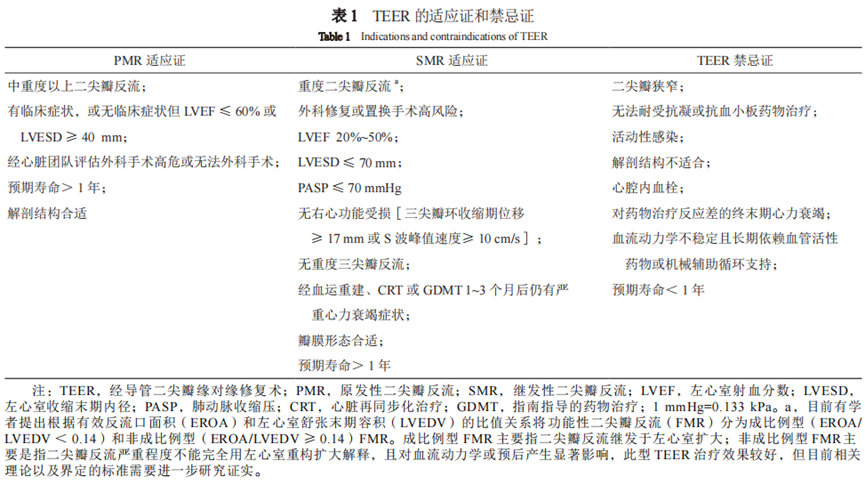
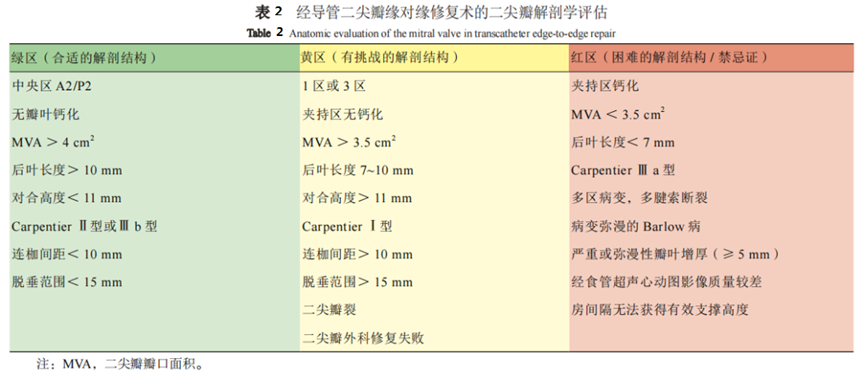
2023年1月在北京瓣膜论坛会议上,2022中国经导管二尖瓣缘对缘修复(TEER)临床路径正式发布。这对我国TEER临床操作的规范化管理具有非常重要的指导意义。更新了TEER的适应证及禁忌证,详见表1。临床路径中也重申了“绿区-黄区-红区”概念,绿区病变即为符合EVEREST Ⅱ和COAPT研究入选标准的简单病变;黄区病变为超越指南推荐标准的复杂病变;红区病变则为困难的解剖结构或禁忌证,需要评估二尖瓣置换指征(表2)。临床路径也指导了TEER团队的构成以及手术的流程。随着该项技术在国内的逐步推进,期待国际交流中有更多的中国声音。
MitraClip用于心房FMR
心房FMR是近年来提出的一种FMR的新分型,与长期持续性心房颤动、二尖瓣环和左房扩张伴左心室射血性保留有关。它还具有其他几种病因和病理生理因素,如二尖瓣环收缩力降低、二尖瓣环鞍形变形、二尖瓣环扩张修复不足、瓣叶重塑不足、二尖瓣后部收缩力减弱等,导致瓣叶覆盖力降低,这些奇特的机制仍有待进一步研究。
MitraClip用于心房FMR的研究很少,缺乏明确的指南建议。由于心房FMR的病理生理学特征是射血分数保留,患者可能不符合COAPT 标准,提示对 MitraClip 产生良好反应的可能性增加。因此,如果心脏团队考虑使用 MitraClip,根据2021年ESC/EACTS指南,这将是IIb类推荐。Tanaka等报道了来自德国的单中心数据,MitraClip疗法在心房FMR患者中取得了很高的技术成功率(94.1%)和MR降低≤1+(79.7%)。西班牙登记处报告称,在6个月和12个月的随访中,心房FMR患者与心室FMR或DMR/混合MR患者在MR降低、全因死亡率、HF住院率以及NYHA分级改善方面没有显著差异。不过,伴随的三尖瓣反流(TR)率在该人群中没有显著变化。Doldi等报道了TEER欧洲登记处对FMR的分析结果,结果显示,在欧洲临床实践中接受MitraClip植入的有症状FMR患者中,约有8%的心房FMR,MitraClip治疗有效且与MR降低和NYHA等级改善有关。此外,右心室功能不全和晚期心衰对心房FMR患者有显著的预后影响。
尽管LVEF保留,但仍有相当比例的长期AF患者观察到显著的心房FMR和心房功能性TR。在COAPT试验亚组分析中,同时患有中度或更严重TR的重度FMR患者,有更差的临床和超声心动图特征,以及较差的临床结局,而MitraClip的使用似乎具有与TR相关的不良结局。美国 MitraClip手术的 上市后1年监测结果数据也表明,重度TR 以及年龄增长、基线LVEF降低、术后MR恶化、中度或重度肺部疾病、透析与MitraClip 植入后因HF导致的死亡率或再住院相关。需要进一步的证据来评估MitraClip在心房FMR并发TR和右心室功能障碍患者中的长期结局。
超声心动图和超声心动图专家的重要性
一些进行过PCI和TAVI的心内科医生可能认为TEER成功的关键是MitraClip设备和导管操作者技术的进步。但是,TEER与这些手术完全不同。如前所述,必须使用超声心动图而不是透视来评估MR。超声心动图是根据 EVEREST标准在TEER手术前选择患者的重要工具,以评估MR严重程度、MR病因、左心室和右心室功能以及二尖瓣解剖结构。在TEER手术过程中,高质量的TEE图像对于手术成功至关重要。经房间隔穿刺的位置,应该在卵圆窝内,并在二尖瓣环上足够高的位置。然后将可操控的导管和夹子输送系统插入LA同时避免损伤LA壁,后者位于MV的目标病变上。然后,夹子抓住前后MV瓣叶,并在闭合时持续监测MR降低和MV压力梯度。最后,评估夹子植入术后残余MR严重程度。此外,在系统移除后评估医源性房间隔缺损。超声心动图技术的发展和心脏团队成员之间的良好沟通无疑有助于比早期试验更好的TEER手术结局。
MitraClip的未来展望
在不久的将来,两项大规模的RCT将为MitraClip提供额外的证据支持。其中之一是 RESHAPE-HF2研究,对MitraClip系统的安全性和有效性的临床评估试验,该试验根据症状招募了具有临床显著功能的中重度或重度MR和不同LVEF阈值的患者(NYHAⅡ级:LVEF 15%~35%;NYHA Ⅲ/Ⅳ级:LVEF 15%~45%),并根据6分钟步行距离(步行>距离475米或无法进行步行)排除患者。本研究提供了有关MitraClip 在NYHAⅢ级或Ⅳ级HF伴有严重FMR患者中的安全性和有效性的信息。另一项RCT是MATTERHORN试验,是一项多中心、随机、对照研究,该研究比较了在高手术风险、LVEF≥20%和临床上具有中度至重度FMR的患者,行MitraClip植入术与手术治疗的安全性和有效性。TEER的代替方法,有植入在冠状窦中的Carillon二尖瓣轮廓系统,经导管瓣环成形术(Cardioband)。此外,目前正在试验(APOLLO试验)的Intrepid经导管二尖瓣置换系统,以及NeoChord人工腱索植入系统,可以弥补MitraClip相关的解剖学禁忌证病例。国内自主研发的TEER器械正在进行上市前临床研究,主要包括:ValveClamp、DargonFly-M、NovoClasp、Valveclasp、SQ-Krine、ValveClip、Neonova、Kokaclip等。
总结
MitraClip是中重度或重度MR患者的一种新的经导管治疗选择,西方国家的临床试验已经证明了其安全性和有效性。值得注意的是,对于因左心室收缩功能障碍而出现症状性FMR 和HF的患者,应将 MitraClip 视为Ⅱa 类推荐。然而,由于并发TR,心房FMR患者的远期结局尚不清楚。超声心动图专家和心脏介入团队成员之间需要良好沟通,旨在更轻松、更安全的实施MitraClip治疗,从而提高手术成功率。



