Blood:口服伊沙佐米-来那度胺-地塞米松治疗不能移植的新确诊多发性骨髓瘤
时间:2021-07-05 10:02:23 热度:37.1℃ 作者:网络
基于来那度胺-地塞米松 (Rd) 的连续方案是不符合移植条件的新确诊的多发性骨髓瘤 (NDMM) 患者的标准治疗之一。口服蛋白酶体抑制剂伊沙佐米适用于连续给药,具有可预测、可控的毒性。
TOURMALINE-MM2试验是一项双盲、安慰剂为对照的临床试验,招募了不符合移植条件的NDMM患者,随机分成了两组,接受伊沙佐米 4mg(n=351)或安慰剂(n=354)联合Rd。18个疗程后,停用地塞米松,继续采用减剂量伊沙佐米(3 mg)和来那度胺(10 mg)治疗,直到病情进展或不可耐受的毒性。主要终点是无进展生存期(PFS)。
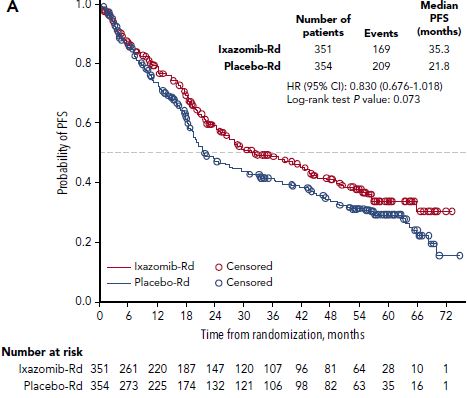
伊沙佐米-Rd组和安慰剂-Rd组的PFS率
伊沙佐米-Rd组和安慰剂-Rd组的中位随访时间分别是53.3个月和55.8个月,中位PFS分别是35.3 vs 21.8个月(风险比[HR] 0.830, 95%CI 0.676-1.019;p=0.073)。与安慰剂-Rd组相比,伊沙佐米-Rd组的完全缓解率(26% vs 14%;优势比[OR] 2.10;p<0.001)和≥非常好的部分缓解率(63% vs 48%;OR 1.87;p<0.001)均更高。
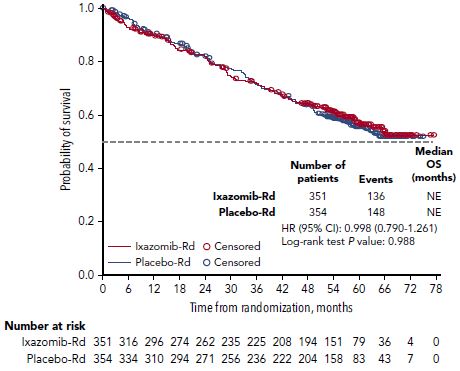
伊沙佐米-Rd组和安慰剂-Rd组的OS率
在预先指定的高风险细胞遗传学亚组中,伊沙佐米-Rd组和安慰剂-Rd组的中位PFS分别为23.8个月和18.0个月(HR 0.690;p=0.019)。
需紧急治疗的不良事件(TEAE)多是1/2级的。伊沙佐米-Rd组和安慰剂-Rd组分别有88% vs 81%的患者经历了≥3级TEAE,66% vs 62%的患者经历了严重TEAE,而且分别有35% vs 27%的TEAE病例导致了治疗中断;两组分别有8% vs 6%的患者在研究期间死亡。
综上所述,将伊沙佐米添加到Rd方案中是可以耐受的,没有导致新的安全信号,并导致13.5个月的具有临床意义的PFS获益。 总而言之,伊沙佐米-Rd为可以从全口服三联疗法中获益的患者提供了新选择。
原始出处:
Thierry Facon, et al. Oral ixazomib, lenalidomide, and dexamethasone for transplant-ineligible patients with newly diagnosed multiple myeloma. Blood (2021) 137 (26): 3616–3628. https://doi.org/10.1182/blood.2020008787