ESMO 2021:特瑞普利单抗一线治疗食管癌的Ⅲ期临床研究结果公布,OS高达17个月
时间:2021-09-21 16:02:58 热度:37.1℃ 作者:网络
2021年9月16日至21日,2021年欧洲肿瘤内科学会(ESMO)年会采用线上会议的方式举行。作为全球最具影响力的肿瘤学术平台之一,ESMO年会每年都会汇聚全球肿瘤专业人士,共同分享肿瘤领域的前沿研发趋势和进展。
在本次ESMO年会上,君实生物特瑞普利单抗共有11项最新研究集中亮相,覆盖消化道肿瘤、肺癌、妇科肿瘤、尿路上皮癌、头颈部肿瘤等多个瘤种,以口头报告、壁报等形式发表。其中,特瑞普利单抗联合化疗一线治疗晚期或转移性食管鳞癌(ESCC)的三期临床试验(JUPITER-06研究)首次公布结果,显著改善了患者的生存获益,有望成为该领域新的标准治疗方案。
食管癌是消化道领域最常见的恶性肿瘤之一。据统计,2020年中国的食管癌新发病例数高达32万,约占全球的50%,而死亡病例数也高达30万,约占全球的56%,发病率和死亡率分别位居所有恶性肿瘤中第五和第四位。食管鳞癌和腺癌是食管癌的两种主要组织学亚型,其中中国患者以食管鳞癌(ESCC)为主要亚型,约占总体病例数的90%以上。
中山大学肿瘤防治中心王峰教授在本次ESMO学术年会上以口头汇报(编号:1373MO)形式报告了一项随机、双盲、安慰剂对照、多中心的Ⅲ期研究(JUPITER-06研究,NCT03829969),由中山大学肿瘤防治中心徐瑞华教授担任主要研究者,旨在比较特瑞普利单抗联合紫杉醇/顺铂(TP化疗)与安慰剂联合TP化疗在晚期或转移性ESCC一线治疗中的有效性和安全性。

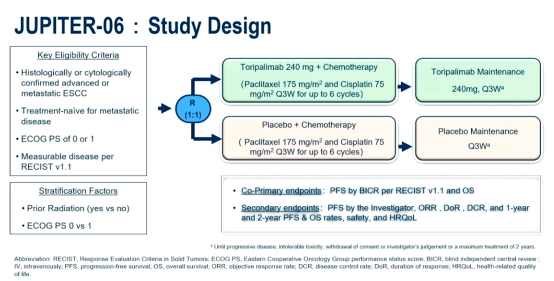
JUPITER-06研究共纳入514例未接受过治疗的晚期或转移性ESCC患者,随机分配至特瑞普利单抗联合化疗组(n=257)或安慰剂联合化疗组(n=257),分别接受特瑞普利单抗(240mg)或安慰剂联合TP化疗方案(Q3W)治疗最多6个周期,随后接受特瑞普利单抗或安慰剂维持治疗。JUPITER-06研究的主要终点是由BICR(盲态独立中心阅片)根据RECIST v1.1进行评估的无进展生存期(PFS)和总生存期(OS),次要终点为研究者评估的PFS、客观缓解率(ORR)和缓解持续时间(DoR)等。
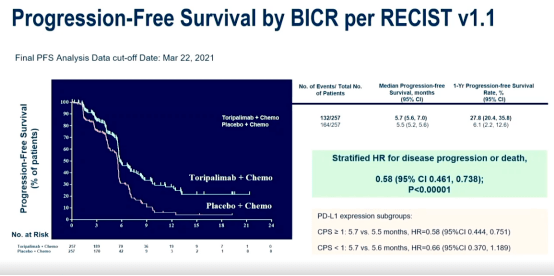
截至2021年3月22日,经BICR评估,特瑞普利单抗组和安慰剂组的中位PFS分别为5.7个月和5.5个月。特瑞普利单抗组的疾病进展或死亡风险降低了42%(HR=0.58 [95% CI:0.461-0.738],P<0.00001),27.8%的患者在1年内未发生疾病进展,获益比例是安慰剂组的4倍以上,后者仅为6.1%。
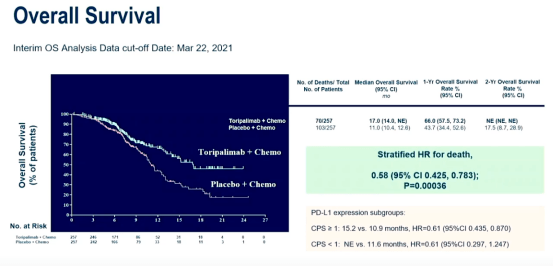
同时,与单纯化疗相比,特瑞普利单抗联合化疗将患者的生存期显著延长,中位OS为17.0个月 vs. 11.0个月,延长时间长达6个月。特瑞普利单抗组的患者死亡风险降低了42%(HR=0.58 [95% CI:0.425-0.783],P=0.00036)。特瑞普利单抗组和安慰剂组的1年OS率分别为66.0%和43.7%。此外,在各关键亚组中均观察到了特瑞普利单抗联合化疗的PFS和OS获益,包括PD-L1表达亚组。在安全性方面,在化疗基础上加入特瑞普利单抗进行治疗,未发现新的安全性信号。
研究结果显示,在标准一线TP化疗方案中加入特瑞普利单抗,可使晚期或转移性ESCC患者获得更优的PFS和OS,显著降低患者的疾病进展或死亡风险,显著改善生存获益,且无论PD-L1表达如何均可获益。这些结果有望支持特瑞普利单抗联合化疗成为晚期或转移性ESCC新的一线标准治疗。
王峰教授表示:“食管癌是消化道常见的恶性肿瘤。晚期食管癌虽然有含铂的双药化疗作为一线标准方案,但患者预后仍不乐观,5年生存率不足20%。JUPITER-06研究的结果令人振奋,相较单独化疗,特瑞普利单抗联合化疗一线治疗晚期或转移性食管癌不仅显著降低了患者的进展或死亡风险,还将中位生存期延长了6个月,这是目前已知的三期试验中总生存期最长的,且安全性和耐受性良好。我们期待JUPITER-06研究后续总生存期数据的公布,有望进一步加速免疫联合化疗方案成为晚期或转移性食管癌的一线标准,为中国乃至全球的食管癌患者带来获益!”
君实生物首席医学官Patricia Keegan博士表示: “中国是全球食管癌发病率和死亡率最高的国家之一,作为立足中国、布局全球的创新药企,君实生物持续关注本土高发,且对免疫治疗有较好响应、临床急需治疗的瘤种。随着针对黑色素瘤、鼻咽癌、尿路上皮癌、肺癌和食管癌的关键注册临床研究数据的陆续公布,特瑞普利单抗在多种肿瘤治疗中保持了一贯强大的疗效与安全性特点。我们将继续推进特瑞普利单抗在食管癌领域的新适应症上市申请工作,尽快为中国和海外患者带来新的治疗选择”。
君实生物与合作伙伴Coherus计划于2022年向FDA提交特瑞普利单抗联合含铂化疗一线治疗晚期或转移性ESCC适应症的生物制品许可申请(BLA)。2021年7月,国家药品监督管理局(NMPA)已受理该适应症在中国的上市申请。
原始出处:
Rui-Hua Xu, et al. JUPITER-06: A randomized, double-blind, phase III study of toripalimab versus placebo in combination with first-line chemotherapy for treatment naive advanced or metastatic esophageal squamous cell carcinoma (ESCC). ESMO 2021, Sep 16-22. Abstract 1373MO.


