NBT:Angela Wahl/姚文博构建首个无菌人源化小鼠模型揭示常驻菌群对EBV和HIV感染的作用
时间:2023-08-20 23:37:34 热度:37.1℃ 作者:网络
人体肠道微生物基因组作为人类的第二套基因组,与人类健康密切相关。大量的研究表明肠道微生物与包括心血管、肿瘤、神经、消化等多种疾病的发生发展密切相关,阐明其因果关系一直是该领域的主要目标之一。
2023年8月10日,北卡罗来纳大学教堂山分校的Angela Wahl,姚文博及 J Victor Garcia合作在Nature Biotechnology 在线发表题为“A germ-free humanized mouse model shows the contribution of resident microbiota to human-specific pathogen infection“的研究论文,该研究成功开发了无菌免疫人源化小鼠模型,为直接研究肠道微生物在人类特异性病原体感染的易感性和致病机制提供了可能。
利用这种模型,该研究成功评估常驻菌群在人类特异性病毒EBV和HIV的感染建立、复制和致病过程中的作用。研究发现肠道微生物的存在促进了EBV感染和EBV诱导的肿瘤发生的建立,并且增加了HIV的感染率和复制活跃水平。与无菌小鼠相比,有肠道菌群的小鼠感染后的血浆和组织中HIV- RNA水平更高。分析肠道组织发现,HIV的靶细胞CCR5+ CD4+ T细胞在有肠道菌群小鼠中更高,表明肠道微生物群是通过调控HIV靶细胞的水平来促进了HIV的感染和致病过程。

研究者利用骨髓-肝-胸腺(BLT)平台创造了拥有人类免疫系统的小鼠,并将它们分别饲养在具有肠道微生物群(SPF,CV小鼠)或没有微生物群(无菌,GF小鼠)的环境中。将这些小鼠暴露于HIV或EBV,并监测病毒的感染率、复制水平以及致病过程。
研究结果表明肠道微生物群的存在促进了HIV和EBV感染率和致病过程。研究者发现有肠道菌的CV小鼠在直肠感染后显示出了HIV的感染率增加(提高了200%);相比于无菌小鼠,CV小鼠在经口暴露后HIV的感染率增加了300%,并且HIV复制水平显著增加。其中肠道内病毒复制水平增加最显著,HIV-RNA水平在肠道微生物群的存在下提高了近1,500倍,在外周血浆以及其他非肠道组织,如骨髓、肝脏和肺部,也观察到了HIV-RNA水平的升高。此外,与GF小鼠相比,CV小鼠在EBV感染后也出现了更高的感染率以及致瘤性。这些结果表明,肠道微生物群在两种人类特异性病原体,HIV和EBV的感染建立中发挥着中心作用,并且促进了其致病性。
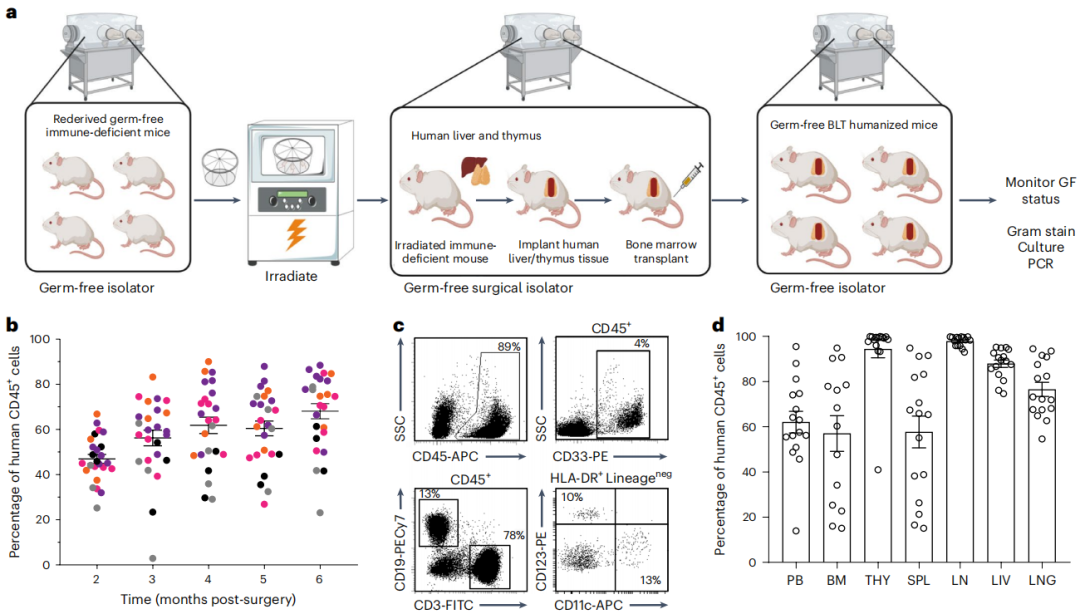
用人造血细胞对GF-BLT小鼠进行重建(图源自Nature Biotechnology )
总之,该模型为直接研究肠道微生物在多种感染性疾病(尤其是人类特异性病原体)以及非传染性疾病的发生与发展中所扮演的作用和相关机制提供了实验可能,也为进一步通过定植和操纵特定肠道微生物以对抗疾病,保护人体健康奠定了平台基础。
参考消息:
https://www.nature.com/articles/s41587-023-01906-5


