NEJM | 单药Divarasib(GDC-6036)治疗KRAS G12C突变实体瘤
时间:2023-08-27 11:44:27 热度:37.1℃ 作者:网络
KRAS基因突变是人类癌症中最常见的致癌驱动突变。KRAS蛋白第12位(G12C)的甘氨酸突变为半胱氨酸会干扰三磷酸鸟苷(GTP)的水解,从而使KRAS主要处于活性的GTP结合状态。KRAS G12C蛋白活性的增加通过直接促进肿瘤细胞存活,增殖和转移的多个下游途径驱动致癌信号传导。KRAS G12C突变存在于约12%至14%的非小细胞肺癌(NSCLC)患者,4%的结直肠癌患者和高达4%的其他实体瘤类型(不包括NSCLC和结直肠癌)患者中,频率因种族和性别而异。KRAS G12C突变型实体瘤的标准治疗方法各不相同,但通常包括非选择性化疗,免疫治疗或两者兼有,治疗对先前接受治疗的患者产生了适度的益处。尽管最近开发的KRAS G12C抑制剂(包括索托拉西布和阿达格拉西布)已在先前治疗过的KRAS G12C突变癌症患者中显示出抗肿瘤活性,但临床获益的程度仍然有限,更好的靶向KRAS G12C的治疗仍然是重中之重。
Divarasib(GDC-6036)是一种共价KRAS G12C抑制剂,旨在表现出高效力和选择性。它与半胱氨酸残基结合,不可逆地将蛋白质锁定在无活性状态,从而关闭其致癌信号传导。divarasib在体外的效力是索托拉西布和阿达格拉西布的5至20倍,选择性高达50倍。这项正在进行的1期研究正在评估divarasib作为单一药物,并与其他抗癌疗法联合用于患有KRAS G12C突变的晚期或转移性实体瘤患者。

方法:在一项1期研究中,该研究评估了患有KRAS G12C突变的晚期或转移性实体瘤患者每天口服一次(剂量范围为50至400 mg)的Divarasib。主要终点是评估安全性;药代动力学,研究者评估了抗肿瘤活性,并评估了反应和耐药性的生物标志物。
结果:共有137名患者(60名非小细胞肺癌(NSCLC),55名结直肠癌和22名其他实体瘤)接受了divarasib治疗。没有报道剂量限制性毒性作用或治疗相关死亡。127例患者(93%)发生治疗相关不良事件;15名患者(11%)发生3级事件,1名患者(1%)发生4级事件。治疗相关不良事件导致19名患者(14%)剂量减少,4名患者(3%)停止治疗。在NSCLC患者中,53.4%的患者(95%置信区间[CI],39.9至66.7)观察到确诊反应,中位无进展生存期为13.1个月(95%可信区间,8.8至无法估计)。在结直肠癌患者中,29.1%的患者(95%CI,17.6至42.9)观察到确诊反应,中位无进展生存期为5.6个月(95%CI,4.1至8.2)。在其他实体瘤患者中也观察到反应。循环肿瘤DNA的系列评估显示,与反应相关的KRAS G12C变异等位基因频率下降,并确定了可能赋予对divarasib抗性的基因组改变。


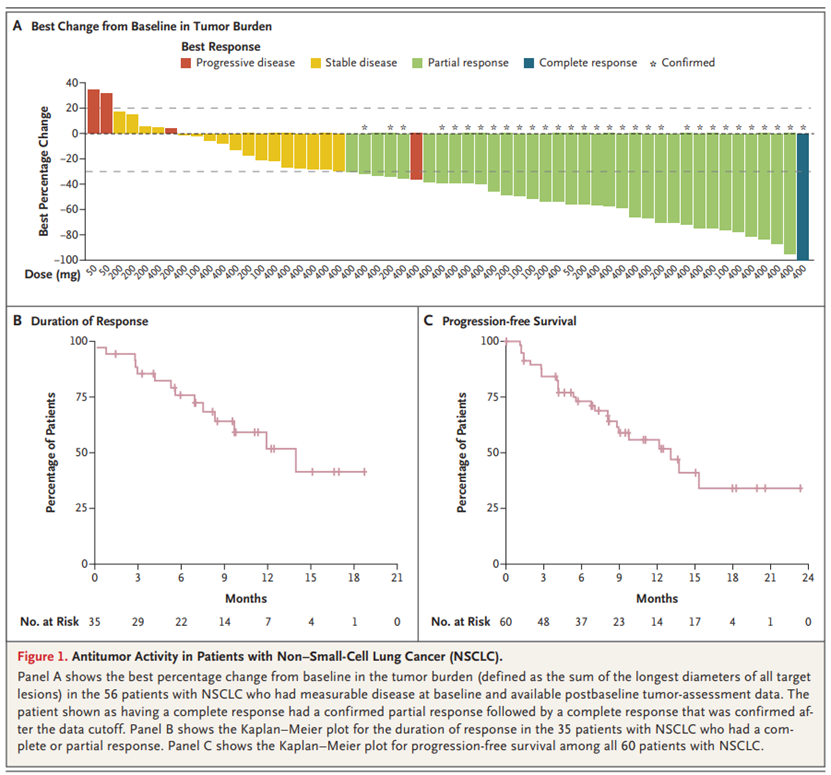
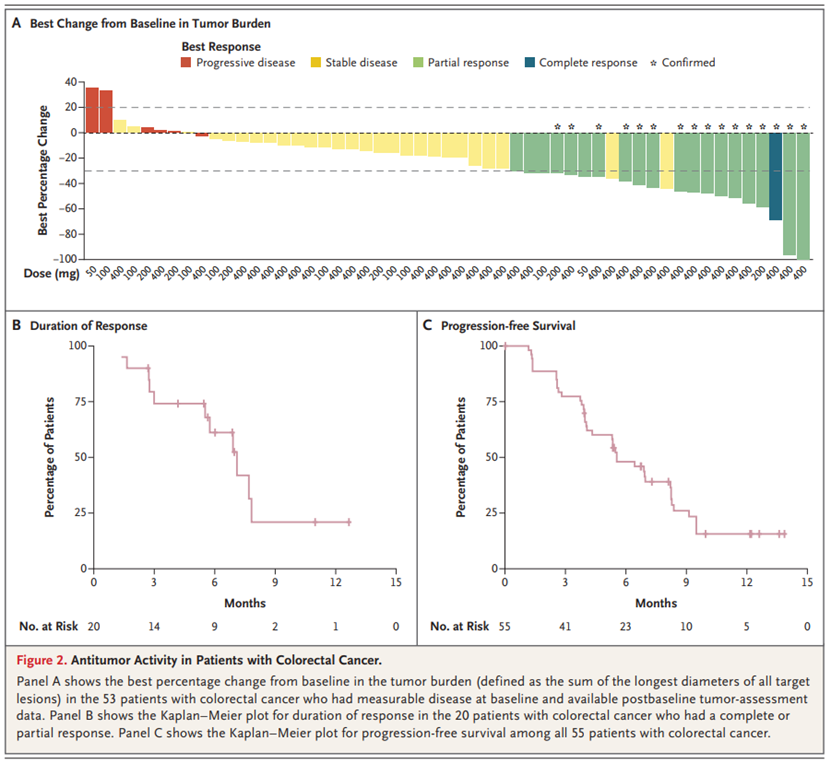
结论:单药divarasib被证明在先前治疗过的NSCLC,结直肠癌或其他癌症患者中具有可控的安全性和非常有希望的抗肿瘤活性,在这项研究中KRAS G12C阳性肿瘤中产生持久的临床反应,主要发生的是低级别不良事件。
原始出处:
Sacher A, et al. 2023. Single-Agent Divarasib (GDC-6036) in Solid Tumors with a KRAS G12C Mutation. New England Journal of Medicine 389:710-721. DOI: 10.1056/nejmoa2303810.


