感冒未痊愈健身,引发心梗去世!
时间:2023-09-05 18:59:39 热度:37.1℃ 作者:网络
媒体从李林多位友人处获悉,重庆广播电视台知名主持人李林9月2日晚因病去世,得年42岁。9月3日,中播网官方微博也发文悼念:重庆之声新闻主播李林,因感冒尚未痊愈,9月2日晚锻炼身体时,突发心肌梗塞,离开了我们。

急性心肌梗死(Acute Myocardial Infarction,AMI)是指各种原因造成冠状动脉血供急剧减少或完全中断,使相应心肌严重而持久的急性缺血而致心肌细胞的坏死。
急性心肌梗死是心原性休克(CS)最常见的原因,全球注册研究显示急性心肌梗死合并心原性休克(AMICS)总体发生率为4%~12%,30 d死亡率高达40%~45%,急性心肌梗死合并心原性休克(AMICS)主要表现为反复或进行性药物难以控制的缺血性症状,同时伴随血流动力学不稳定、危及生命的心律失常、心脏骤停、机械性并发症和急性心力衰竭。
危险因素
AMI发生CS的危险因素包括:
(1)年龄>70岁(2分)、
(2)既往卒中/TIA(2分)、
(3)既往心脏骤停(3分)、
(4)前壁MI(1分)、
(5)首次医疗接触到急诊PCI延迟>90 min(2分)、
(6)住院时killip II级(2分)、
(7)killip III级(6分)、
(8)心率>90次/min(3分)、
(9)SBP<125 mmHg且PP<45 mmHg(4分)、
(10)血糖浓度>10 mmol/L(3分)、
(11)罪犯病变位于左主干(5分)、
(12)PCI术后TIMI血流<3级(5分)。
根据上述分数累计,0-7分为低危,CS发病率1.3%;8-10分为低到中危,CS发病率6.6%;11-12分为中到高危,CS发病率11.7%;≥13分为高危,CS发病率31.8%。
AMICS的诊断和评估
AMICS早期诊断依据包括心电图(ECG)、心肌损伤标志物、影像学表现、心源性休克(CS)指标检测、AMICS临床症状和体征。
1、心电图
所有患者均应在首次医疗接触后10 min内记录12或18导联ECG,高度怀疑下后壁及右心室心肌梗死者应记录18导联ECG。对有持续性缺血症状但首份ECG不能明确诊断的患者,需在15~30 min内复查ECG。

2、心肌损伤标志物
优先选择肌钙蛋白作为AMI常规心肌损伤标志物的检测指标,宜动态观察心肌损伤标志物演变,对疑似患者,推荐发病1 h内行首次高敏肌钙蛋白检测,观察0-1 h内结果变化,根据基线水平及1 h内绝对变化进行诊断(0 h/1 h方案),并将0 h/2 h方案作为替代选择。
3、影像学表现
临床常见的影像学检查为超声心动图和多排CTA,前者可了解心脏结构和功能,有助于高危急性胸痛和AMICS的危险分层,后者有助于鉴别胸痛三联征,即肺栓塞、主动脉夹层和急性MI。
4、AMICS的评估

5、CS指标监测
根据外周血压、组织灌注、心脏指数(CI)、全身血管阻力(SVR)、肺毛细血管楔压(PCWP)等血流动力学表现差异,CS可分为湿冷性休克(三低两高)、干冷型休克、湿暖型休克、干暖型休克(非CS)、血压正常型休克、右心室休克(两低一高)。

6、心脏骤停不良预后相关因素
院外心脏骤停患者的不良预后包括:
①无脉性电活动;
②非可电击复律心律;
③无院外目击者心肺复苏;
④>30 min的心肺复苏;
⑤pH<7.2;
⑥血乳酸>6.5 mmol/L;
⑦年龄>85岁;
⑧终末期肾病;
⑨非心脏原因的心脏停搏。
AMICS治疗
AMICS治疗应遵循病因治疗、稳定血流动力学(血运重建、辅助循环装置)、保护重要脏器功能、维持内环境稳定、防治心律失常、改善心肌代谢、综合支持治疗7大原则。
AMICS休克A和B期,通常应直接进行紧急冠状动脉造影和IRA血运重建。
休克C~E期,应首先关注血压、脏器灌注、氧合及酸碱平衡状况,但同时应尽可能地减少前期治疗导致的再灌注时间延误。
休克E期,应充分评估姑息治疗和早期侵入性治疗的获益-风险比。
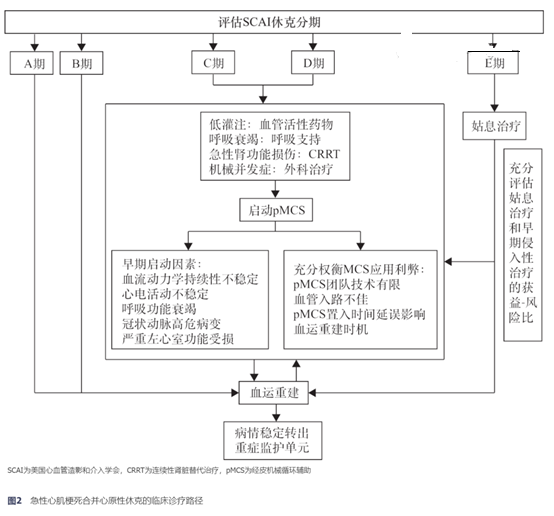
1、血运重建
早期血运重建对AMICS的预后至关重要。SHOCK研究表明,早期血运重建患者的6年存活率明显高于药物保守治疗患者。
急诊经皮冠状动脉介入治疗(PCI)是AMICS血运重建的主要方式。
以下情况适合CABG治疗:
①冠状动脉解剖结构复杂且远端血管适合CABG者;
②因急诊PCI失败导致死亡风险增高者;
③AMICS合并机械并发症需实施紧急外科修补手术者。
当非IRA存在复杂多支病变(如左主干病变、慢性完全闭塞病变、严重钙化或扭曲病变、弥漫性病变等)时,可考虑IRA急诊PCI联合择期CABG治疗以达到完全性血运重建。
部分AMICS合并严重机械并发症或难以纠正的心力衰竭时,需要启动外科干预。
2、多支血管病变的处理策略
AMICS患者行急诊PCI血运重建时,不推荐常规同期处理非IRA。仅在特定情况下可考虑同期或出院前处理非IRA,如:非IRA供血范围大且存在90%以上狭窄;非IRA存在不稳定病变(如斑块破裂、夹层、血栓等);IRA开通后仍存在可能与非IRA相关的缺血症状或血流动力学不稳定等。
3、延迟支架置入策略
对于血栓负荷重、病变不适宜支架置入或支架置入困难的患者,可考虑延迟支架置入。建议根据术者经验、患者基本情况、冠状动脉病变解剖特点、血栓负荷、无复流或慢血流发生风险、再灌注损伤等,综合评估确定最终支架置入策略。
4、心脏骤停患者处理策略
不合并院外心脏骤停不良预后因素时,AMI心脏骤停患者成功复苏,自主循环和神经功能恢复后(格拉斯哥昏迷量表评分≥8分),应尽快将其转移至心脏导管室,以进行冠状动脉血流的全面评估;如果复苏后持续昏迷(拉斯哥昏迷量表评分<8分)或未能执行简单指令,应尽快予以目标温度(32~36 ℃)管理。
有适应证且有条件时鼓励结合E-CPR技术(即ECMO支持下的心肺复苏技术),积极联合开展早期血运重建,但E-CPR技术还需要进一步研究,以明确其实施可行性、组织转运、ECMO优化管理等。
5、经皮机械循环辅助装置治疗
经皮机械循环辅助(pMCS)是治疗AMICS的重要技术之一,其主要作用是降低AMICS心室负荷,增加全身灌注和心肌灌注,提供强有力的血流动力学支持。
现行pMCS共识推荐对于血流动力学不能迅速稳定的AMICS患者应尽早启动pMCS治疗,但pMCS的种类选择、使用时机、预后获益均需要根据SCAI休克分级进行个体化的治疗。
(1)pMCS的种类选择
临床上主要依据AMICS病理生理学特征选择合适的pMCS:
①左心室衰竭为主的AMICS患者:
可选择IABP、左心室-主动脉辅助装置Impella 系统。
伴随难治性呼吸衰竭者建议优先选用ECMO。但VA-ECMO需严密监测左心室负荷指标,如出现左心室扩张、左心房压力升高、肺水肿、主动脉瓣开放受限等情况时,应积极行左心减压。
左心减压常用方法包括IABP、介入下房间隔造瘘、经胸右上肺静脉引流、联合左心室Impella等。
②右心室衰竭为主的AMICS患者:
pMCS可选择经皮右心辅助装置Impella RP系统等。
③双心室功能衰竭的患者:
可以使用双心室Impella系统,或采用VA-ECMO联合左心减压治疗。
(2)pMCS的使用时机
早期启动pMCS治疗AMICS的优点:主要是支持全身灌注、减轻心脏负荷、增强心肌做功、阻止休克进展;缺点:出血、溶血、血管入路并发症等器械置入相关风险。
经初始优化药物治疗后血流动力学持续性不稳定、心电活动不稳定、呼吸功能衰竭、冠状动脉高危病变、严重左心室功能受损患者,应积极考虑早期使用pMCS支持和足疗程使用。
当IABP辅助仍需较大量血管活性药物维持循环、心电活动仍不稳定、组织灌注不佳或呼吸衰竭不能改善时,应考虑尽早联合启动VA-ECMO、Impella等更高级别的pMCS支持。
如pMCS团队技术有限、血管入路不佳、pMCS置入的时间延误影响血运重建时机等,则应充分评估权衡pMCS应用的利弊。
6、呼吸支持
①机械通气:当患者吸入高流量氧气后动脉氧分压(PaO2)<60 mmHg,和/或氧饱和度<90%,和/或二氧化碳分压(PaCO2)>50 mmHg时,建议积极使用机械通气辅助呼吸。
②无创正压通气:无创呼吸对轻中度呼吸衰竭非常重要,无创正压通气应用于急性心原性肺水肿患者,能够缓解呼吸困难,提高氧合能力,降低气管插管率及病死率,其中持续气道正压和双水平气道正压都可作为首选通气方式治疗。
③有创通气:对于意识障碍和无创呼吸机辅助呼吸仍不能纠正低氧血症的患者,应及时行气管插管,转换为有创通气治疗。
7、急性肾功能损伤治疗
AKI诊断:
当 48 h内血肌酐增高>26.5 μmol/L,或7 d内血肌酐增高至≥基础值的1.5倍,或持续6 h尿量<0.5 ml/(kg·h)时,均可诊断为AKI。
CRRT启动时机:
对于AMICS合并AKI患者,由于血流动力学不稳定,建议采用连续性肾脏替代治疗(CRRT)或持续缓慢低效透析,并应早期启动治疗。
利尿剂无反应性水肿、药物难以控制的高血钾、严重代谢性酸中毒、非梗阻性少尿或无尿、尿毒症等需快速启动CRRT。
此外,液体超负荷(当累积的体液超过体质量的10%)也是开始CRRT的重要指标之一。终止CRRT:
终止CRRT的指征目前尚无统一标准,推荐患者临床病情好转和肾功能恢复后可暂停CRRT。
参考文献:
中华医学会心血管病学分会 中华心血管病杂志编辑委员会.急性心肌梗死合并心原性休克诊断和治疗中国专家共识(2021)[J]. 中华心血管病杂志,2022,50(3) : 231-242.


