WCLC 2023:Dato-DXd联合度伐利尤单抗模式在NSCLC一线治疗中展示巨大潜力(TROPION-Lung04研究)
时间:2023-09-11 16:57:43 热度:37.1℃ 作者:网络
2023年WCLC大会于9月9日至12日在新加坡举行,汇聚国际肺癌领域专家、学者和医疗专业人士,共同探讨肺癌领域的最新进展、研究成果和临床实践。通过丰富的专题报告、研讨会、海报展示和互动讨论,为与会者提供了一个全面了解肺癌领域最新动态和未来趋势的机会。
TROP2是由TACSTD2基因编码表达的细胞表面糖蛋白,主要表达于上皮细胞,在胚胎发育中扮演重要角色。TROP2在肺癌、胰腺癌、乳腺癌等多种肿瘤中高表达,可促进肿瘤细胞增殖、侵袭、转移扩散等过程,并且其高表达与肿瘤患者生存期缩短及不良预后密切相关。在非小细胞肺癌(NSCLC)患者中,高达64%的腺癌和高达75%的鳞状细胞癌中观察到TROP2表达[1,2],提示TROP2有望成为治疗NSCLC的重要分子靶点。
靶向TROP2 ADC是NSCLC领域的一个热点话题,多项探索TROP2 ADC联合治疗模式的临床试验在2023年WCLC大会中亮相[3,4],或将为晚期/转移性NSCLC提供一线治疗新选择。
TROPION-Lung04是一项多中心、开放标签、剂量递增/确认和剂量扩展的Ⅰb期研究,旨在6个队列中评估Dato-DXd+度伐利尤单抗±卡铂在无可靶向基因改变的初治或经治晚期/转移性NSCLC的安全性和有效性。本次WCLC大会首次报告了队列1-4的中期分析结果。
该研究纳入了≥18岁、ECOG PS为0/1、经组织学/细胞学确诊为晚期/转移性NSCLC,且无可靶向基因改变的患者。其中,队列1的患者和队列2的1例患者接受了≥1种含铂化疗方案和抗PD-1/PD-L1治疗,其他患者为初治或既往接受过≤1线全身化疗且未使用过免疫治疗。患者接受Dato-DXd(4 mg/kg,队列1/3;6 mg/kg,队列2/4)+度伐利尤单抗(1120 mg,所有队列)+至多4个周期的卡铂(AUC 5,队列3/4),Q3W,直至疾病进展 (RECIST v1.1)或出现不可接受的毒性。该研究的第一部分为剂量探索阶段,采用3‒6例患者的mTPI-2设计。根据观察到的剂量限制毒性(DLT),开放第二部分(剂量扩展,队列3为按需递减队列)。主要终点是安全性/耐受性。次要终点包括客观缓解率(ORR)和研究者评估的疾病控制率(DCR)(RECIST v1.1)。

图1.TROPION-Lung04队列1-4的研究设计
截止2023年03月06日,队列1(n=5)、队列2(n=19)和队列4(n=14)共有38例患者可评估疗效。由于队列1第1部分(n=5)完成且无DLT,开放队列2第1部分(n=3)。由于队列2中无DLT,跳过队列3,并开放队列4第1部分(n=6)。队列2(双联)和队列4(三联)的剂量扩展部分均未观察到DLT。
在队列2/4中,肿瘤细胞PD-L1表达<1%、1‒49%和≥50%的患者比例分别为31.6%/42.9%、31.6%/21.4%和36.8%/35.7%。队列2/4的中位治疗周期数为8.0/8.5;截止2023年03月06日,31.6%/50.0%的患者正在接受治疗。未发生给药相关死亡。
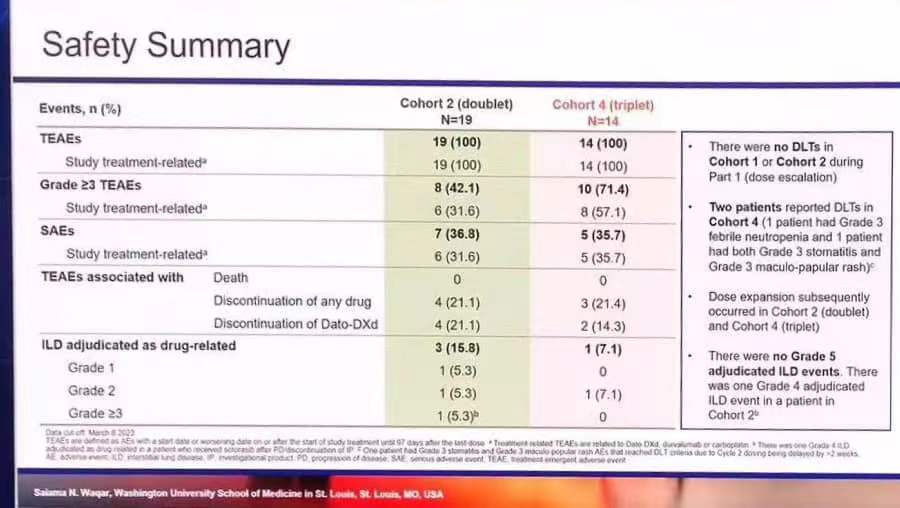
图2. TROPION-Lung04研究的安全性结果
在一线治疗时,6 mg Dato-DXd双联组(队列2,n=14)的ORR为50.0%[7例经证实的部分缓解(PR)],DCR为92.9%;而三联组(队列4,n=13)中,ORR为76.9%(9例经证实的PR,1例在DCO后证实的PR),DCR为92.3%。总人群中,双联组和三联组的ORR分别为47.4%和71.4%。在所有PD-L1表达水平的患者中均观察到缓解,且三联治疗的缓解率通常高于二联治疗。
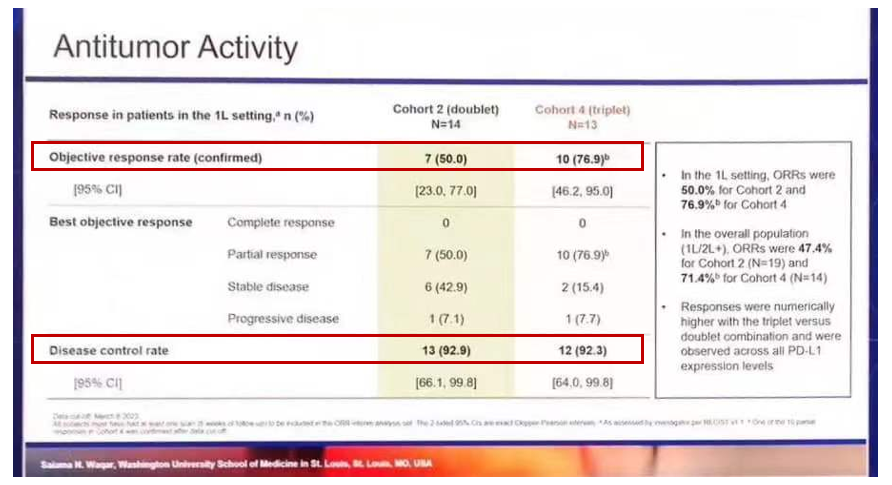
图3. TROPION-Lung04研究的肿瘤缓解结果
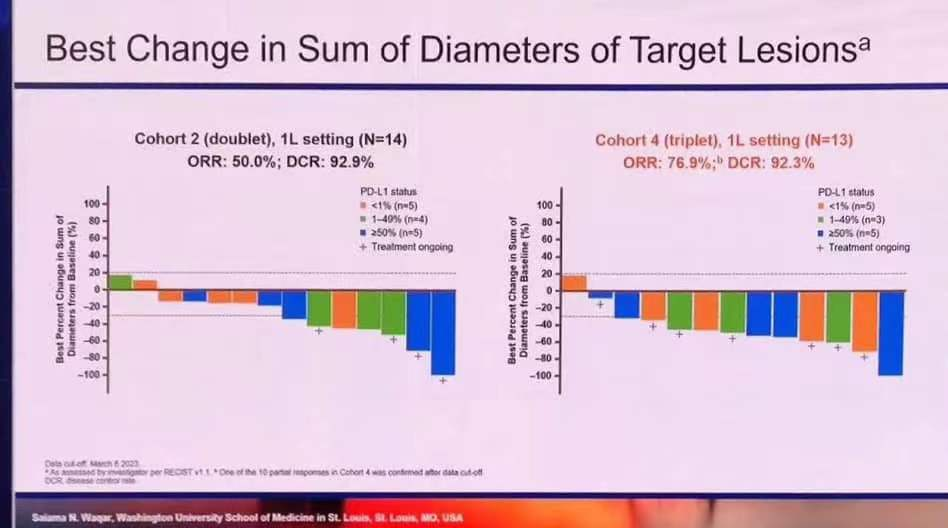
图4. TROPION-Lung04研究队列2和队列4的瀑布图
从研究进展来看,Dato-DXd已经率先在Ⅲ期研究中验证其卓越疗效和可控的安全性。后续布局多项研究将其治疗线数前移或探索联合用药模式,积极拓展NSCLC获益人群边界,以期覆盖更广泛人群,惠及更多患者。综合而言,Dato-DXd在NSCLC的适应症布局具有全球领先优势,有望引领TROP2靶向ADC药物研发赛道,开启肺癌TROP2 ADC元年。同时也期待更多TROP2 ADC在NSCLC领域取得新的突破,为更多患者带来治疗新选择和希望。
总体而言,Dato-DXd+度伐利尤单抗±卡铂在晚期/转移性NSCLC中表现出可耐受且可管理的安全性特征,与单个药物的已知特征一致。并且抗肿瘤活性较为显著,支持该联合方案在初治/经治且无可靶向基因组改变晚期/转移性NSCLC的后续探索和应用。
参考文献:
[1]Mito R, Matsubara E, Komohara Y, et al. Clinical impact of TROP2 in non-small lung cancers and its correlation with abnormal p53 nuclear accumulation. Pathol Int. 2020 May;70(5):287-294.
[2]Inamura K, Yokouchi Y, Kobayashi M, et al. Association of tumor TROP2 expression with prognosis varies among lung cancer subtypes. Oncotarget. 2017 Apr 25;8(17):28725-28735.
[3]Papadopoulos KP, Bruno D, Kitazono S, et al. Datopotamab Deruxtecan (Dato-DXd) + Durvalumab ± Carboplatin in Advanced/mNSCLC: Initial Results from Phase 1b TROPION-Lung04. 2023 WCLC. OA05.06
[4]Cho BC, Dols MC, Cabanillas RR, et al. Sacituzumab Govitecan + Pembrolizumab in 1L Metastatic Non-Small Cell Lung Cancer: Preliminary Results of the EVOKE-02 Study. 2023 WCLC. OA05.04
[5]Stepan LP, Trueblood ES, Hale K, et al. Expression of Trop2 cell surface glycoprotein in normal and tumor tissues: potential implications as a cancer therapeutic target. J Histochem Cytochem, 2011, 59(7):701-710.
[6]Shimizu T, Sands J, Yoh K, et al. First-in-Human, Phase I Dose-Escalation and Dose-Expansion Study of Trophoblast Cell-Surface Antigen 2-Directed Antibody-Drug Conjugate Datopotamab Deruxtecan in Non-Small-Cell Lung Cancer: TROPION-PanTumor01[J]. J Clin Oncol. Published online June 16, 2023.
[7]Bardia A, Hurvitz SA, Tolaney SM, et al. Sacituzumab Govitecan in Metastatic Triple-Negative Breast Cancer. N Engl J Med. 2021 Apr 22;384(16):1529-1541.
[8]Okajima D, Yasuda S, Maejima T, et al. Datopotamab Deruxtecan, a Novel TROP2-directed Antibody-drug Conjugate, Demonstrates Potent Antitumor Activity by Efficient Drug Delivery to Tumor Cells. Mol Cancer Ther. 2021 Dec;20(12):2329-2340.
[9]Cheng Y, Yuan X, Tian Q, et al. Preclinical profiles of SKB264, a novel anti-TROP2 antibody conjugated to topoisomerase inhibitor, demonstrated promising antitumor efficacy compared to IMMU-132. Front Oncol. 2022 Dec 23;12:951589.
[10]Nagai Y, Oitate M, Shiozawa H, et al. Comprehensive preclinical pharmacokinetic evaluations of trastuzumab deruxtecan (DS-8201a), a HER2-targeting antibody-drug conjugate, in cynomolgus monkeys. Xenobiotica. 2019 Sep;49(9):1086-1096.






