张真发教授组稿|赵晓亮医生:非小细胞肺癌围手术期免疫治疗的进展和思考-天肿经验
时间:2023-09-14 23:01:04 热度:37.1℃ 作者:网络
编者按:
【专家组稿】以匠心,敬初心。本期组稿由天津医科大学肿瘤医院张真发教授担任执行主编,特邀肺癌外科领域专家进行学术观点分享,共计4期,以供交流。
目前的肺癌外科,大部分是小结节的患者,对于小结节的手术方式,虽然有争议,但肺段/亚段切除以及楔形切除,必然有其适应症,也在临床中广泛应用。我们5年前提出“动脉先行-以动脉为核心的解剖性肺段切除”,随着时间的推移,我们觉得对于肺段切除的意义很大,可以使肺段切除变得更简单、准确。除了小结节,围手术期的治疗也是近年来的热点。辅助靶向治疗目前已有两项多中心临床研究证明能够延长总生存;而围手术期的免疫治疗,尽管有很多问题目前仍然弄不清楚,但是也给很多患者带来较大获益,正在获得大量的临床应用。
自Checkmate159实验在NEJM杂志报道II期探索性非小细胞肺癌免疫治疗的安全性和有效性,2015年成为非小细胞肺癌治疗领域的免疫治疗元年。
至今八年来,免疫治疗以星星之火可以燎原的态势,在不同瘤种、不同病理类型、不同分期全面铺开,明显延长了晚期肺癌患者生存时间,显著改善患者生活质量,应用人群不断扩大,应用场景从晚期二线至一线,再到目前关注度很高的局部晚期非小细胞肺癌围手术期治疗的应用不一而足。
Checkmate816作为全球首个前瞻随机对照新辅助化免治疗对比新辅助化疗III期临床实验,在2021年和2022年以高出对照组10倍的PCR(完全病理缓解)、超出单纯新辅助化疗组10个月的EFS(无事件生存)的结果双双报阳,达到了实验设计的双终点,同时术后复发、转移、死亡的风险下降37%(HR=0.63),基于此美国FDA在今年3月批准将新辅助免疫联合化疗作为IIA期及以上NSCLC患者的推荐治疗方案。
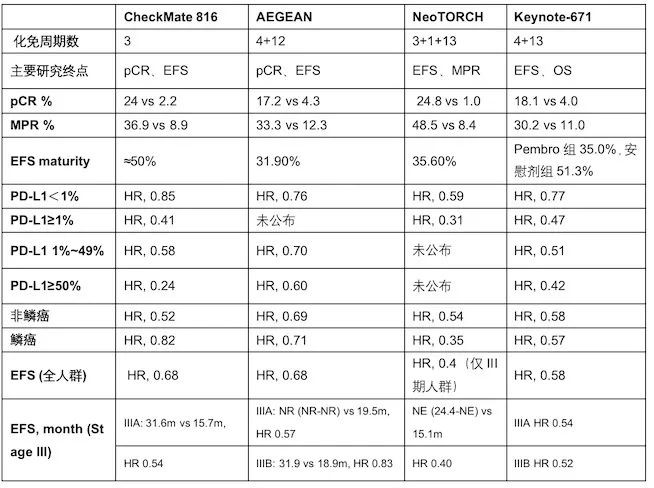
今年6月ASCO会议又以LBA(late breaking abstract)形式宣布帕博利珠单抗的keynote671实验中期结果,为确立化免新辅助+手术+免疫辅助围手术期全周期优选模式治疗结果,在实验组中EFS为NR尚未达到,单纯化疗组为17.0个月,HR=0.58,降低了42%的复发风险,在次要研究终点,即短期病理指标中,全周期化免联合依然存在碾压趋势,pCR率分别为18%:4%,MPR分别为30.2%:11.0%,联想到今年早些时间关于PDL1单抗度伐利尤单抗单抗为主要研究药物的AEGEAN实验和同样今年ASCO披露新辅助化免手术后辅助免疫治疗后的国产PD1单抗药物特瑞普利单抗的Neotorch实验的初步结果大体会带给我们20%左右的PCR,35%左右的MPR,两项实验2年EFS率相差不足1%,均在63%-64%(详见表1)。同时,由于传统意义的新辅助化疗临床降期率并不理想,5年OS收益提高4%,完全病理缓解率(PCR)不足5%,患者临床绝对受益不高,新辅助治疗后手术风险未见明显改善,不出意外,新辅助免疫联合化疗在局部晚期非小细胞肺癌患者中将体现出巨大临床优势,同时为处于边缘期的可切/不可切的非小细胞肺癌患者带来临床转化的希望。研究结果支持化免联合新辅助+手术+手术后免疫辅助的治疗模式在II-IIIB(N2)非小细胞肺癌患者中的临床应用,再次创立了新的围手术期模式。
表1 目前免疫治疗围手术期治疗临床实验初步结果
天肿肺部肿瘤科作为全国最早接触和开展新辅助免疫治疗局部晚期非小细胞肺癌临床研究中心之一。自2018年针对局部晚期NSCLC患者开展新辅助免疫治疗至今,我中心共经治围手术期免疫为治疗手段的NSCLC患者超过600例,并牵头主持多项有关新辅助免疫相关的全国多中心临床研究,我中心牵头关于替雷利珠的全国多中心III期注册研究“一项在可切除的 II 期或 IIIA 期非小细胞肺癌中比较替雷利珠单抗(BGB-A317,抗-PD-1 抗体)或安慰剂联合含铂双药化疗作为新辅助治疗,后续辅以替雷利珠单抗或安慰剂辅助治疗的有效性和安全性的随机、双盲、安慰剂对照的 3 期研究”已顺利完成,完成入组450例,我单中心完成入组128例,并且达到实验之初所设定的目标,主要研究终点报阳,实验组MPR率超过50%,PCR率在30%左右,部分患者达到临床降期,手术难度改善,手术创伤缩小。
此外,随着IMPOWER 010和Keynote091实验结果的公布,术后辅助免疫治疗的地位也得到了确立,两项实验的结果相互印证,阿特利珠单抗及帕博利珠单抗均有条件获批非小细胞肺癌术后辅助治疗适应症。至此,新辅助化疗+免疫治疗-手术-术后辅助免疫治疗的围手术期全周期治疗模式似乎成为可手术非小细胞肺癌治疗的标准模式,但随着临床的应用扩大,治疗和相关的研究逐步进入深水区,出于对治疗人群和治疗方法的个体化,精细化,准确化的要求,对于非小细胞肺癌的围手术期免疫治疗的模式和内容上仍有很多方面需要探讨、有待完善,并达成更为广泛的共识。
首先,对于哪些是需要围手术期新辅助化免治疗的人群仍有争议。诚然,随着新辅助治疗中免疫治疗的加入,大量处于边界可切/不可切的III期非小细胞肺癌患者达到临床降期的目的,并最终获得的手术根治的机会,这也使得对于哪些是可以手术的局部晚期的非小细胞肺癌患者的界定范围更加模糊,对于化疗时代常规意义上不能手术的某些特定类型如锁上淋巴结转移,对侧肺单发转移的患者新辅助化疗免疫治疗的效果,是否可以手术,特别是长期治疗效果仍没有确切答案,对于此,我中心对部分锁上淋巴结转移的IIIB期患者和部分严格适应症挑选的IVA期非小细胞肺癌患者也进行了新辅助免疫综合治疗安全性及有效性的关注和探索,截止目前,入组的5例手术患者均达到MPR或者PCR疗效,达到很好的临床治疗结果。在另一方面,对于可接受新辅助治疗最早分期仍有争论,Checkmate816入组患者包括IB期患者,但通过分析发现围手术期新辅助治疗过程中HR及EFS的收益与患者的分期成显著的正相关,通过围术期治疗收益最高的患者往往都是IIIA期局晚非小细胞肺癌患者。而同时,Checkmate816的结果提示,实验组经过新辅助化免治疗后最终接受手术治疗的患者比例为83%,AEGEAN实验组最终接受手术患者的比例为80.6%。换而言之,有接近20%的非小细胞肺癌患者在接受新辅助化免治疗后丧失了手术根治的机会,虽然包含疾病进展的情况,但对于IB期等偏早期的患者是否有必要接受新辅助化免治疗确实需要深思熟虑和更多的临床权衡。
其次,对于在晚期肺癌的研究中,相较于PDL1单抗,PD1单抗在疗效上的表现更为突出;虽然目前没有关于PD1单抗和PDL1单抗在围术期的头对头研究,但仅从直观上的数字比较,PDL1单抗在围术期治疗中的表现并不劣于PD1单抗(Keynote671与AEGEAN实验),对于两种单抗在术前新辅助或术后辅助治疗阶段使用的原则亦或是治疗介入的时间目前仍无规定或共识。为解决此类问题,我中心亦开展真实世界研究,以手术时间点为界,在观察记录术前术后治疗药物上的选择外,同时对治疗的有效率、安全性以及治疗期间产生的副作用进行详尽的观察分析,以期对上述问题的解决提供参考。
此外,新辅助免疫治疗药物种类增多,由开始的经典的PD1单抗,到PDL1单抗,以及目前临床探索研究中越来越多诸如PD1+VEGF双抗、PD1+LAG3双抗等多靶点药物,与此同时,我们还在积极探索新辅助治疗中的“去化疗化”,单纯的双靶点或双免药物的应用,在保证治疗效果的同时,化疗相应的血液学及非血液学毒性明显改善,患者的依从性更好,治疗效果提高。我中心牵头开展的全国多中心AK112-205实验即为PD1与VEGF的双抗在II至IIIA期围手术期化免及术后辅助综合治疗的II期临床研究,值得一提的是,应用双抗单药的治疗组PCR达到30%,MPR达到60%左右,这也让我们在局晚期非小细胞肺癌的治疗中看到去化疗化治疗的可能性。此外,除用药种类有待探索外,对于围手术期免疫治疗用药的周期数、时间间隔、用药方式,同样有多种方案。此次在ASCO上报道的Neotorch实验更是创新性的应用的“3+1+13”围手术期免疫治疗模式,即术前3周期,术后1周新辅助/辅助免疫化疗综合治疗,随后13个周期术后辅助免疫治疗维持。对于新辅助免疫治疗的周期数,2021年在《Translational Lung Cancer Research》刊登的《NSCLC新辅助免疫治疗国际专家共识》提出,其中对于新辅助免疫治疗的周期数定为2-4个周期为宜,治疗后手术达到PCR的患者给出建议术后辅助免疫治疗维持至少一年时间,但对于术前、术后不同的时间节点应用的周期数并无统一。目前对于围术期免疫治疗的全程管理和细节控制的研究层出不穷,有真实世界研究结果认为将相较于同时应用免疫治疗和化疗,将免疫治疗延后至化疗后48小时应用,有效率和患者受益更佳,当然这些研究的结果需要更大的样本和前瞻的研究结果验证。
最后,新辅助/辅助免疫治疗的疗效预测、预后因子的筛选也是影响免疫治疗应用的重要因素之一。新辅助免疫治疗中,多项II期、III期临床实验结果表明,PCR或者MPR与非小细胞肺癌患者预后、总生存(OS)呈显著强烈的正相关关系,PCR或主要病理缓解(MPR)可能是一种较为理想的预后以及新辅助免疫治疗疗效的预测因子,但PCR状态不再作为术后是否进行辅助免疫治疗的决定因素,而辅助目前肿瘤分子残留检测(MRD)及术后ctDNA动态监测则有可能成为是否需要术后免疫治疗等辅助治疗的关键因素之一。同时,理想的预测因子应具有无创、可重复、稳定性高的要求,依据目前临床实践,PDL1的表达水平多与辅助免疫或新辅助免疫治疗效果成呈正相关。但Keynote091实验又得到反例,在术后免疫辅助治疗中,PDL1 > 50%的强阳性亚组中,得到阴性结果,虽然作者解释为“对照组的超常表现”,但也说明PDL1作为疗效预测因子表现仍不稳定,需要更多的研究结果双向验证。
综上,我中心建议应加强免疫治疗的全程管理,对于局部晚期肺癌患者的围手术期治疗设计,贯穿新辅助治疗和术后的辅助治疗阶段,同时,这也是目前国际临床实验研究的主流方向,在扩展入组分期适应症的同时,同样注重免疫药物治疗的全程干预。针对明显具有异质性的局部晚期非小细胞肺癌的患者而言,系统检测、个体化、精准化是围术期免疫治疗干预的前提;对可能发生的免疫治疗相关性不良反应及术后出现复发高危因素的患者,提前预警,提早干预;在严格把控手术风险和综合治疗干预的同时,探索性的扩大手术治疗的适应症,争取不遗漏任何一个可能从手术治疗中获益的局晚期患者。虽然目前我们在围术期免疫治疗的治疗模式、用药方式、疗效标志物等诸多细节上仍有待于进一步细化和讨论以达成更为广泛的共识,但可以预料,在不久的将来,免疫治疗必将在局晚期非小细胞肺癌患者的围术期综合治疗中发挥更加重要的作用。
主编评语
目前的肺癌外科,除了小结节的热点,就是围手术期的免疫治疗。随着大家对免疫治疗应用的增多,我们对免疫治疗的应用也产生了更多的问题。其实核心问题是什么样的患者需要应用免疫治疗以及怎样应用的问题。个人认为,一些人适合应用新辅助免疫,一些人适合围手术期应用,而一些人只适合辅助免疫治疗。也就是说新辅助、辅助还是围手术期应用各有其适应症,需要大家的研究和总结。


