【Blood】BCMA CAR-T治疗后神经毒性的发生率、表现、管理及结局
时间:2023-10-18 14:31:52 热度:37.1℃ 作者:网络
BCMA CAR-T神经毒性
CD19 CAR-T 细胞治疗可发生免疫效应细胞相关神经毒性综合征 (ICANS),介于意识模糊至重度脑水肿,而在 BCMA CAR-T 细胞方面,多发性骨髓瘤的关键临床试验中发生了独特的毒性,包括帕金森样症状。但因为这类疗法最近才获得商业批准,真实世界的数据仍然很少。
近日《Blood》发表一篇文章,介绍了马萨诸塞州总医院在 BCMA CAR-T 细胞治疗后神经毒性的发生率、表现、管理和结局方面的经验。

研究结果
作者分析了马萨诸塞州总医院在2016-2023期间接受BCMA CAR-T治疗的多发性骨髓瘤患者共76例(表1),在 CAR-T 细胞输注后12个月内评价毒性和结局。患者既往接受过多线治疗(中位既往治疗5.0;范围,1-11)。7例患者 (9.2%) 存在基线症状,包括轻度意识模糊、震颤、神经根病和表达性失语症。无患者存在中枢神经系统疾病。
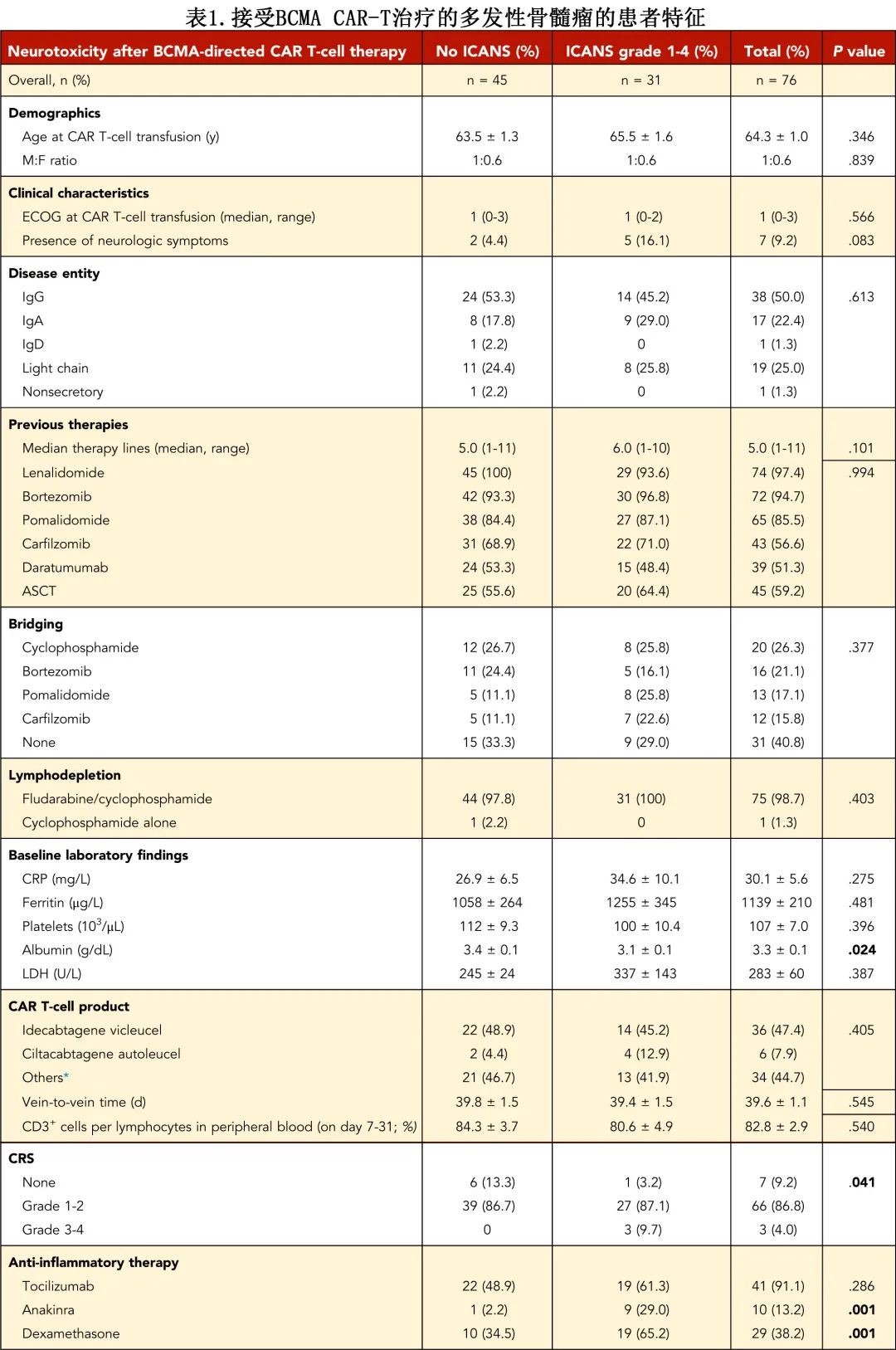
BCMA CAR-T 细胞治疗后,31例患者 (40.8%) 表现出新的神经系统症状,包括6例患者出现重度症状(7.9%;图1A)。轻度ICANS(美国移植和细胞治疗学会1-2级)的特征为头痛、表达性失语症和中度意识模糊,重度ICANS(3-4级)表现为实质性脑病,转化为严重意识模糊或觉醒水平受损(1例并发败血症的患者需要插管)。ICANS 常伴有震颤或肌阵挛。未观察到神经病变。轻度 ICANS 的中位症状发作时间为第3天(范围,0-27),重度 ICANS 的中位症状发作时间为第0-1天(范围,0-4)。
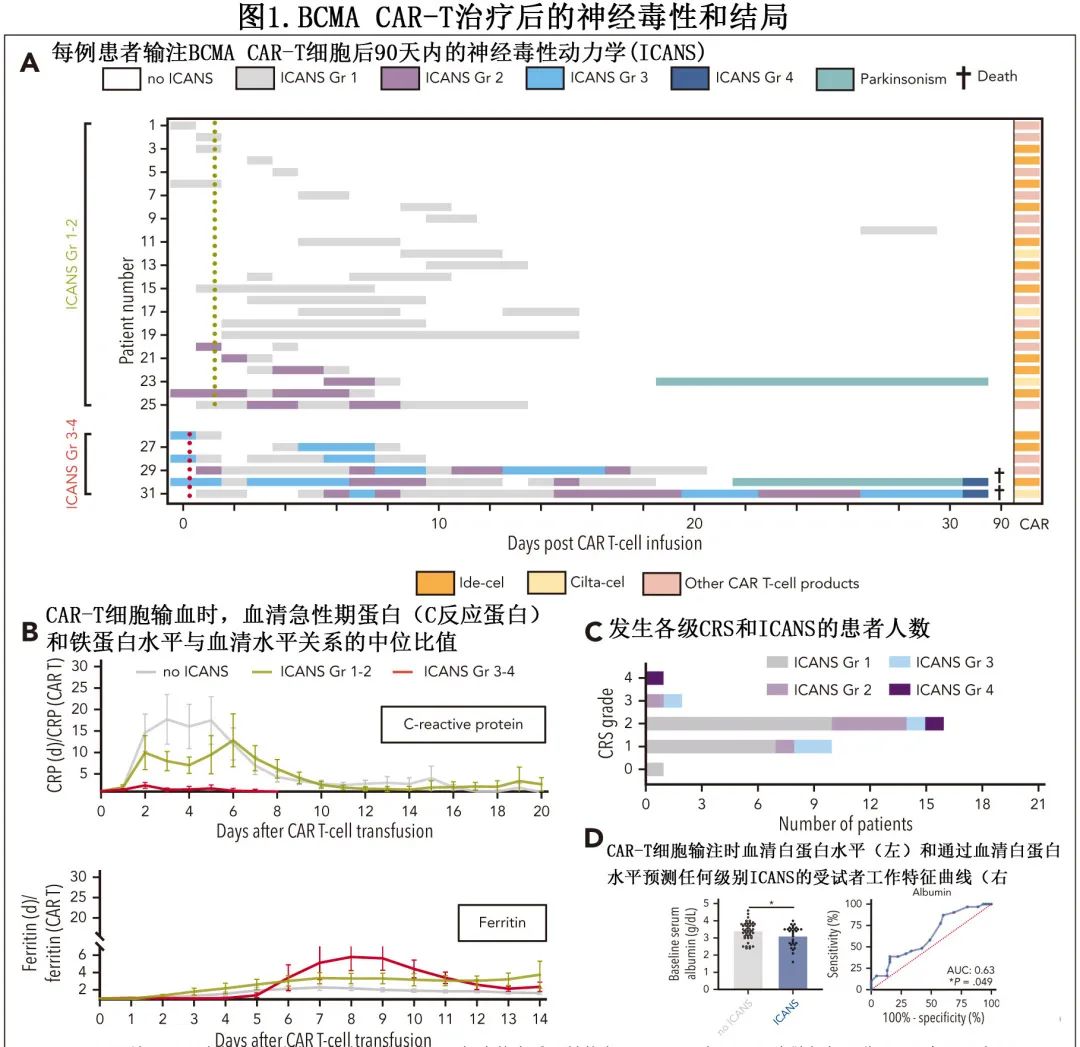
尽管没有观察到炎症标志物的明显血清特征(图1B),但全身炎症和 ICANS 之间有密切的联系,几乎所有神经毒性患者都表现出细胞因子释放综合征(CRS;P=0.041;图1C)。发热≥38℃作为早期 CRS 体征,且在重度 ICANS 患者中倾向于更早发生(0.3±0.4 vs 1.5±0.2天;P=0.143)。在 ICANS 患者中观察到 CAR-T 细胞输注时白蛋白水平较低,可能识别风险升高的患者(曲线下面积,0.63;P=0.049)(图1D)。
ICANS 分级为1-2级的5例患者和 ICANS 分级为3-4级的5例患者进行了脑电图 (EEG) 检查,多可发现背景减慢(1-2级:60%[3/5] 的EEG;3-4级:80%[4/5] 的EEG)。未发现癫痫发作,但在1例 ICANS 2 级和2例 ICANS 3 级患者中证实了全身节律性δ活动;且抗癫痫药未显著改善症状。影像学未显示异常。轻度 ICANS 的管理包括支持性治疗和白介素-6(IL-6) 受体拮抗剂托珠单抗治疗CRS;重度 ICANS 接受大剂量类固醇和 IL-1 受体拮抗剂anakinra治疗。骨髓瘤亚型、托珠单抗使用和特定市售 CAR-T 细胞产品均与 ICANS 发生或特殊神经毒性动力学无关。在并发败血症的情况下发生2例死亡。
急性 ICANS 完全恢复后,2例患者(2.6%;1例高肿瘤负荷,1例低肿瘤负荷)出现帕金森样症状。1例患者在 idecabtagene vicleucel 给药后第22天出现意识模糊和运动迟缓伴肌张力增加,[18F] FDG-PET显示双侧基底神经节代谢减退(图1E);尽管采用了多模式方法(类固醇、anakinra和左旋多巴/卡比多巴),但症状仍恶化,患者最终死于细菌性和真菌性败血症。第2例患者在 ciltacabtagene autoleucel 给药后第19天出现意识模糊、姿势不稳、轻度震颤和运动迟缓伴轻躁狂和低音调,[18F] FDG-PET显示额叶代谢减退;输血后2周循环淋巴细胞流式细胞术检测到高比率(99%)CD3+ T细胞;地塞米松(初始剂量10 mg,每6小时一次;缓慢减量)和anakinra(100 mg,每12小时一次;10天)给药后2周内,意识模糊和运动迟缓改善;在大剂量环磷酰胺(2000 mg/m2,计划给药一次)降低循环 T 细胞数量后4周内,患者姿势稳定性完全恢复。
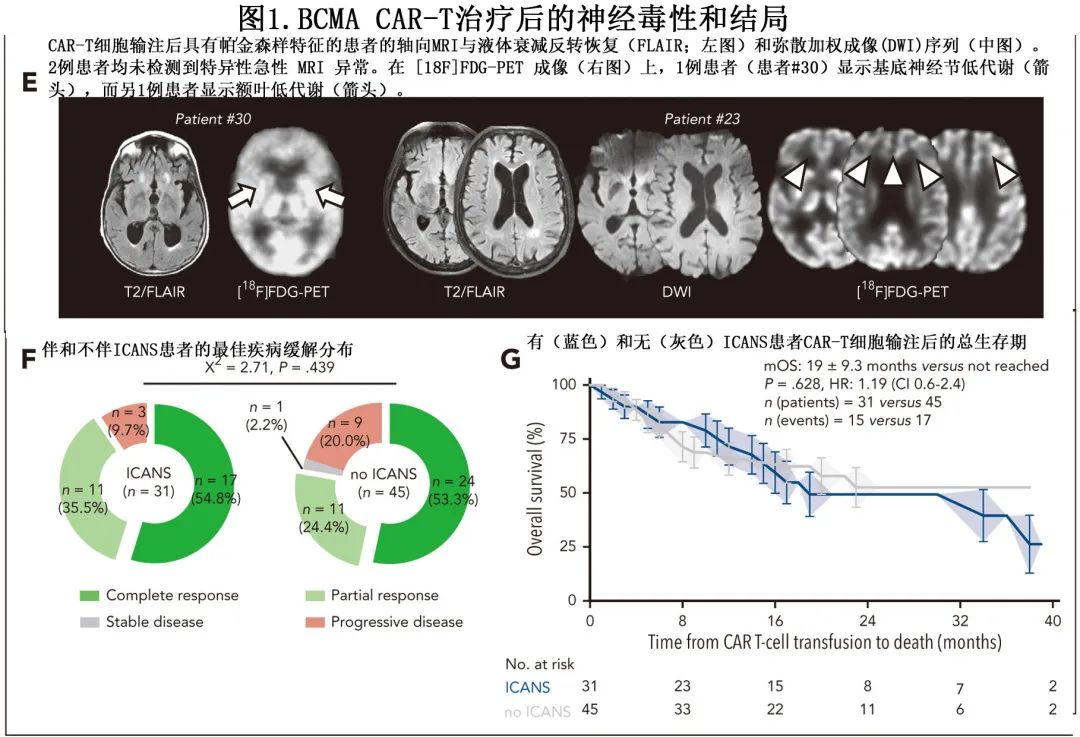
63例患者(82.9%;包括2例有帕金森样症状的患者)达到完全或部分疾病缓解,发生或未发生 ICANS 的患者之间无缓解差异(P=0.439;图1F),中位随访22个月,ICANS与总生存期无关(ICANS的风险比=1.19;P=0.628)(图1G)。此外比较重度 ICANS 患者与轻度 ICANS 患者时,结果仍然如此。13例患者因疾病进展接受第二次 CAR-T 细胞输注;1例首次 CAR-T 细胞输注后出现轻度 ICANS 的患者出现重度ICANS,而在既往无 ICANS 的患者中仅观察到轻度症状。
讨论&总结
该研究中ICANS的发生率为41%,高于BCMA CAR-T的关键研究。该队列包括临床表现较差的老年患者,这些患者可能不适合接受既往临床试验的治疗,并且这些临床因素易患神经毒性。然而ICANS症状通常为轻度和一过性,因此并未改变该队列的生存率。但谨慎起见,也不能排除可能的筛选偏倚。该研究观察到的神经毒性频率也略高于既往真实世界样研究。低血清白蛋白(可能反映广泛疾病或基线炎症)或高级别 CRS 患者存在 ICANS 风险。重要的是,重复 CAR-T 细胞输注似乎不会增加 ICANS 风险,但需要在更大的队列中得到证实。
临床 ICANS 症状主要包括不同程度的脑病,常可见 EEG 异常。在 CD19 CAR-T 细胞治疗后也有这样的发现,支持具有相似的发病机制。以早期发热为特征的全身性炎症与高 CRS 率之间存在密切关联,支持全身性促炎性细胞因子是 ICAN 的驱动因素。CD19 CAR-T 细胞治疗后,针对脑壁细胞的交叉反应性可能导致 ICANS 率升高。
值得注意的是,BCMA CAR-T治疗后可能发生复杂的运动障碍重组帕金森综合征。对基底神经节中BCMA+ 细胞的On-target–off-tumor效应是一种机制;该队列中观察到的显著 CAR-T 细胞扩增、环磷酰胺对症状的有效性和基底神经节代谢减退可能支持该假设。然而可逆性和额叶代谢减退也提示其他病理机制,仍有待阐明。值得注意的是,在使用 ciltacabtagene autoleucel 和 idecabtagene vicleucel 后均观察到帕金森样症状;不同CAR产品(包括试验性)是否具有不同的风险特征尚不清楚,因为由于研究报告限制而无法提供更详细的结果。但症状可能是可逆的;最佳治疗、长期结局以及帕金森样症状与特异性 CAR-T 细胞产品或 CAR 动力学的相关性仍有待确定。尽管从该初步数据中无法得出明确的结论,但减少循环 CAR-T 细胞数量的策略(例如环磷酰胺)可能起作用。此外该研究中未观察到既往报告的神经病变。
总的来说,该研究结果证明了 BCMA CAR-T 细胞治疗整体可控的神经毒性特征。但有必要对治疗方案进行研究,因为可能发生重度急性神经毒性和迟发性运动功能减退疾病。
参考文献
Karschnia P,et al. Neurologic toxicities following adoptive immunotherapy with BCMA-directed CAR T cells.Blood . 2023 Oct 5;142(14):1243-1248. doi: 10.1182/blood.2023020571.


