【衡道丨笔记】食管基底样鳞状细胞癌临床病理特征
时间:2023-10-22 23:33:12 热度:37.1℃ 作者:网络
内容摘要
病理组织学特点
(1)肿瘤细胞以基底样细胞为主,体积较小,形态较一致,嗜伊红胞质少,核呈圆形或卵圆形,深染,核仁一般不明显,核分裂象常见。
(2)肿瘤细胞排列密集,呈大小不一的巢状、大分叶状、筛孔样、假腺样、条索状排列。
(3)癌巢周边癌细胞常呈栅栏状排列,较大癌巢中央可见非角化的粉刺样坏死。
(4)癌巢内与癌周间质常可见透明基底膜样物质沉积,部分病例呈小梁状与假筛孔腺样结构,其腔内可见淡蓝色黏液样物。
(5)表面黏膜鳞状上皮可呈不典型增生至原位癌,可见密切伴行的鳞状细胞成分(浸润性鳞癌或个别鳞状细胞分化或角化),也可见伴行的其他肿瘤亚型。
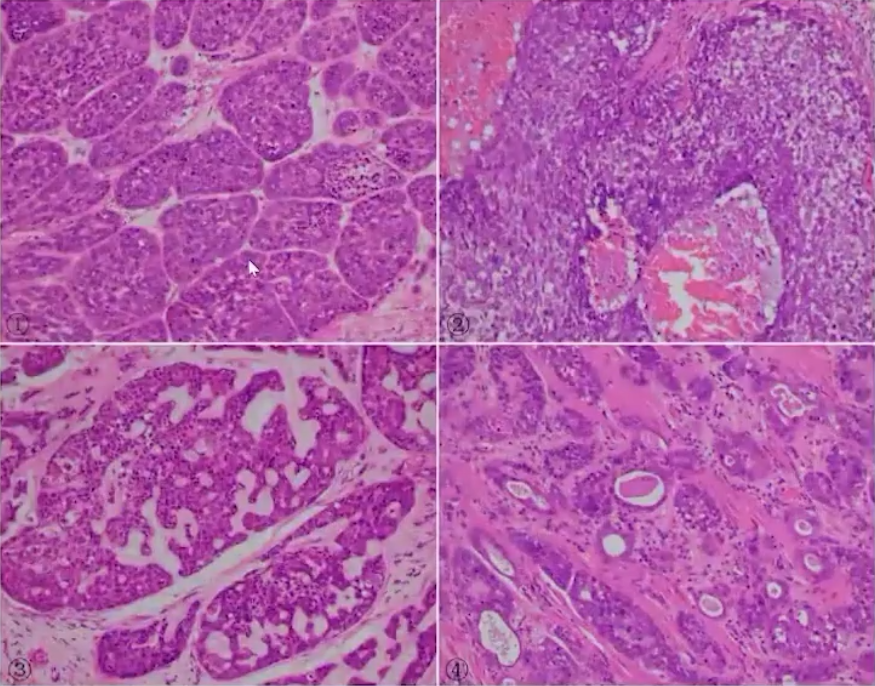
-
食管BSCC镜下形态多变,可伴行鳞癌、癌肉瘤、小细胞癌、腺癌等成分,需要病理医师多部位取材,多视野观察。
-
依据是否有伴行成分,食管BSCC可分为单纯型和混合型,而后者BSCC成分比例的变化较大(5%~95%)。
-
一般认为BSCC应以基底样细胞为主要成分(>50%),Sato-Kuwabara等研究中BSCC成分均大于90%,但是在一些研究中BSCC成分要求并不严格,如Li等研究中BSCC成分比例10%~90%。
-
混合型食管BSCC对BSCC成分比例并没有明确的界值,不同研究中人群纳入标准不同,可能造成不同研究间难以进行比较分析。
发现及流行病学特点
1986年Wain等首先报道了10例头颈部病例,命名为BSCC,它具有独特的形态学特征:
(1)小叶状实体生长,与表面黏膜相连;
(2)密集的小细胞,胞质少;
(3)核深染,无核仁;
(4)含有黏液样物质的小囊腔隙,PAS和/或AB可着色。
其他特征包括瘤巢中央小灶或大灶凝固性坏死,间质玻璃样变。
1984年,Epstein等首次提出食管癌伴有腺样囊性分化,其实代表一种分化差的基底样肿瘤,而不同于涎腺起源的腺样囊性癌。
自此,有关食管BSCC的报道逐渐增多。
组织形态学差异:
1、除外囊性、筛状形态,伴有实体状或基底样区域;
2、基底样核,核分裂像易见,2-3个/HPF;
3、与表面鳞状上皮的连续性,伴有原位癌、鳞状分化。
截至2022年12月,PubMed可检索到食管BSCC命名文献86篇,其中55.8%为个例报道,10例以下研究占12.8%,30例以下研究占20.9%,多于100例的报道仅占4.7%。文献报道的发病率相差悬殊,0.07%~11.3%不等。
总结4篇多于100例食管BSCC数据:
男性患者多于女性,男性比例为71.1%~87.6%,
中位年龄61岁,
中段食管比例较高(49.3%~62.0%),
肿瘤平均直径45.8~500mm,
多数有吸烟饮酒史。
中国医学科学院肿瘤医院报道的数据中,BSCC大体主要表现为髓质型(48.6%),其次为蕈伞型(19.7%)。
患者最常见的临床症状为吞咽困难(89.4%),其他症状包括体重减轻、胸骨后疼痛等。
免疫表型
目前BSCC研究中的抗体主要分为4类:
上皮性抗体:细胞角蛋白(CK)7(7.7%~54.5%)、CK14(50.0%~100%)、CK17(28.6%)、CK18(0~76.2%)、CK19(40.0%~87.5%)、CK34βE12(100%)、广谱细胞角蛋白(CKpan,96.8%~100%)、癌胚抗原(0~40.0%)、上皮细胞膜抗原(EMA,13.6%~100%)、p63(100%)、p40(100%)、CK5/6(100%)。
肌性抗体:平滑肌肌动蛋白(SMA,0~50.0%)、肌动蛋白(0~50.0%)、S100蛋白(0~50.0%)。
神经内分泌抗体:神经元特异性烯醇化酶(NSE,0~75.0%)、突触素(0~28.6%)、嗜铬粒素A(CgA,0~28.6%);多表现为单个抗体阳性。
细胞增殖相关抗体:Ki-67(30.0%~90.0%)、p53(40.0%~91.3%)、bcl2(40.0%~86.9%)。
以上抗体,在不同食管BSCC研究中的阳性率存在较大差异,可能与样本量大小、选择的抗体克隆号、免疫组织化学结果判读方式等方面的差异相关。
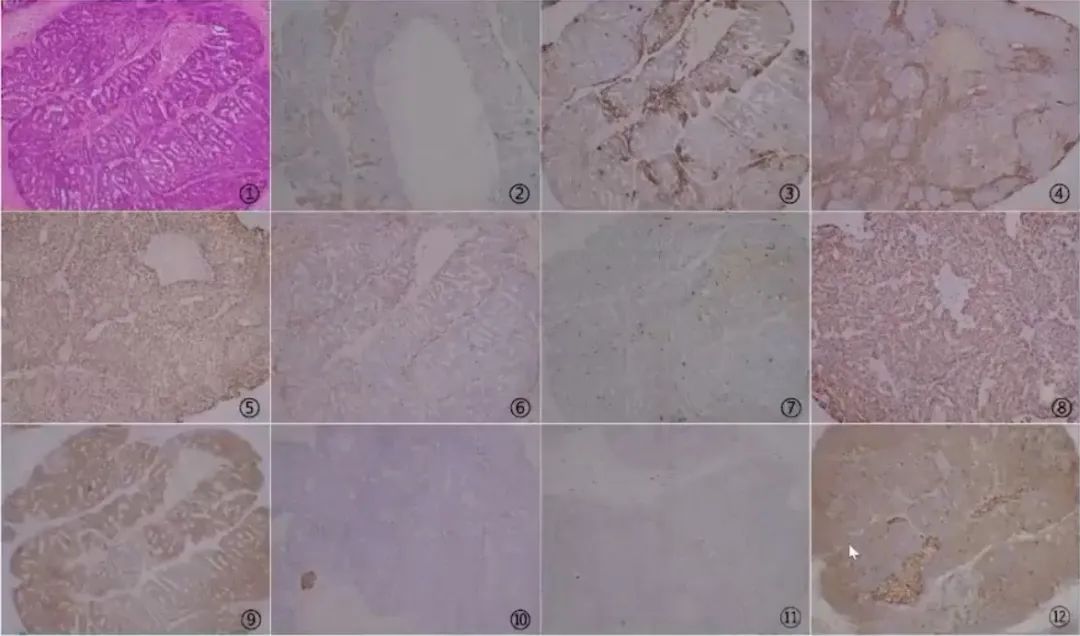
CK14局灶阳性、CK19局灶阳性、HCK局灶阳性、p40阳性、平滑肌肌动蛋白阴性、S100蛋白阴性、Ki67约90%阳性、bcl2阳性、突触素阴性、p16阴性、SFRP1阳性表达
超微结构
-
电镜下超微结构,BSCC的肿瘤细胞很幼稚,呈多角形,胞质少,胞质内细胞器数量稀少,含少量张力丝原纤维,可见游离核糖体;核染色较浅,染色质分布均匀;细胞之间可见桥粒及连接复合体。
-
也有报道可见细胞间腺样腔隙(原始腺腔)与细胞外间隙,腔缘可见微绒毛;细胞外间隙内含重叠基板样物。
-
超微结构提示肿瘤细胞既有鳞状上皮分化,又有腺上皮分化。
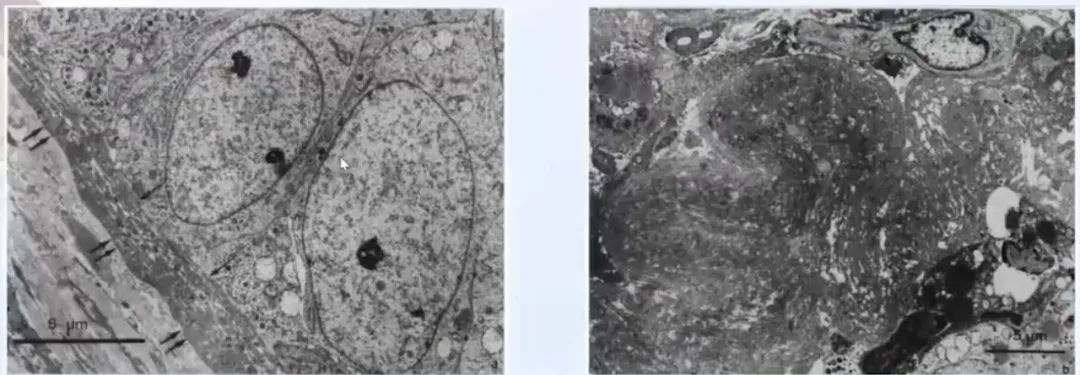
组织学来源
食管BSCC的组织起源,目前尚不清楚。
大部分研究者认为其起源于食管上皮底层中的全能干细胞,具有多方向分化潜能。
这一观点能解释BSCC具有复杂的组织学类型和免疫表型。
分子生物学特征
Sauer等利用癌症基因组图谱(TCGA)的BSCC和ESCC数据,发现两者TP53突变、CDKN2A/B缺失和CCDN1扩增水平相似,基因学水平存在相似性。
Li等在多组学水平分析BSCC成分和ESCC成分的分子差异,同样发现两者基因突变谱相似,而与血管生成、基底膜和上皮间质转化相关的基因在BSCC中表达水平明显上调,KRT14(鳞状分化)和CCL21(免疫反应相关)在BSCC中表达水平明显下调。
鉴别诊断
实体型腺样囊性癌:无鳞状分化灶,不伴有表面上皮的异型增生或原位癌,缺乏BSCC瘤巢中粉刺样坏死,核小形态一致,核分裂象少,胞质透明,SMA、S100蛋白阳性。MYB在两者鉴别诊断中的价值,尚需要进一步的研究数据证实。
小细胞神经内分泌癌:片状核深染小细胞,镶嵌状排列,无明显癌巢周边栅栏状排列,间质少,片状坏死,免疫组织化学至少表达2种以上神经内分泌标志物。
腺鳞癌:有明确的导管腺癌灶,内衬腺上皮而非基底细胞样细胞,免疫组织化学低相对分子质量CK8呈阳性表达,无巢内及周围的基底膜样物质沉积。
低分化鳞癌:细胞异型性明显,缺乏BSCC的成分和结构。
-
当食管BSCC缺乏鳞状细胞成分时,形态酷似小细胞癌,而两者治疗方案差异较大,鉴别诊断极其重要;
-
lshida等报道了34例具有小细胞癌样形态特点的BSCC,发现所有病例p40均阳性,而突触素和CgA均为阴性,42%病例表达CD56,8%病例表达p16;
-
作者认为小细胞癌样形态特点常发现在活检BSCC标本中,可能与活检过程中的挤压损伤有关,p16与CD56联合使用有助于两者的鉴别诊断。
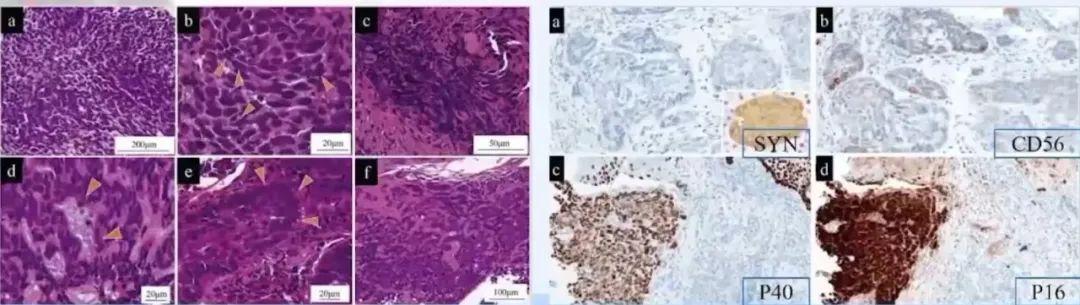
治疗
目前食管BSCC无标准的治疗模式,规范的手术切除被认为是有效的治疗方式。
Maebayashi等认为对于拒绝手术切除的老年患者,局部放疗是可行的。
对于BSCC新辅助治疗疗效的报道,目前比较少。
新近Li等研究显示,BSCC患者对新辅助免疫联合化疗的治疗反应倾向于比普通ESCC患者差(33.3%对比65.6%);而对新辅助化疗的治疗反应与普通ESCC患者相似(42.9%对比42.9%),提示BSCC患者可能不能从新辅助免疫治疗中获益。
随着内镜诊疗技术的发展,一些早期病变可行内镜下切除治疗。
Shiratori等总结了目前报道为黏膜下肿物的早期BSCC,这些病例均接受了内镜下切除治疗,仅1例后续补充了局部放疗,作者认为内镜下治疗是早期BSCC的有效治疗方式。
而Takii等报道了2例表浅BSC伴血管侵犯,早期即发生淋巴结、肝和肺转移,推荐表浅BSCC接受多模式治疗。
预后
-
国内外一些研究中心对患者的预后进行了分析,得出不同的结论。
-
在一些小样本对比研究中,也发现BSCC与ESCC患者的预后差异无统计学意义。
-
Salami等利用SEER数据库,整合16158例食管癌信息,比较了173例BSCC和15985例ESCC的临床病理信息,发现BSCC患者的生存优于ESCC(中位生存时间:14个月对比8个月,P<0.01;3年生存率:25%对比17%)。
-
进一步分期分析,Ⅰ~Ⅱ期患者中,BSCC患者的生存优于ESCC(中位生存时间:33个月对比15个月;3年生存率:45%对比30%);而在Ⅲ~Ⅳ期患者中,两者差异无统计学意义。


