实现CR和术后PCR!一例局部晚期食管癌新辅助免疫治疗的探索
时间:2023-11-27 16:27:04 热度:37.1℃ 作者:网络
食管癌是全球范围内最常见的恶性肿瘤之一,而我国食管癌疾病负担较重,每年新发病例数约占全球总例数的50%。由于食管癌患者的早期临床症状不明显且难于发现, 因此大多数患者确诊时已为局部晚期或存在远处转移,预后较差,研究显示,早期(I期)患者5年的总生存(OS)率为80%~90%,而局部晚期(IB~IVA期)患者5年OS率仅为14%~26%,。
如何进一步提升局晚期食管癌的生存率,一直是临床研究及临床实践中积极探索的问题。近年来,随着免疫治疗进展,免疫治疗已进军食管癌领域二线治疗和一线治疗,甚至在局部晚期食管癌的围术期中也具有潜在的疗效。本文特分享一则斯鲁利单抗联合化疗用于局晚期食管癌患者术前新辅助治疗的真实临床病例,供广大同道参考。
病例介绍
一、 基本情况
基本信息:患者男性,60岁。
主诉:因“吞咽困难4月余,确诊食管癌2月”于2023年4月14日11时33分入院。
既往史:患者过去体质良好。否认高血压、糖尿病、冠心病等病史。
现病史:患者2022-11无明显诱因出现吞咽困难,且进行性加重,目前可进食半流食,无饮水呛咳,无咳嗽咳痰,无声嘶气短,无胸闷胸痛等不适,为行诊治就诊于河津市人民医院,胃镜示:食管癌,慢性非萎缩性胃炎伴肠化。活检病理:(食管)中分化鳞癌,(胃窦)粘膜中度慢性炎,腺体中度肠化,局灶腺体腺上皮细胞轻度不典型增生。、
二、 入院相关检查
2023-02-18胸腹CT示:
1.食管中段肿物,符合恶性肿瘤改变,详见描述,纵隔内多发增大淋巴结,请结合临床。
2.右肺下叶外基底段结节(低危),建议年度复查。
3.右肺中叶支气管轻度扩张;左肺下叶支气管管腔内高密度影,考虑粘液栓可能,建议复查。
4.左侧肾上腺结节状增粗,请结合临床。我院病理会诊:(食管)1号切片呈恶性肿瘤,倾向为鳞状细胞癌,取材较表浅,请结合临床。2号切片呈慢性炎伴腺上皮肠化。
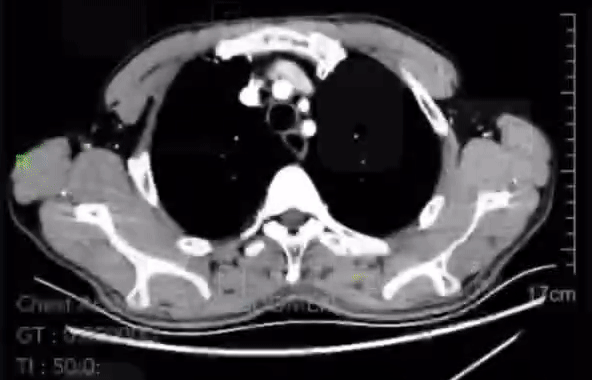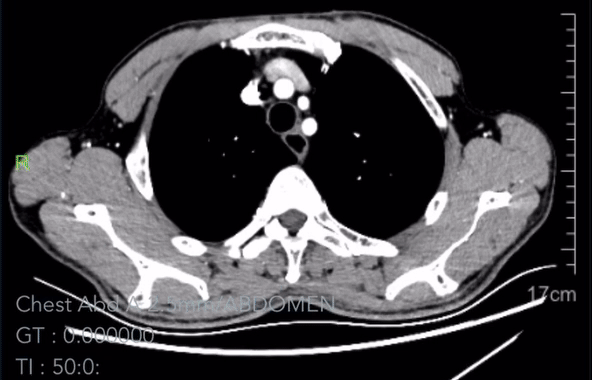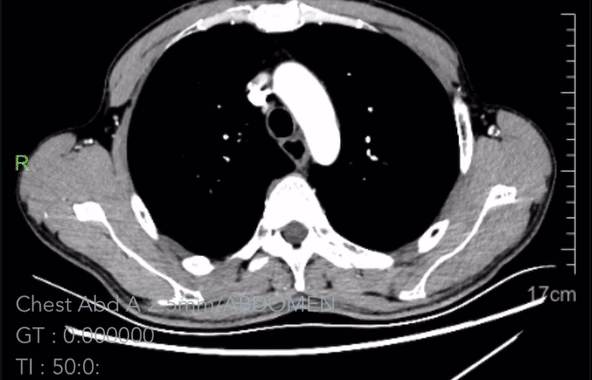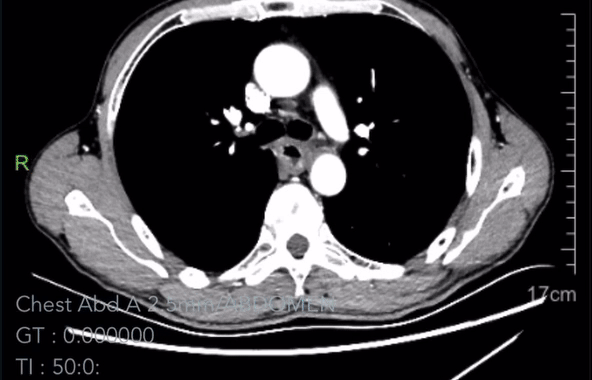
2023-02-18胸腹CT
三、 临床诊断
食管癌cT3N+MO IIIB期。
四、 治疗经过
l 新辅助治疗
考虑患者食管累及范围较长,分期属于局部晚期,建议新辅助化疗,查无禁忌,于2023-02-25、2023-03-18予患者斯鲁利单抗+白蛋白紫杉醇+奥沙利铂抗肿瘤治疗3周期。
术前复查CT评价CR
2023-04-17胸腹CT诊断:
1.食管癌复查,病灶显示不清,纵隔内多发增大淋巴结较前(2023-02-18)基本相仿,请结合临床。
2.右肺中叶支气管轻度扩张;左肺下叶支气管管腔内高密度吸收未见显示。
3.双肺新增多发斑片状灶、结节灶,炎症可能,建议复查。
4.左侧肾上腺结节状增粗较前基本相仿,请结合临床。
5.新增门静脉管径增宽,随诊复查。
6.新增盆腔积液。
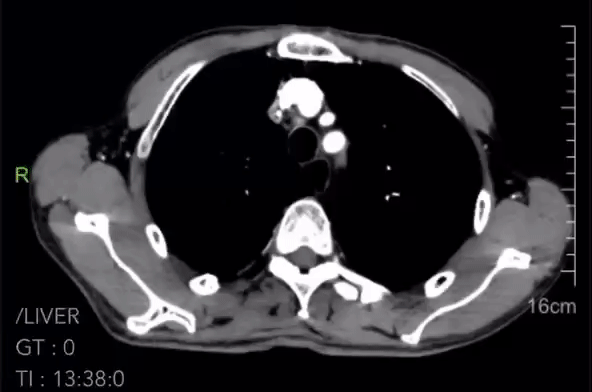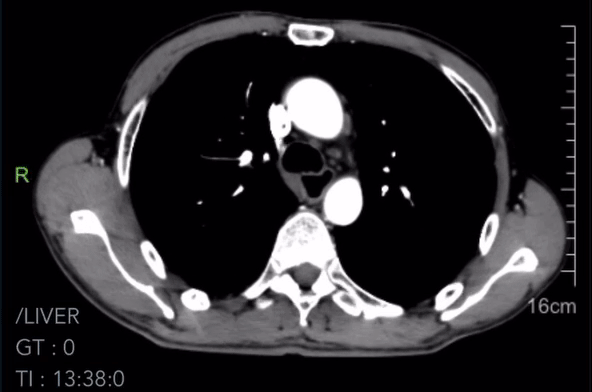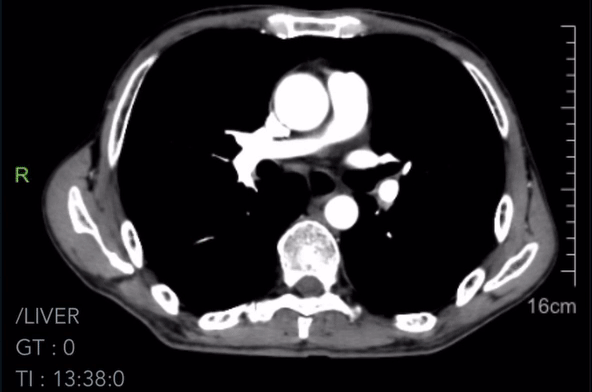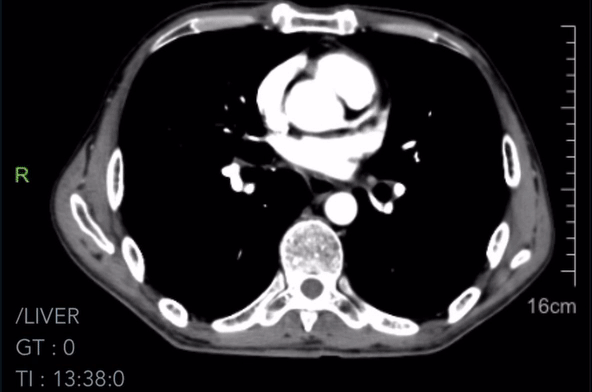
2023-04-17胸腹CT
l 手术治疗
手术治疗后病理PCR
给予斯鲁利单抗+白蛋白紫杉醇+奥沙利铂抗肿瘤治疗3周期后,复查CT评价CR,遂至胸外科手术,术后病理PCR,之后一直随访,病情未见复发,肿瘤标志物一直正常。
2023-05-13颈部超声示:
左侧颈部IV区可见数个低回声,皮髓质分界清,可见血流信号,较大者1.0cmx0.5cm。
右侧颈部及锁骨上窝未见明显异常肿大淋巴结。
2023-05-15上消化道造影示:
食管各段钡剂通过顺利,食管管壁柔软,蠕动良好,粘膜线完整连续,未见明显破坏征象。
胃张力中等,胃大、小弯轮廓光整,粘膜涂抹欠佳,略增粗,未见明显龛影和充盈缺损,胃壁柔软,蠕动良好,幽门开放自然,胃排空良好。
十二指肠球部充盈良好,降部及水平部粘膜无殊。
2023-05-19病理报告诊断:
(食管+部分胃+上切缘+淋巴结)
进行3次新辅助化疗+免疫抑制剂(斯鲁利单抗+白蛋白紫杉醇+奥沙利铂方案)抗肿瘤治疗后,原瘤床区域食管粘膜组织经充分取材,间质炎细胞浸润,未见明确肿瘤残留,未见明确脉管瘤栓及神经侵犯。符合治疗后改变。周围局灶粘膜及肌层见嗜酸性粒细胞浸润,伴鳞状上皮乳头状瘤样增生。食管两侧切缘、另送(上切缘)及胃粘膜上、下切缘未见特殊。
淋巴结未见癌转移:0/13(食管旁:0/5;胃壁:0/5;左喉返神经旁:0/2;隆突下:0/1)。
免疫组化结果:34BE12(+),CK5/6(+),Ki-67(局灶增殖指数高),P53(-),P63(+),P16(斑驳+)。
术后复查CT:
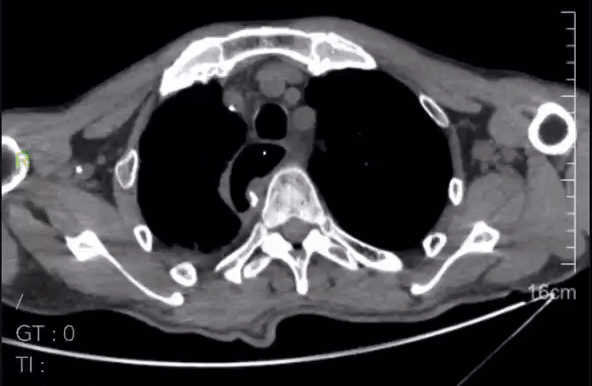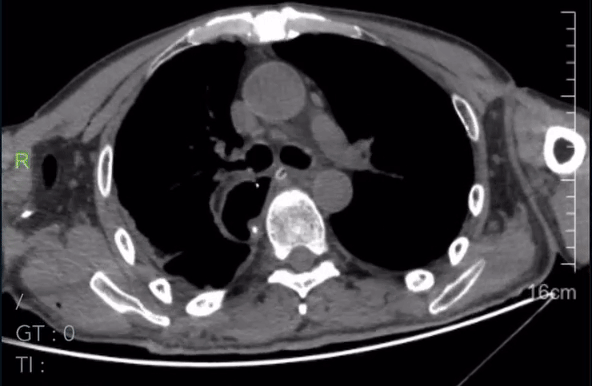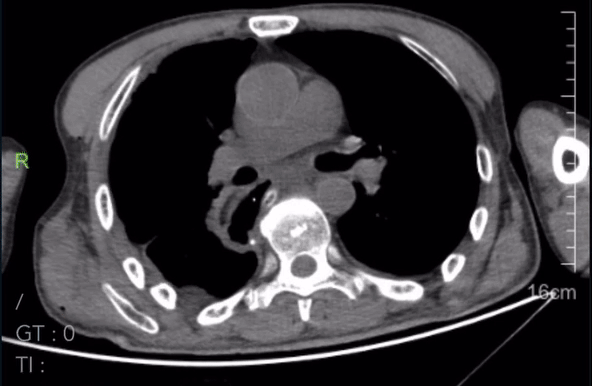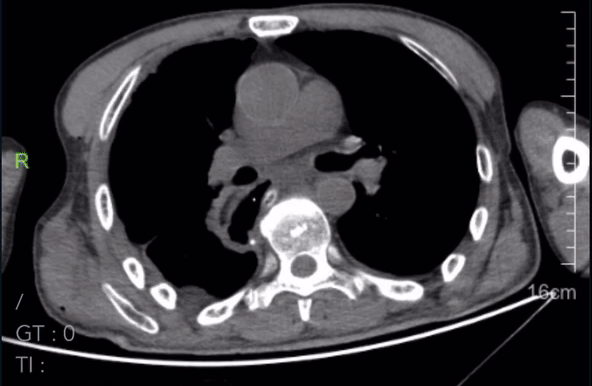
2023-05-22胸腹CT
术后3个月复查胸腹CT:
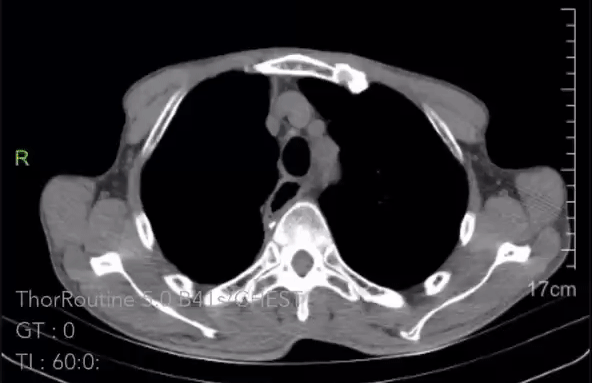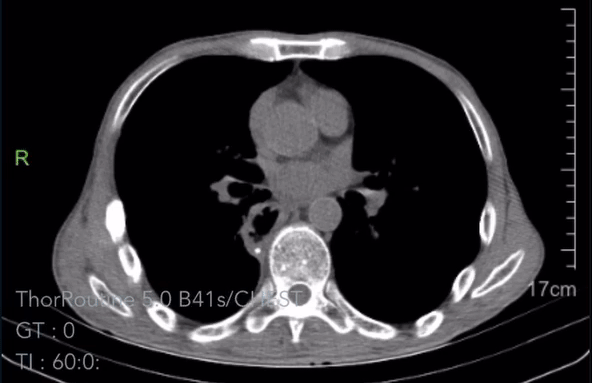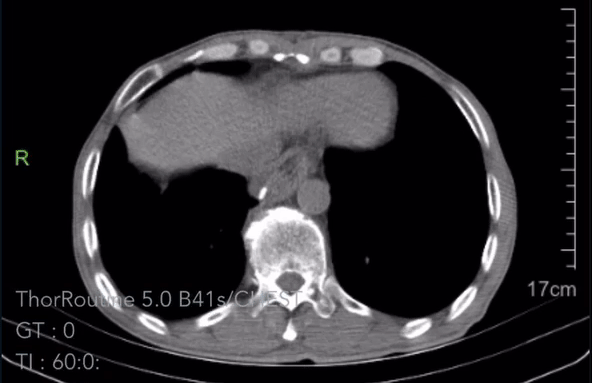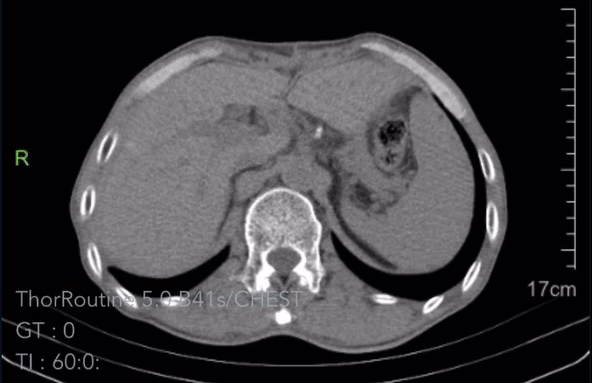
2023-08-02胸腹CT
治疗前与手术前CT对比:
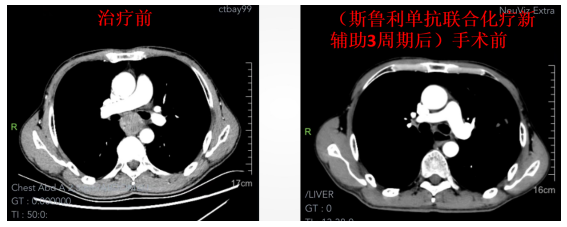
术后与术后3个月CT对比:
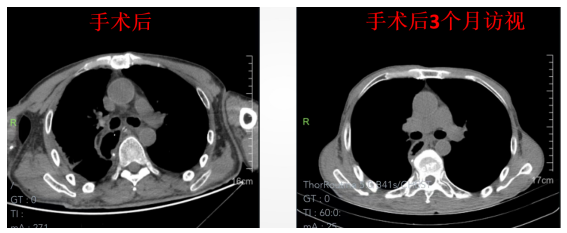
五、 病例小结
该病例为食管癌cT3N+MO IIIB期的局晚期患者。由于患者食管累及范围较长,分期属于局部晚期,因此先采取新辅助化疗联合免疫治疗(斯鲁利单抗+白蛋白紫杉醇+奥沙利铂)3个周期,术前复查CT评价CR。其后行手术治疗,术后病理PCR。术后CT及术后3个月复查CT均提示较前好转,且患者病情未见复发,肿瘤标志物一直正常。
讨论
本例食管癌患者分期属于局部晚期,对于这类局部晚期食管癌患者,国内外指南均推荐术前行新辅助治疗,。目前,已有高质量证据的荟萃分析结果显示,同单纯手术治疗相比,无论何种新辅助治疗模式(同步放化疗或单纯化疗)均显著改善了局部晚期/局部进展期食管癌患者术后的OS。
但新辅助放化疗或新辅助化疗的疗效依然有限。CROSS研究结果显示,在经历长达10年的随访后,与单纯手术相比,术前新辅助同步放化疗尽管显著延长了食管鳞状细胞癌患者的生存期,但另一方面,该研究的复发模式分析中,新辅助放化疗组经过10年随访,累计远处转移率仍高达40%,仅比单纯手术组的50%略有下降,而两组的累计局部复发率分别为21%和40%。此外,新辅助化疗在安全性方面仍不理想。
近年来,以 PD‑1/PD‑L1 免疫检查点抑制剂为代表的免疫治疗已经显著改善了晚期食管及食管胃交界部癌患者的长期预后,根据ASTRUM-007研究,斯鲁利单抗联合化疗一线治疗在晚期食管癌患者中,可显著延长总生存期和无进展生存期,同时斯鲁利单抗联合化疗的安全性良好。免疫治疗在晚期食管癌中所获得的肿瘤学疗效优势,已引发临床研究对局部晚期食管癌新辅助免疫治疗模式的探索,为了进一步提高局晚期食管癌患者的生存率,众多临床研究开启了新辅助免疫治疗的探索,且取得了良好的疗效,。
本案例经过3个周期的斯鲁利单抗联合化疗的新辅助治疗模式后,术前复查CT就实现了CR,随后行手术治疗还实现了PCR,该案例,斯鲁利单抗在局部晚期食管癌新辅助治疗的应用具有巨大潜力,能为局部晚期食管癌患者延长生存期带来新的希望。
目前,《中国可切除食管癌围手术期诊疗实践指南(2023版)》提到,包含PD‑1/PD‑L1免疫检查点抑制剂的方案是否适合用于术前新辅助治疗模式尚缺乏高级别循证医学证据,推荐在临床研究范畴内患者充分知情同意后开展1。这表明,新辅助免疫治疗是局部晚期食管癌患者一种潜在的治疗手段,期望未来有更多的临床研究能带来新辅助免疫治疗的好消息。
讲师介绍

任伟东个人简历
运城市中心医院肿瘤科主治医师
山西省抗癌协会多原发肿瘤专委会委员
山西省基层卫生协会肿瘤防治专委会委员
山西省医师协会免疫治疗专委会委员
山西省老年学会胸部肿瘤专委会委员
山西省老年学会热疗专委会委员
运城市医学会肿瘤学专委会秘书
参考文献:
1. 国家癌症中心, 中国医师协会胸外科医师分会, 中华医学会胸心血管外科学分会, 等. 中国可切除食管癌围手术期诊疗实践指南(2023版)[J]. 中华医学杂志, 2023, 103(33): 2552-2570.
2. Malik S, Sharma G, Sanaka MR, Thota PN. Role of endoscopic therapy in early esophageal cancer. World J Gastroenterol. 2018;24(35):3965-3973.
3. Reeh M, Nentwich MF, Asani S, et al. Locally advanced esophageal carcinoma: is there still a role of surgery alone without neoadjuvant treatment?. J Gastrointest Surg. 2015;19(4):587-593.
4. Yu S, Zhang W, Ni W, et al. A propensity-score matching analysis comparing long-term survival of surgery alone and postoperative treatment for patients in node positive or stage III esophageal squamous cell carcinoma after R0 esophagectomy. Radiother Oncol. 2019;140:159-166.
5. NCCN Guidelines Version 3.2023:Esophageal and Esophagogastric Junction Cancers.
6. 中国临床肿瘤学会(CSCO).食管癌诊疗指南2023.
7. Fan N, Wang Z, Zhou C, et al. Comparison of outcomes between neoadjuvant chemoradiotherapy and neoadjuvant chemotherapy in patients with locally advanced esophageal cancer: A network meta-analysis. EClinicalMedicine. 2021;42:101183.
8. Eyck BM, van Lanschot JJB, Hulshof MCCM, et al. Ten-Year Outcome of Neoadjuvant Chemoradiotherapy Plus Surgery for Esophageal Cancer: The Randomized Controlled CROSS Trial. J Clin Oncol. 2021;39(18):1995-2004.
9. 朱军格,李建彬,张英杰,食管癌新辅助治疗研究现状与进展[J].中华放射肿瘤学杂志,2022,31(04) : 389-394.
10. Song Y, Zhang B, Xin D, et al. First-line serplulimab or placebo plus chemotherapy in PD-L1-positive esophageal squamous cell carcinoma: a randomized, double-blind phase 3 trial. Nat Med. 2023;29(2):473-482.
11. Liu J , Li Z , X Fu, et al. 127P A prospective phase II clinical trial exploring neoadjuvant immunotherapy combined with chemotherapy in resectable thoracic esophageal squamous cell cancer (TESCC) with multi-station lymph node metastases (NICE study): Preliminary results. Annals of Oncology, 31.
12. Chen X, Xu X, Wang D, et al. Neoadjuvant sintilimab and chemotherapy in patients with potentially resectable esophageal squamous cell carcinoma (KEEP-G 03): an open-label, single-arm, phase 2 trial. J Immunother Cancer. 2023;11(2):e005830.


