Clin Cancer Res:许剑民/樊嘉/张玮/何川团队合作构建基于全基因组5hmc的结直肠癌及进展期腺瘤早筛模型
时间:2024-06-08 23:00:34 热度:37.1℃ 作者:网络
DNA甲基化(DNA methylation)是表观遗传领域中非常重要的研究方向,它能引起染色质结构、DNA构象、DNA稳定性及DNA与蛋白质相互作用方式的改变,从而控制基因表达,具有非常重要的生物学意义。5-甲基胞嘧啶(5-methylcytosine,5mC)是真核生物中最常见的DNA甲基化修饰。5mC羟甲基化生成的5-羟甲基胞嘧啶(5hmC)是5mC去甲基化过程中产生的重要的中间体。研究表明5hmC参与了染色体重新编程、基因表达调控、DNA损伤修复等重要生物学过程,其修饰的改变与肿瘤的发生、发展等密切相关。前期工作显示,外周血5hmC既有良好的组织指向性,又能在多种癌症及其它疾病的患者中呈现良好的早期诊断的生物指标性能。
5hmC-SEAL技术是美国人文与科学院院士、芝加哥大学何川教授团队发明的特异性富集含5hmC修饰的DNA片段的捕获技术。利用5hmC-SEAL技术,可以富集全基因组近2万个基因的含有5hmC修饰的DNA片段,进一步高通量测序分析可获得全基因组5hmC的分布及长度和丰度等信息。该技术具有特异性高、无序列偏好性、可进行通量研究等优点,适合用于肿瘤的探索与临床研究。
国际肿瘤研究领域著名杂志之一Clinical Cancer Research(2023年度影响因子11.5)近日发表了一篇题为《A 5-hydroxymethycytosine-based non-invasive model for early detection of colorectal carcinomas and advanced adenomas: the METHOD-2 study》的论文。该研究由复旦大学附属中山医院樊嘉院士、许剑民教授,美国西北大学张玮教授,美国芝加哥大学何川教授团队联合柏锘(上海)医疗科技有限公司、301医院、浙江大学医学院附属第二医院、长海医院、厦门大学附属第一医院等单位合作完成。

结直肠癌是全世界范围内第三常见的癌症,在中国尤其值得关注的是,其年新发病率从1990年的约10万,攀升至2015年的40万,到2020年已占到全球病例的约四分之一。癌症分期是决定结直肠癌预后的最重要因素,早期还未发生转移的病人,其五年期生存率在90%左右,但对于中后期已发生转移的结直肠癌病人,其五年期生存率则降至14%。肠镜筛查目前仍然是发现确诊结直肠癌或者进展期腺瘤的“金标准”,但由于其侵入式的特点,可能引起筛查对象的不适,而且也有可能发生出血、肠穿孔、心脑血管意外等副作用,所以依从性较低;而CEA、CA199等血清标志物,其灵敏度和特异性又有限。之前的研究已经表明,5hmC位点主要分布在基因活跃区域,其丰度变化可以潜在地用于结直肠癌以及早期腺瘤的筛查、诊断,而且检测来自血浆中游离DNA(cfDNA)的5hmC水平便捷、无创,有利于在还有较多治疗手段可供选择的结直肠癌发病早期将其检出。
该研究中,研究人员采集了2576例cfDNA,其中包含来自2019年1月至2020年1月在8家参与医院就诊的1074名结直肠癌(CRC)患者、356名进展期腺瘤(ADA)患者,80名其它癌种(肝癌、胃癌、食管癌和肺癌)患者及1066名对照,对这些样本进行了全基因组5hmC水平的分析(实验设计如图1所示)。其中,来自上海及浙江地区四家医院的样本(含664例I至III期结直肠癌,144例四期或者分期不明结直肠癌,246例腺瘤,960例对照)作为训练及内部验证集,来自国内另外4家医院的样本(266例结直肠癌,110例腺瘤,106例对照)作为外部验证集。
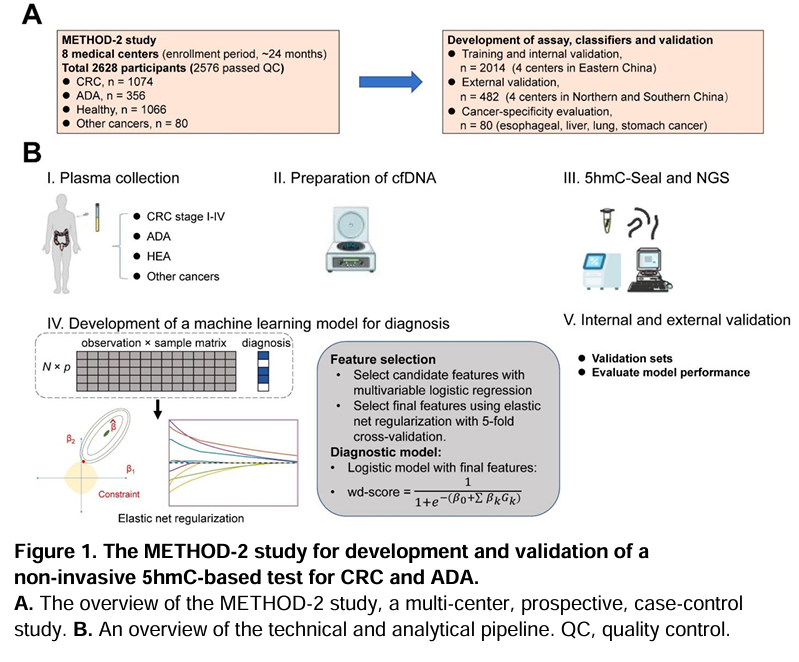
图1 实验设计图
排除了年龄、性别因素的差异后,训练集中共得到1391个在I-III期结直肠癌/腺瘤和健康对照有显著差异(p<0.01)的基因区域,经过逻辑回归和弹性网络归一化处理之后,得到由96个基因组成的模型。由这些基因组成的模型可以较好地区分健康对照和肠癌I-III期及腺瘤患者,在训练集、内部验证集和外部验证集的曲线下面积(AUC)分别为94.6%,92.6%和87.2%(图2A),也能分别较好地区分健康对照和肠癌I-III期(图2B,AUC分别为95.6%,94.3%和90.7%),以及健康对照和腺瘤患者(图2C,AUC分别为91.8%,87.9%和78.6%),均高于单独使用这些基因的区分能力(AUC一般在52.0%到65.2%之间)。而且,从健康到腺瘤再到肠癌患者,基于5hmC基因模型的判分呈现出逐步升高的趋势,这在训练集、内部验证集和外部验证集中都表现得很明显(图2D)。
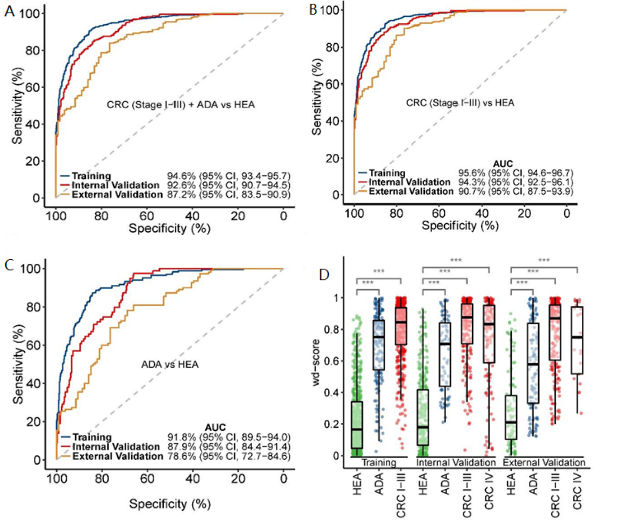
图2 由96个基因组成的模型可以较好地区分健康人和肠癌I-III期及腺瘤患者
与基于5hmC的基因模型相比,传统血清标志物CEA区分健康人和肠癌I-III期患者的能力明显稍逊一筹,其在训练集、内部验证集和外部验证集的AUC分别为78.0%,77.1%和73.2%(图3A)。基于5hmC的基因模型,无论是从AUC来看,还是根据90%特异性下的灵敏度来看,正确识别腺瘤和肠癌I-III期患者的能力都优于CEA(图3C, 3D)。尤其需要指出的是,基于5hmC的基因模型可以纠正单独使用CEA被错判的案例,如图3B所示,内部验证集中215例肠癌I-III期患者,其中145例(67.4%,图3B中第二、三象限)因为CEA值小于5ng/mL的标准阈值而被错判,但基于5hmC的基因模型能够正确判别其中的124例(57.7%,图3B中第二象限),因此大大提高检测的灵敏度。
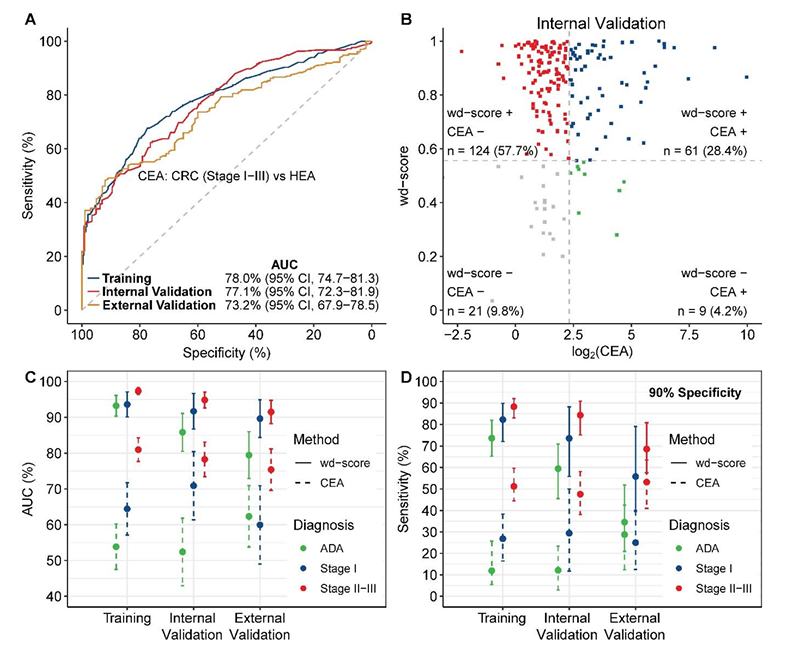
图3 基于5hmc检测的预测模型表现好于传统血清标志物CEA
对1391个在I-III期结直肠癌/腺瘤和健康对照有显著差异的基因区域进行功能注释,发现其中富集了多个与癌症相关的KEGG代谢通路,例如神经活性配体-受体相互作用,钙离子、MAPK、cAMP信号通路等(图4A)。共修饰分析发现六组互作/共修饰模块(图4B),这些模块中涉及到的诸多基因和结直肠癌的发病机理和转移相关,例如模块M2中的GJA1基因(编码间隙连接蛋白α-1,图4C,4D)不但是得到的96基因模型之一,而且有文献报道表明和结直肠癌免疫浸润相关,是表征结直肠癌预后的生物标志物之一。
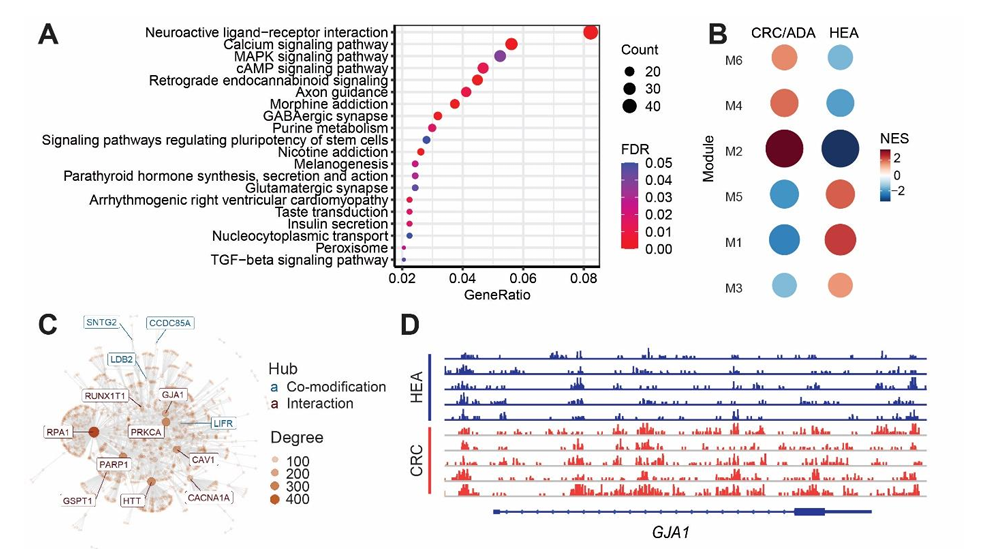
图4 差异基因的功能分析
同为无创检测,美国一项研究表明基于血液的检测,相比粪便检测更容易被人接受。而市面上多款仅限于Sept9基因甲基化的血清检测,其检出结直肠癌的灵敏度只有约48%,检出腺瘤的能力则更低,只有21%的灵敏度和79%的特异性。基于血液cfDNA进行全基因组5hmC水平检测,其检出结直肠癌和进展期腺瘤的灵敏度优于CEA等目前常用的各种标志物,而且由于其无创的特点,可以更加方便地加以推广,从而有助于在结直肠癌尚可通过手术切除的发展早期被及时发现,因此具有很好的研究和临床应该前景。
论文原文:
Chang W, Zhang Z, Jia B, Ding KF, Pan Z, Su G, Zhang W, Liu T, Zhong Y, He G, Ren L, Wei Y, Li D, Cui X, Yang J, Shi Y, Bissonnette M, He C, Zhang W, Fan J, Xu J. A 5-hydroxymethylcytosine-based non-invasive model for early detection of colorectal carcinomas and advanced adenomas: the METHOD-2 study. Clin Cancer Res. 2024 May 30. doi: 10.1158/1078-0432.CCR-24-0199. Epub ahead of print. PMID: 38814264.
https://doi.org/10.1158/1078-0432.CCR-24-0199


