Schizophrenia | 中国学者发文:苯环利定诱导精神分裂症样动物模型及其潜在神经机制研究进展
时间:2024-07-29 10:00:44 热度:37.1℃ 作者:网络
精神分裂症(SZ)是一种慢性、严重的精神障碍,具有异质性临床表现和未知病因。SZ的研究长期以来受到动物模型可靠性低和病理机制不明确的限制。苯环利定(PCP),一种非竞争性N-甲基-D-天冬氨酸受体(NMDAR)拮抗剂,能够迅速诱导啮齿动物产生SZ的正性和负性症状以及稳定的认知障碍。然而,PCP诱导的SZ样症状背后的神经机制尚未完全明了。非多巴胺病理生理学,特别是NMDAR功能低下引起的前额叶皮质(PFC)中过量的谷氨酸释放,可能在PCP诱导的SZ样症状发展中起关键作用。

本综述总结了PCP对行为和代谢的影响以及PCP在PFC和海马(HIP)中的细胞和回路靶点。研究发现,PCP主要靶向腹侧海马-前额叶皮质(vHIP-PFC)通路,而非PFC-腹侧被盖区(VTA)通路和丘脑皮质通路。系统性PCP给药可能优先抑制vHIP中的γ-氨基丁酸(GABA)神经元,进而导致海马锥体细胞去抑制。来自海马的兴奋性输入可能触发持续、过度和病理性的PFC锥体神经元激活,从而介导各种SZ样症状。此外,在PCP诱导的SZ模型中,观察到皮质或海马中的星形胶质细胞和小胶质细胞激活及氧化应激。这些发现完善了精神分裂症的低谷氨酸假说。
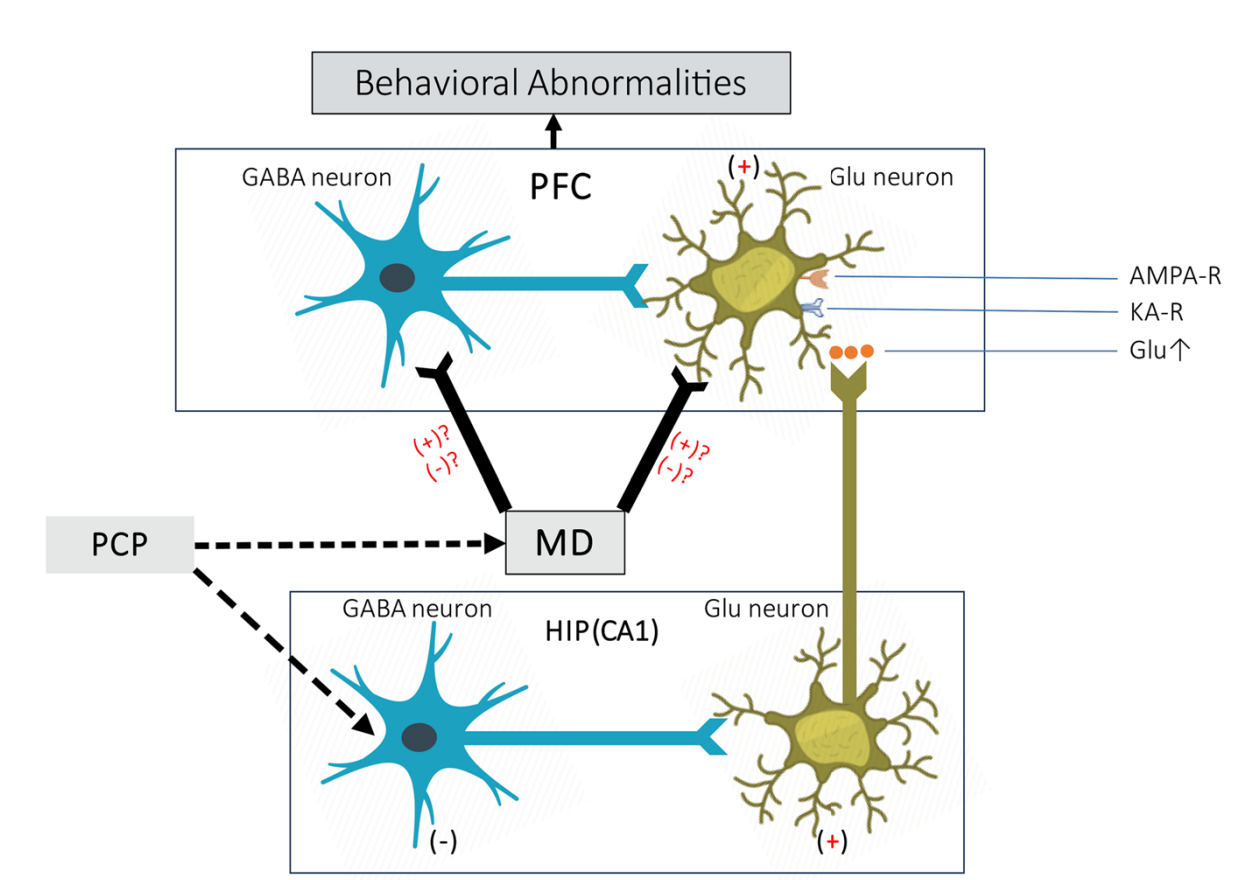
图1.腹侧海马有密集的谷氨酸能投射到PFC
实验动物研究表明,慢性和重复低剂量PCP给药在啮齿动物大脑中产生的特定代谢和神经化学变化与SZ患者大脑中的变化惊人地相似。单次腹腔注射PCP增加了大鼠内侧前额叶皮质(mPFC)中的谷氨酸、多巴胺、5-羟色胺(5-HT)和去甲肾上腺素水平,并降低了γ-氨基丁酸(GABA)的细胞外浓度,而在几个其他脑区,PCP给药后多巴胺水平升高。谷氨酸受体激动剂可以抑制上述PCP诱导的变化,并阻断PCP诱导的运动增加。与此一致,MK801的急性系统给药也增加了啮齿动物前额叶皮质中多种神经递质的释放,包括谷氨酸、多巴胺、5-HT和乙酰胆碱。PFC中过量的谷氨酸释放可能是由NMDAR功能低下引起的,并在PCP诱导的SZ样症状的发展中起关键作用,而PCP诱导的NMDAR功能低下也被认为与SZ中的认知障碍有关。
在PCP处理的小鼠中,PFC和海马中的脑源性神经营养因子(BDNF)水平和磷酸化TrkB(p-TrkB)与TrkB的比率下降,并伴有认知障碍。(R)-氯胺酮可以通过激活大脑中的BDNF-TrkB信号通路改善PCP诱导的认知障碍。此外,周围BDNF水平与SZ患者的认知障碍之间存在关联。PCP增加了动物PFC和腹侧海马(vHIP)中的NO水平,表明NO似乎是SZ中的关键信号分子。在亚慢性苯环利定(scPCP)处理的小鼠中,PFC和vHIP中标记为副伽马蛋白的抑制性中间神经元数量和PSD95水平显著减少,而纹状体中的多糖神经细胞黏附分子(PSA-NCAM)水平显著降低。在PCP诱导的SZ样小鼠模型中,PFC中观察到增强的炎症和氧化应激。
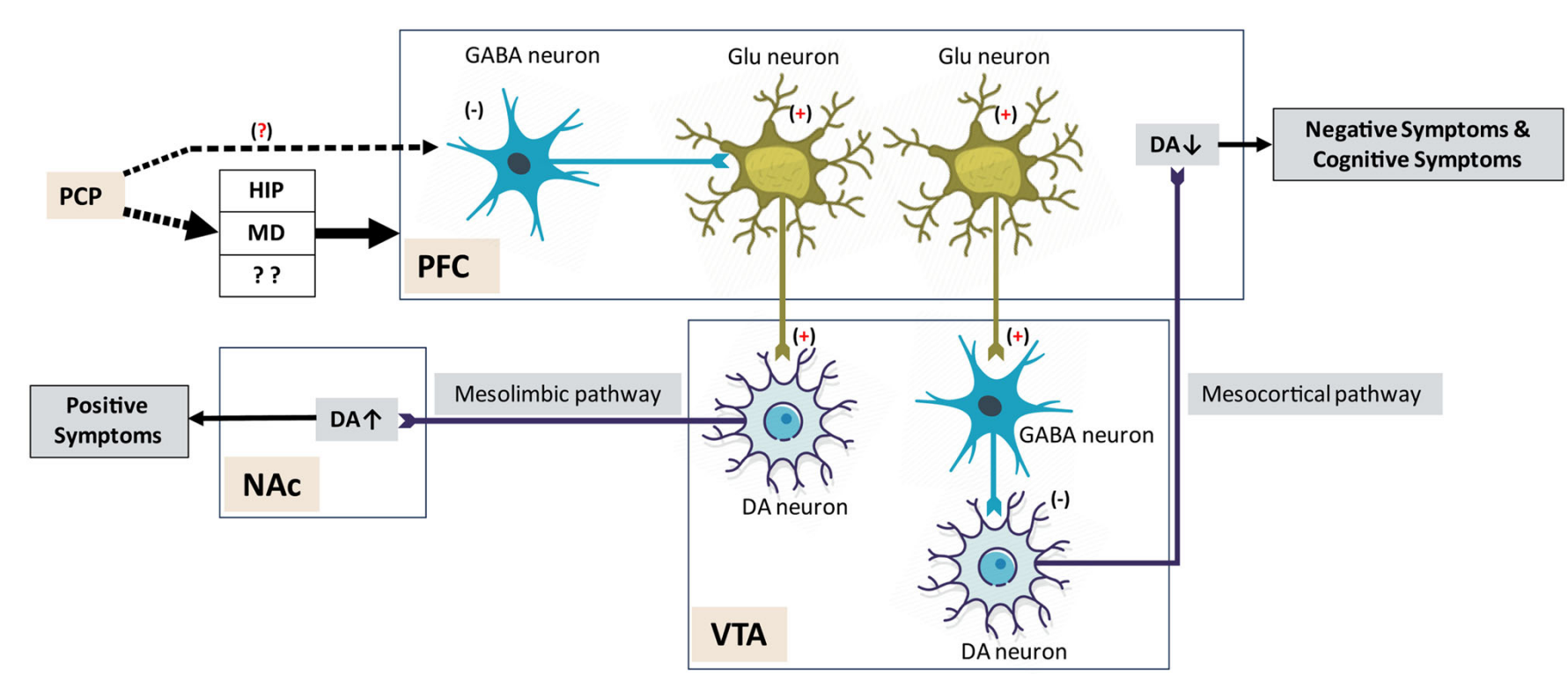
图2.PCP作用于PFC-VTA通路
PCP诱导的SZ样动物模型被认为是SZ的最可靠药理模型。与遗传或神经发育模型相比,PCP模型更简单、廉价且更易于复制。系统性PCP给药引起的行为异常可能是通过外部脑区对mPFC神经元的兴奋性输入介导的。这些发现支持NMDAR功能低下参与SZ药理模型的假设,即通过诱导腹侧海马-前额叶皮质投射的过度和病理性兴奋,PCP可能导致SZ相关症状。此外,星形胶质细胞和小胶质细胞作为PCP的靶点可能也会直接或间接影响vHIP-PFC通路的正常功能,从而促成PCP诱导的SZ样行为。
原始出处:
Dabing Li, Qiangwen Pan, Yewei Xiao, Kehui Hu. Schizophrenia (2024) 10:65. DOI: 10.1038/s41537-024-00485-x.


