Meta分析|经治慢性乙型肝炎患者低病毒血症发生率和影响因素
时间:2024-08-05 15:00:42 热度:37.1℃ 作者:网络
据世界卫生组织估计,2019年慢性HBV感染者有2.96亿,因乙型肝炎相关肝硬化和癌症死亡人数82万。尽管疫苗接种和预防支持降低了HBV感染发病率,但每年仍有150万新发HBV感染者。我国一般人群HBsAg流行率约为6.89%,慢性HBV感染者超过8 000万例。血清HBV DNA病毒载量是影响预后的重要因素,最大限度地长期抑制HBV复制,减轻肝细胞炎症坏死及肝纤维化,延缓和减少相关并发症,改善患者生命质量,延长其生存时间是慢性乙型肝炎(CHB)抗病毒治疗的目标。恩替卡韦(ETV)、富马酸替诺福韦酯(TDF)和富马酸丙酚替诺福韦(TAF)因其抗病毒作用强、耐药性低、副作用小等优势已作为一线用药在临床广泛应用。经过48周的抗病毒治疗,50%~80%的患者可以实现完全病毒学应答,但仍有10%~45%的患者存在持续或间歇低病毒血症(LLV)。LLV是指排除依从性问题及病毒耐药突变,经过48周规范一线抗病毒药物治疗后,使用灵敏qPCR法(检测下限为20 IU/mL或10 IU/mL)仍可检测到,但<2 000 IU/mL。研究表明,持续的低病毒载量可以加速肝纤维化进程,是肝细胞癌发生及复发的危险因素。因此,了解CHB患者LLV发生率及其影响因素,是减少并发症发生,改善患者预后,提高生存质量,进一步针对患者制订个体化治疗方案的重要环节,对实现“2030计划”消除病毒性肝炎损害的目标具有重要意义。证据是临床决策的核心,高质量的证据能为临床工作者提供有价值的参考。但是,目前关于CHB患者LLV发生率及影响因素的报告证据分散,且差异性较大,不利于指导临床决策。故本研究旨在通过Meta分析的方法将现有临床证据进行定量分析,对经治CHB患者LLV的发生率及影响因素进行探讨,综合现有证据,为优化个性化治疗方案、有效干预和预防LLV的发生提供循证医学证据。
1资料与方法
1.1 规程与注册
本研究根据PRISMA指南完成,PROSPERO注册号:CRD42023455304。
1.2 检索策略
计算机检索中国知网、万方数据库、维普网、中国生物医学文献服务系统、PubMed、Embase、Web of Science、Cochrane Library数据库。检索时间为建库至2023年7月21日。检索方式为主题词和自由词相结合。中文检索词为“乙肝”“乙型肝炎”“乙型病毒性肝炎”“慢乙肝”“慢性乙型肝炎”“慢性乙型病毒性肝炎”“低病毒血症”“低病毒载量”“影响因素”“危险因素”。英文检索词为“hepatitis B”“low level viremia”“hypoviremia”“risk factor”“influencing factor”。
1.3 文献纳入与排除标准
1.3.1 纳入标准
(1)研究类型:队列研究、横断面研究和病例对照研究;(2)研究地点为中国,研究对象为中国人群,符合乙型肝炎诊断标准且抗病毒疗程至少为48周;(3)研究结局为LLV的发生;(4)语言限定为中、英文文献。
1.3.2 排除标准
(1)研究对象合并其他任意疾病(如艾滋病、丙型肝炎、肝癌等);(2)综述类文献;(3)数据无法提取;(4)无法获取全文的文献;(5)重复发表文献。
1.4 文献筛选及数据提取
由两名研究者严格按照检索策略和纳排标准独立进行文献检索、文献筛选及数据提取。主要提取内容包括:第一作者、发表年份、研究类型、研究地点、地理区域、样本量、LLV发生例数、多因素分析中的影响因素等。如遇分歧,由两名研究者讨论决定,协商不一致时,由第三名研究者决定。
1.5 文献质量评价
对纳入文献进行质量评价。队列研究和病例对照研究使用纽卡斯尔-渥太华质量评估量表进行评价,评分0~3分为低质量文献,4~6分为中等质量文献,7~9分为较高质量文献;横断面研究使用美国卫生保健质量和研究机构评价量表进行评价,条目中“是”计1分,“否”或“不清楚”计0分,总分0~3分为低质量文献,4~7分为中等质量文献,8~11分为高质量文献。文献质量评价亦由两名研究者独立进行,如遇分歧讨论决定,不能统一时由第三方决定。
1.6 统计学方法
应用Stata 16.0软件进行Meta分析。影响因素采用比值比(OR)及95%可信区间(95%CI)合并效应量。采用Q检验及I2统计量评估纳入研究的异质性大小,若I2≤50%、P≥0.10,提示各研究间无明显异质性,采用固定效应模型进行Meta分析;若I2>50%、P<0.10,提示各研究间异质性较大,采用随机效应模型进行Meta分析,并通过亚组分析、敏感性分析以寻找异质性来源。当影响因素研究数量低于2篇或数据不能进行合并时,对结果进行描述性分析。将纳入文献数量≥10篇的研究结果使用Egger’s检验和Begg’s检验进行发表偏倚评估,并绘制漏斗图。P<0.05为差异有统计学意义。
2结果
2.1 文献检索结果
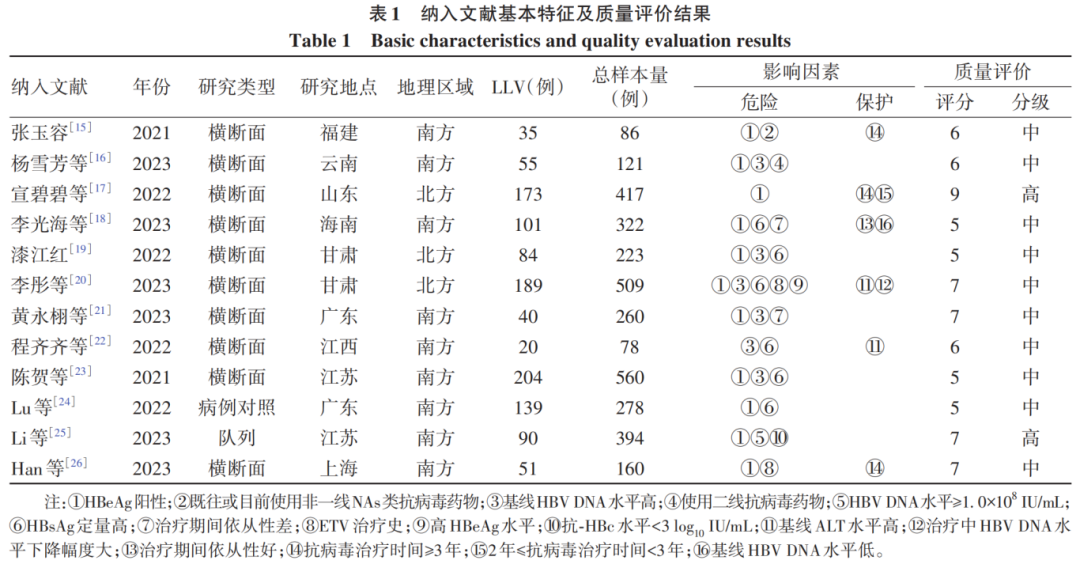
初步检索共获得文献449篇,经过文献筛选后,最终纳入文献12篇,文献筛选流程见图1。总样本量3 408例,包括LLV患者1 181例。4篇为高质量文献,余8篇为中等质量文献。12篇文献共提取HBeAg阳性、既往或目前使用非一线核苷(酸)类似物(NAs)抗病毒药、高基线HBV DNA水平等16个影响因素,结果见表1。
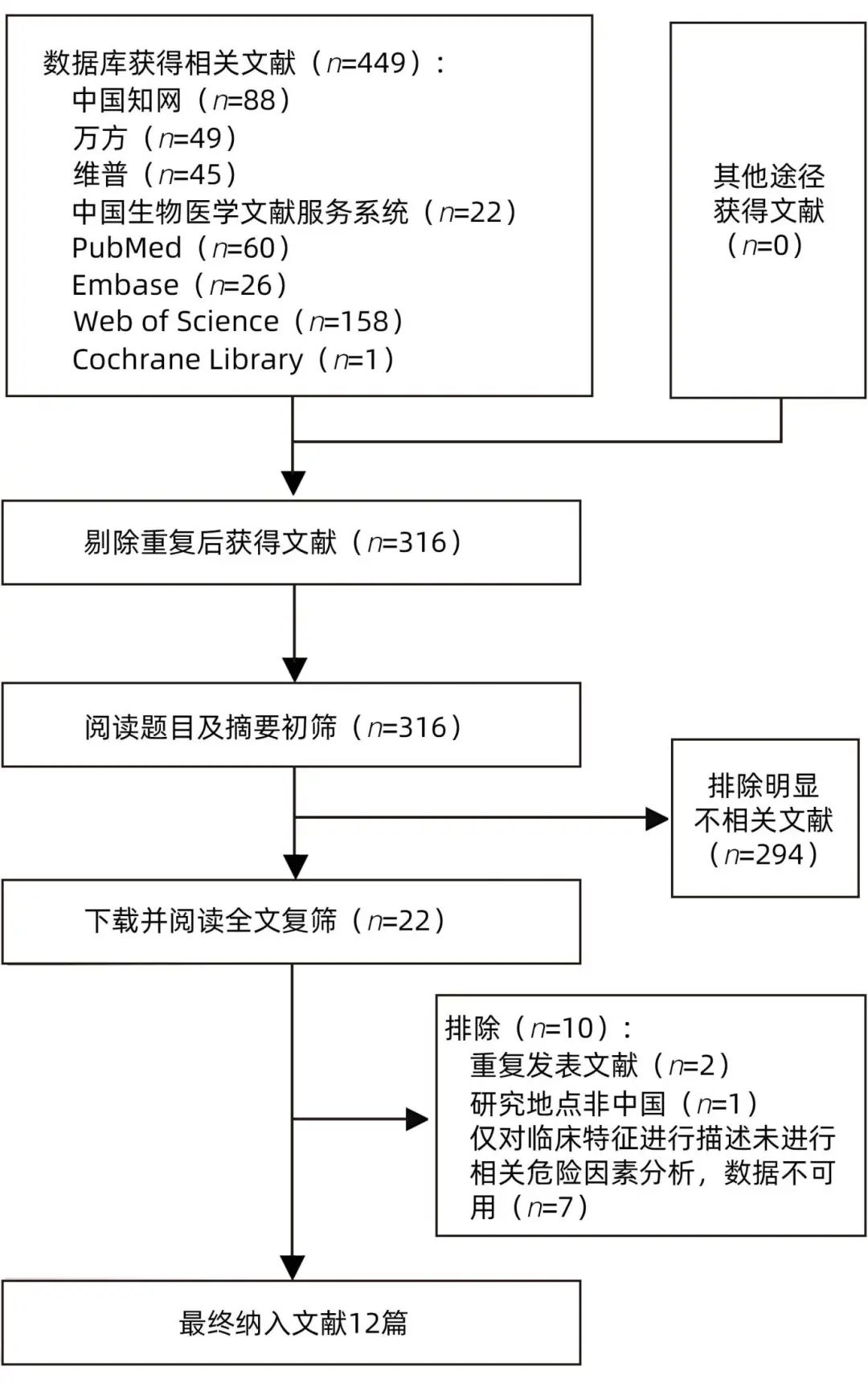
图1 文献筛选流程
2.2 LLV发生率的Meta分析
2.2.1 发病率
11篇文献对LLV发生率进行了研究。异质性检验显示各研究间存在明显异质性(I2=89.931%,P<0.001),故采用随机效应模型分析。结果显示,中国CHB患者LLV的发生率为32.8%(95%CI:27.6%~38.3%)(图2)。
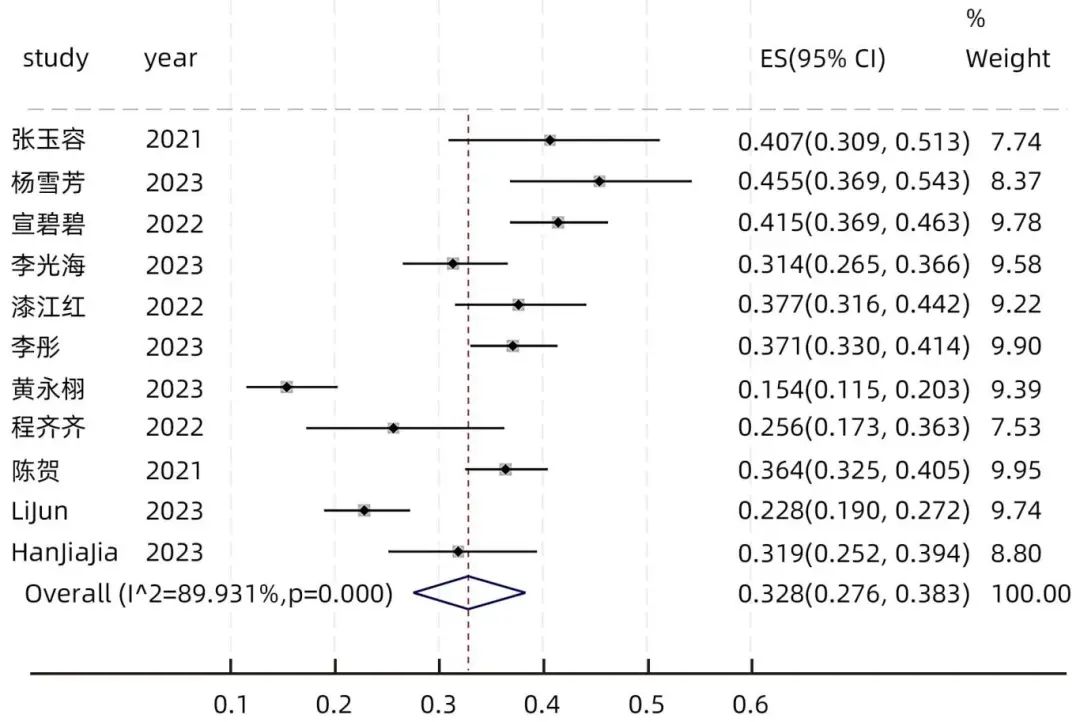
图2 LLV发生率的Meta分析森林图
2.2.2 亚组分析
将纳入研究按照研究地理区域(南方/北方)进行亚组分析。结果显示,南方和北方CHB患者LLV发生率分别为38.8%(95%CI:36.0%~41.6%)、28.4%(26.4%~30.3%)(表2)。
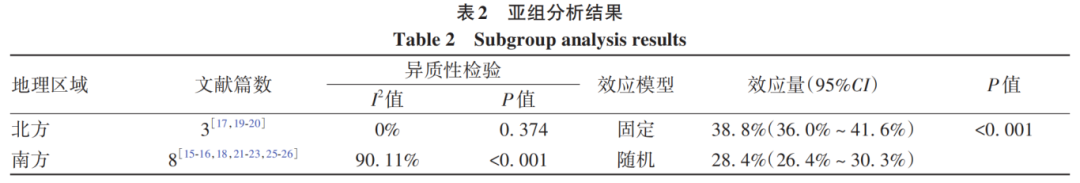
2.2.3 敏感性分析
对总发生率采用逐一剔除法进行敏感性分析,结果显示逐个剔除后合并效应值未发生明显变化,结果相对稳定。敏感性分析结果见图3。
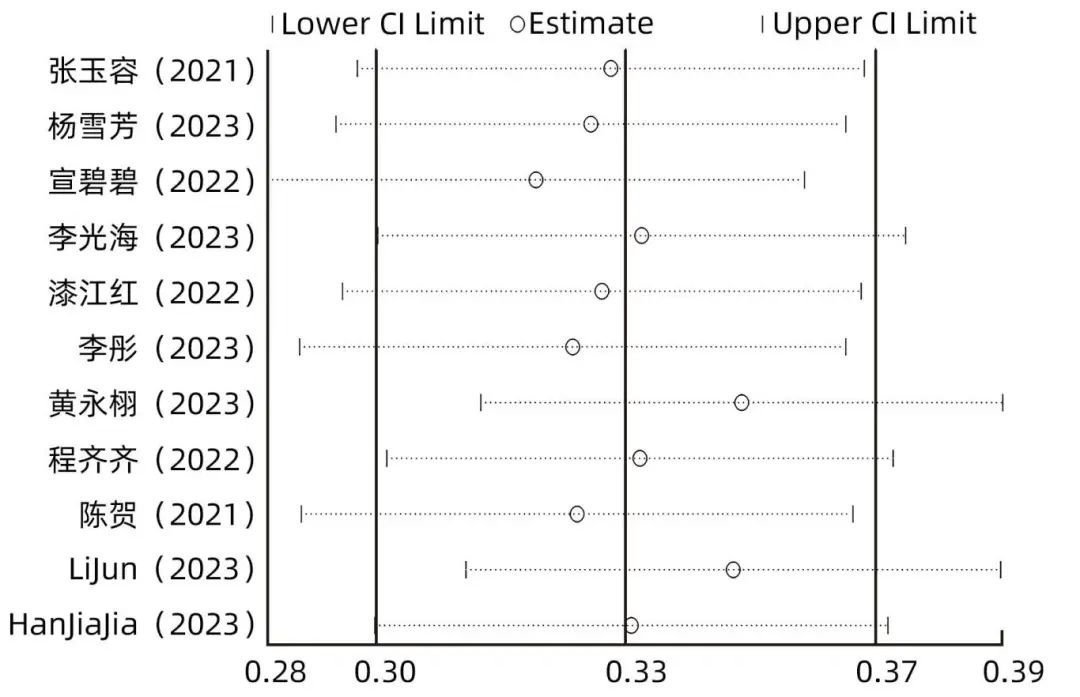
图3 LLV发病率敏感性分析结果
2.2.4 发表偏倚
采用Egger’s检验和Begg’s检验对纳入的11篇文献中CHB患者LLV发生率的发表偏倚进行评估并绘制漏斗图(图4)。Egger’s检验(P=0.498)和Begg’s检验(P=0.755)结果提示发表偏倚较低。
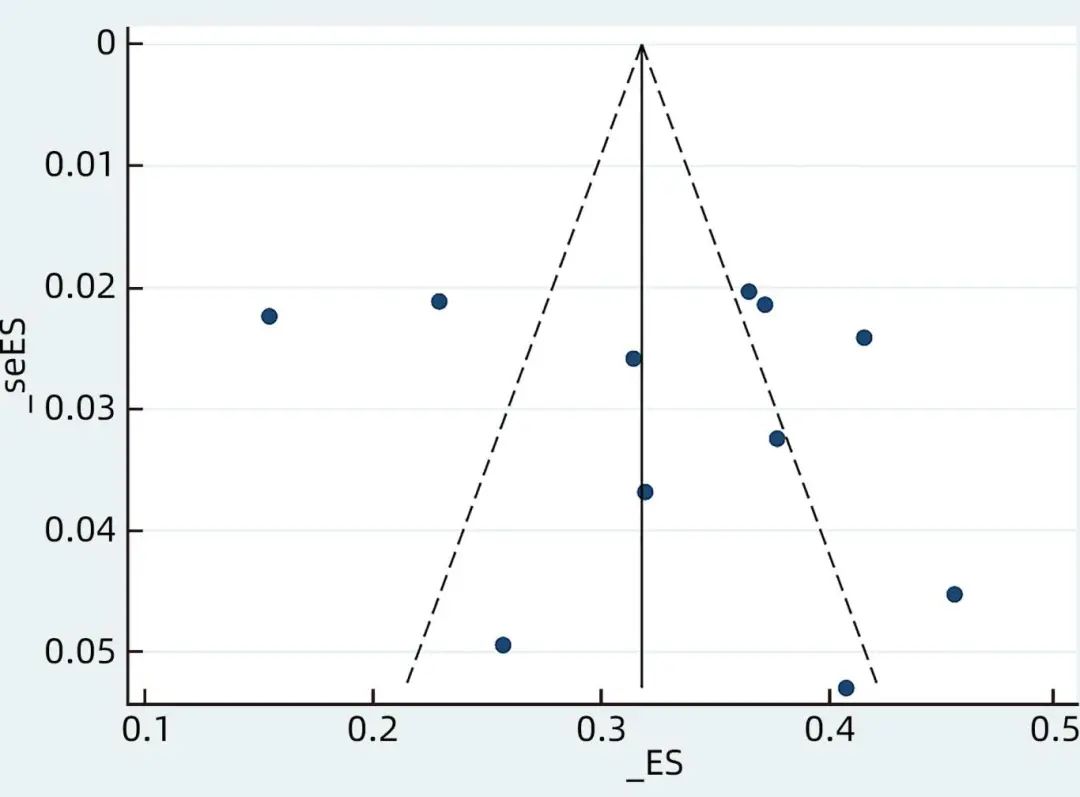
图4 LLV发生率Meta分析的漏斗图
2.3 LLV影响因素的Meta分析
2.3.1 影响因素
对纳入的12篇文献进行影响因素的Meta分析。提取出可以进行效应量合并分析的影响因素共6个,各研究结果之间无明显异质性,故选择固定效应模型进行分析。结果显示,HBeAg阳性(OR=3.258)、基线HBV DNA水平高(OR=1.286)、高HBsAg定量水平(OR=2.107)和有ETV治疗史(OR=3.089)是经治CHB患者发生LLV的危险因素(P值均<0.001);高基线ALT水平(OR=0.985)和抗病毒治疗疗程≥3年(OR=0.175)是LLV发生的保护因素(P值均<0.001)(表3)。
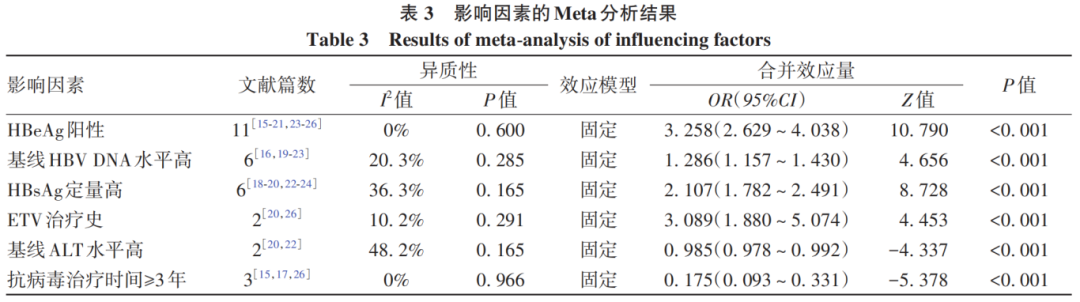
2.3.2 描述性分析
将纳入文献中不能够进行合并的影响因素进行描述性分析。张玉荣研究显示,既往或目前使用非一线NAs类抗病毒药是经治CHB患者LLV发生的危险因素(OR=7.38,95%CI:2.15~25.34,P=0.001)。杨雪芳等研究发现使用二线药物进行抗病毒治疗是LLV发生的危险因素(OR=14.982,95%CI:1.390~161.506,P=0.026)。Li等研究发现HBV DNA水平>1.0×108 IU/mL(OR=2.871,95%CI:1.563~5.272,P<0.001)、抗-HBc水平<3 log10 IU/mL(OR=2.384,95%CI:1.223~4.645,P=0.011)是LLV发生的危险因素。黄永栩等研究发现治疗期间依从性差是LLV发生的危险因素(OR=2.927,95%CI:1.078~7.949,P=0.035)。李彤等研究发现高HBeAg水平是LLV发生的危险因素(OR=1.001,95%CI:1.000~1.002,P<0.05)。
关于保护因素,李光海等研究发现治疗期间依从性好(OR=0.241,95%CI:0.114~0.510,P=0.001)、基线HBV DNA水平低(OR=0.445,95%CI:0.323~0.614,P<0.001)是发生LLV的保护因素。宣碧碧等研究发现2年≤抗病毒治疗疗程<3年是LLV发生的保护因素(OR=0.175,95%CI:0.046~0.674,P=0.01)。李彤等研究发现,抗病毒治疗中HBV DNA载量下降幅度大是LLV发生的保护因素(OR=0.205,95%CI:0.147~0.287,P<0.05)。
2.3.3 敏感性分析
将CHB患者LLV发生的影响因素中HBeAg阳性、高基线HBV DNA水平、HBsAg定量高、抗病毒治疗时间≥3年的合并结果通过逐一剔除法进行敏感性分析,结果显示效应值未发生明显变化,提示研究结果较稳定。余影响因素纳入文献≤2篇,未进行敏感性分析。
2.3.4 发表偏倚
对影响因素中的HBeAg阳性进行发表偏倚分析,漏斗图见图5。Egger’s检验(P=0.130)和Begg’s检验(P=0.371)结果提示不存在明显发表偏倚。其余15个影响因素因纳入的文献数量均低于10篇,故未对影响因素的发表偏倚进行分析。
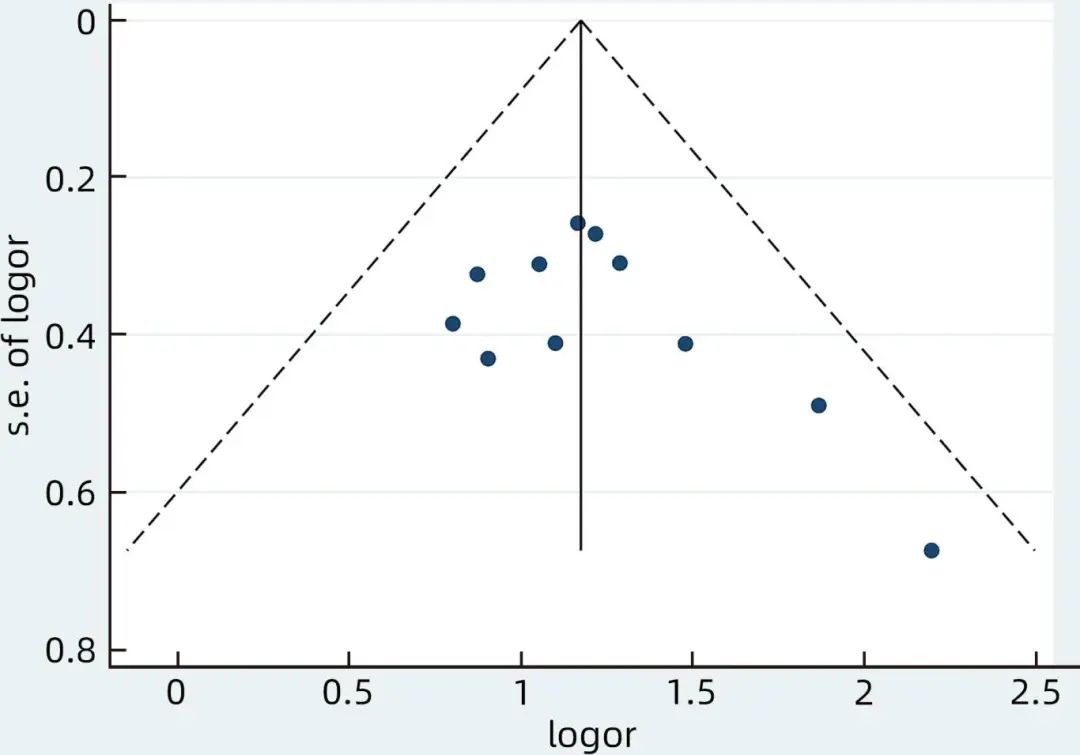
图5 HBeAg阳性Meta分析的漏斗图
3讨论
本研究结果显示,我国经治CHB患者LLV的发生率合并值为32.8%(95%CI:27.6%~38.3%),高于韩国一项回顾性研究报道的26.8%及意大利研究报道的20%。亚组分析发现,我国北方LLV发生率高于南方地区。这可能与南北方经济发展差异、受教育程度及对疾病认识和治疗程度的差异有关。由于本研究纳入文献数量较少,可能存在选择偏倚,需要高质量、大样本的流行病学调查加以验证。
本研究分析结果提示,HBsAg定量高、HBeAg阳性及高HBeAg水平、抗-HBc水平<3 log10 IU/mL、高基线HBV DNA水平(或HBV DNA水平≥1.0×108 IU/mL)、既往或目前使用非一线NAs类抗病毒药(使用二线药物抗病毒治疗)、有ETV治疗史可能是影响LLV发生的危险因素。
HBsAg是HBV感染的血清学标志。HBsAg定量能反映疾病进展、肝细胞核内共价闭合环状DNA(cccDNA)转录水平、HBV DNA复制情况,是监测或预测抗病毒治疗的有效标志物。卢建华等研究发现,患者HBsAg定量与HBV复制程度之间具有相关性,随着HBsAg定量的增高,HBV DNA的表达量增加,HBeAg阳性率也在不断增高。HBeAg是一种由HBV前核基因编码的非结构蛋白,由肝细胞修饰和分泌。通常HBeAg阳性是病毒复制活跃、传染性强的标志。张晓晶等发现与HBeAg阴性患者相比,HBeAg阳性患者HBV RNA表达水平、HBV DNA阳性率及肝功能异常率均更高,提示HBeAg阳性患者肝细胞内cccDNA转录活性更高,病毒复制活跃。HBeAg血清学转换是慢性HBV感染自然史重要的一环,与HBeAg阳性患者相比,实现HBeAg阴转的患者其远期预后往往更佳。HBV感染的病程受先天免疫应答程度的影响,而HBeAg作为HBV的辅助蛋白,与感染期间宿主的免疫应答调节直接相关,高HBeAg定量水平能诱导T淋巴细胞耐受,使HBV逃避先天免疫反应建立慢性感染,在基线和治疗期间测量HBeAg定量有助于识别抗病毒治疗反应。Geng等研究发现较低的HBeAg定量(<313 S/CO)与较高的血清转化率相关。Hudu等通过对82例初治CHB患者的研究发现,高HBeAg定量患者肝硬化比例更高,预后较差。
抗-HBc是HBV感染者B淋巴细胞产生的针对HBcAg的非保护性抗体,在宿主急性HBV感染的免疫反应早期产生,是既往或目前感染HBV的标志,在人体内长期甚至终生存在。Zhang等通过对1 376例CHB患者抗-HBc定量(qAnti-HBc)及肝组织学炎症的研究发现,在初治患者中qAnti-HBc与肝脏炎症呈正相关,在治疗患者中qAnti-HBc降低与肝脏炎症缓解呈正相关。Wang等研究亦证实了qAnti-HBc与肝脏炎症之间的关系。Li等研究发现qAnti-HBc水平与纤维化分期呈正相关(r=0.367,P<0.001),对于疾病的分期、抗病毒疗效的监测具有重要价值,同时对于CHB患者HBsAg清除及停用核苷酸类似物后是否病毒学复发也具有预测作用。本研究发现基线抗-HBc<3 log10 IU/mL是LLV发生的危险因素。作为可以预测肝脏炎症严重程度的标志物,血清抗-HBc水平在ALT水平正常的CHB患者中表现出较高的诊断准确性。Li等研究发现,在49例抗-HBc<3 log10 IU/mL的患者中,有22例(约44.9%)没有发生完全病毒学应答,这些患者极有可能处于免疫耐受期,HBsAg水平、HBeAg状态、HBV DNA载量共同影响了患者最终的病毒学应答。
HBV DNA作为HBV病毒学检测的重要内容,能够帮助诊断HBV感染,判断HBV复制程度,在治疗监测、评估抗病毒疗效等方面具有重要意义。有研究显示,LLV组患者基线HBV DNA中位水平≥7 lg IU/mL,明显高于未发生组。对于高HBV DNA定量水平的描述,美国肝病学会2018版指南定义为≥1×106 IU/mL;而我国《慢性乙型肝炎防治指南(2022年版)》并未明确界定范围。尽管关于高HBV DNA定量水平的具体数值未达成一致,但基线HBV DNA水平的高低作为影响LLV发生、乙型肝炎相关肝癌预后及复发的危险因素仍然值得密切关注。目前国际上公认的“金标准”是COBAS AmpliPrep-COBAS TaqMan(CAP-CTM)实时荧光PCR HBV DNA定量检测试剂盒,具有灵敏度、特异度高,准确率及重复率好的特点,为乙型肝炎患者抗病毒治疗过程中的病情监测提供了有力支撑。对于LLV患者,高敏HBV DNA可有效指导临床决策,降低远期临床风险,避免不良结局。由于病毒基因组在受感染肝细胞的细胞核中转化为cccDNA,因此在治疗过程中很难真正消除HBV。作为病毒模板和维持慢性HBV感染的补充库,了解cccDNA的生物学特性对抗病毒治疗至关重要,但传统的分子生物学手段很难检测,新兴的检测方法如实时荧光定量PCR、磁珠杂交捕获法、滚环扩增结合原位PCR技术和微滴数字PCR、单细胞HBV cccDNA检测等,用于临床病情的长期监测存在时间及成本上的限制。试纸条作为基于单克隆技术、胶体金标记技术和免疫层析技术的检测方法,因其操作简单、反应快、设备便携等优点得到了快速发展。首都医科大学北京佑安医院段钟平教授团队研发的基于RRA-CRISPR/Cas13a的快速便携式HBV DNA检测条可用于LLV患者的检测,是一种直观、快速的替代方法,能扩大HBV感染者的诊断筛查能力和覆盖范围,简化抗病毒的疗效验证过程。
作为一线抗病毒用药,ETV是较早被批准使用的NAs,国内外关于LLV的相关研究也多集中在ETV经治患者中,这可能是有ETV治疗史是LLV发生的危险因素的原因。国内外研究均发现,序贯或联合使用TAF延长抗病毒疗程能有效提高ETV经治后发生LLV的CHB患者的完全病毒学应答率。Sanai等通过混合决策树马尔可夫状态转换模型研究发现,既往接受ETV治疗的LLV患者改用TAF,可提高完全病毒学应答的比例,降低不良事件发生率并减少37%的肝脏相关死亡,并增加成本效益比。尽管目前使用TAF的治疗成本较高,但就远期成本而言,改用TAF是一种成本-效益更优的策略,晚期肝病事件的减少不仅能降低经济成本,更能提高患者生存质量,延长生存周期。
虽然国内外指南均推荐首选强效低耐药的ETV、TDF、TAF等,但由于种种原因,目前仍存在部分患者使用拉米夫定(LAM)、替比夫定(LdT)等非一线抗病毒药物。非一线NAs药物往往抗病毒作用不足,耐药率较高。研究发现,在目前使用ETV或TDF抗病毒治疗的患者中,既往有LAM用药史者与既往无LAM用药史者相比,病毒学应答率更低,且耐药率更高。这可能也是ETV治疗史是LLV发生的危险因素的原因。
关于保护因素,本研究结果提示治疗期间依从性好、坚持抗病毒治疗(抗病毒时间≥3年和2年≤抗病毒时间<3年)、高基线ALT、治疗中HBV DNA下降幅度大可能是经治CHB患者发生LLV的保护因素。
由于NAs对HBV感染肝细胞的cccDNA没有直接作用,HBsAg清除率每年<1%,因此长期的NAs治疗通常是维持病毒学反应所必需的。研究显示,ETV和TDF治疗8年的病毒学应答率可达98%~99%,同时随着治疗时间的增加,肝细胞癌的发生风险不断降低。此外,良好的服药依从性能最大限度地提高治疗效果并降低耐药性的发展。Allard等分析了2010—2013年墨尔本4所主要医院642例CHB抗病毒治疗患者的药学和病理学记录,发现依从性与良好的结局之间呈线性相关,随着依从性的下降,病毒学突破的风险增加。Shin等对894例初治CHB患者10年的纵向观察研究同样证实了依从性差的患者比依从性好的患者有更高的病毒学突破风险(HR=22.42,95%CI:19.57~52.52,P<0.001),且肝细胞癌的发生风险增加2.9倍(95%CI:1.761~4.643,P<0.001),肝硬化并发症的发生风险也增加2.9倍(95%CI:1.925~4.247,P<0.001),全因死亡率的风险增加5.0倍,肝脏相关死亡率的风险增加14.3倍,这种不利影响在肝硬化患者中表现得更为突出。特别强调的是,采用最佳的服用方式(ETV需空腹;TDF与食物同服)也能有效提高病毒学应答率,降低LLV发生风险。值得注意的是在纳入研究中均未指出依从性的明确定义,这可能造成结果在合并时出现偏倚,但是依从性对于抗病毒疗效的影响是毋庸置疑的。在长期的抗病毒治疗中临床医生定期对依从性进行评估十分必要。
血清ALT水平变化可反映肝脏的炎症活动程度,亦可反映机体抗HBV免疫应答的强弱,是肝细胞损伤的主要标志。研究表明,ALT水平越高,表明机体免疫反应越强烈,发生血清HBeAg阴转的可能性就越高,是HBeAg血清转换最关键的独立预测因素。
本研究发现治疗中高HBV DNA下降幅度是LLV发生的保护因素。Boglione等研究证实HBV DNA下降幅度是持续病毒学应答的预测因子。Hansen等亦发现治疗24周内HBV DNA下降2 lg IU/mL与完全病毒学应答密切相关(OR=5.7,95%CI:1.7~20.0,P=0.004)。宿主免疫影响CHB患者的抗病毒疗效,辅助性T淋巴细胞17(Th17)/调节性T淋巴细胞(Treg)在介导抗病毒治疗的免疫应答中起重要作用。研究发现HBV病毒载量高低与机体Th17和Treg及其比率之间存在直接关系,随着病毒载量的增加,Th17、Treg细胞及其比率均增高;经抗病毒治疗后,病毒载量下降,机体炎症反应减弱,Th17、Treg细胞及其比率也随之降低。Th17/Treg平衡失调已经被证实与CHB患者肝功能损伤和肝纤维化相关,积极有效的抗病毒治疗能最大程度地抑制病毒在体内的复制,有助于恢复CHB患者的T淋巴细胞免疫。Liu等通过对接受NAs治疗3~5年后HBeAg消失、抗-HBe存在、ALT水平持续正常且HBV DNA低于检测下限的CHB患者分析发现,经过抗病毒治疗且病毒复制抑制后,循环CD56dim自然杀伤细胞和Th17/Treg平衡得到恢复,并有助于降低患者HBsAg水平。
本研究的局限性在于:(1)受研究类型、纳入排除标准的影响,关于LLV发生率和影响因素的原始研究数量有限,纳入文献数量较少,可能对结果合并造成一定影响,需要更高质量、大样本的研究加以验证。(2)原始研究中存在诸多不能进行合并的影响因素,而在可合并的影响因素中标准不统一,如未明确定义依从性好/差、高基线HBV DNA水平等,上述问题可能影响Meta分析结果。
全文下载
https://www.lcgdbzz.org/cn/article/doi/10.12449/JCH240709



