Cardiovasc Res .:活化T细胞核因子5对于肺内皮细胞对缺氧的平衡适应性转录反应是不可或缺的
时间:2024-08-08 18:00:09 热度:37.1℃ 作者:网络

目的
慢性缺氧会导致肺部结构发生有害变化,进而可能引发肺动脉高压,而这一过程部分由内皮细胞介导。尽管缺氧在肺相关疾病发展中的重要性已经得到广泛认可,但控制肺内皮细胞对缺氧初期适应的决定因素仍然很大程度上未被探索。
方法和结果
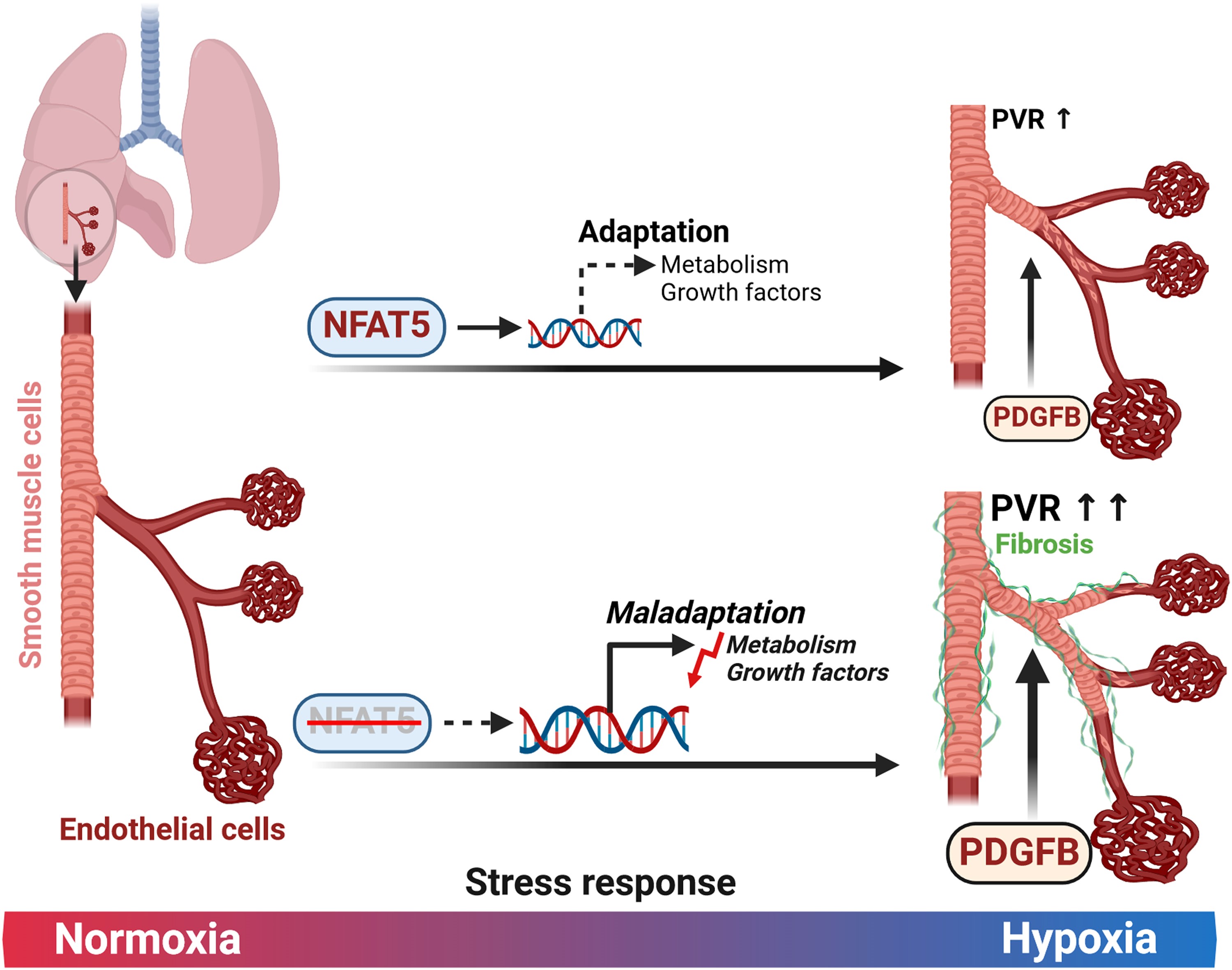
本研究中,我们发现缺氧会激活转录因子活化T细胞核因子5(NFAT5),并研究了其在小鼠肺内皮细胞(MLEC)中的调控功能。通过建立特异性敲除内皮细胞中Nfat5基因的小鼠模型(Nfat5(EC)−/−),并将其暴露于常压缺氧环境(10% O2)21天,结果显示,与对照组小鼠相比,Nfat5(EC)−/−小鼠表现出明显的血管纤维化,并加剧了肺动脉右心室收缩压的增加及右心室功能障碍。基于微阵列和单细胞RNA测序的分析显示,Nfat5缺失的MLEC在暴露于缺氧环境7天后,其生长因子、能量和蛋白质代谢相关基因的表达受到显著影响。具体来说,NFAT5的丧失显著增加了血小板源性生长因子B(Pdgfb)的表达和释放,Pdgfb是由缺氧诱导因子1α(HIF1α)调控的血管平滑肌细胞(VSMC)生长驱动因子。在缺氧暴露的Nfat5(EC)−/−小鼠中,这一变化伴随着远端肺动脉的VSMC覆盖的加剧。
为了进一步验证NFAT5在缺氧反应中的具体作用,我们对缺氧环境下的小鼠肺内皮细胞进行了详细的转录组学分析。结果显示,缺氧导致了NFAT5的激活,而NFAT5的丧失则导致了多个关键调控通路的紊乱。这些通路包括与细胞生长因子、能量代谢和蛋白质代谢相关的基因表达,特别是那些受到HIF1α调控的基因。在这些基因中,Pdgfb的表达显著增加,提示NFAT5在调控HIF1α下游基因表达中的重要作用。进一步的实验表明,NFAT5通过直接与Pdgfb启动子区域结合,抑制其在缺氧条件下的表达,从而限制了VSMC的过度增生和血管重构。
结论
总体而言,我们的研究表明,MLEC对缺氧的早期和短暂的亚群特异性反应可能决定后期器官功能障碍的程度。在这种情况下,NFAT5作为一种保护性转录因子,需要迅速调整内皮转录组以应对缺氧。具体来说,NFAT5限制了HIF1α介导的Pdgfb表达,从而限制了肺血管的肌肉化和阻力。我们的研究揭示了NFAT5在缺氧应答中的关键保护性作用,提示其可能是治疗缺氧相关肺部疾病的潜在靶点。
通过深入理解NFAT5在缺氧条件下的作用机制,我们可以开发出更有效的治疗策略,以减轻或逆转缺氧引起的肺部损伤和功能障碍。未来的研究应着重于探讨NFAT5与其他转录因子及信号通路的交互作用,进一步阐明其在肺内皮细胞中的具体功能和机制。这将有助于我们全面理解缺氧相关肺部疾病的病理生理过程,并为开发新型治疗手段提供理论基础和实验依据。
本研究的结果不仅丰富了我们对肺内皮细胞在缺氧条件下适应机制的认识,还揭示了NFAT5作为治疗缺氧相关肺部疾病潜在靶点的可能性。通过针对NFAT5及其调控的信号通路,我们或许能够找到新的方法来减轻慢性缺氧对肺部的有害影响,从而改善患者的生活质量。
原始出处:
Laban H, Siegmund S, Schlereth K, Trogisch FA, Ablieh A, Brandenburg L, Weigert A, De La Torre C, Mogler C, Hecker M, Kuebler WM, Korff T. Nuclear factor of activated T-cells 5 is indispensable for a balanced adaptive transcriptional response of lung endothelial cells to hypoxia. Cardiovasc Res. 2024 Aug 6:cvae151. doi: 10.1093/cvr/cvae151. Epub ahead of print. PMID: 39107245.


