Basic Res Cardiol 上海健康医学院黄钢/吴兰/李延飞团队揭示自发性运动对抗乳腺癌导致的心脏损伤的保护作用及机制
时间:2024-08-23 22:00:31 热度:37.1℃ 作者:网络
心血管疾病已经成为癌症患者第二大死亡原因,主要包括肿瘤患者伴随心脏恶病质或在抗肿瘤治疗过程中引起的心血管损伤。多项临床研究表明,晚期癌症患者心脏消耗导致心肌变薄、心室质量下降和心肌纤维化,表现为心脏恶病质,进而导致心脏损伤。同时,癌症诱发的心脏损伤的概念在临床前水平上也得到了支持。这些研究强调了对癌症诱发的心脏损伤进行研究的必要性和迫切性,并设想设计新的治疗方法。
最近研究表明,自发性乳腺癌MMTV-PyMT转基因小鼠的血浆炎性因子偏高,而左心室功能、心肌质量和钙调控相关蛋白表达比野生型小鼠有所下降,运动在一定程度上可以减轻乳腺癌导致的心肌损伤,关于其具体机制并未作深入探讨。
STAT3在心肌保护对抗心肌缺血再灌注损伤和肿瘤治疗导致心肌毒性中具有重要地位。运动可以激活STAT3对抗心梗和心力衰竭。STAT3可以作为转录因子调控microRNA及其靶蛋白的表达。关于自发性运动是否激活STAT3调控microRNA及其靶蛋白对抗乳腺癌导致的心脏损伤尚不清楚。
2024年8月19日,上海健康医学院上海分子影像学重点实验室黄钢教授、基础医学院/附属周浦医院吴兰副教授、医学技术学院李延飞副教授团队合作在Basic Research in Cardiology在线发表了题为“Cardioprotection of voluntary exercise against breast cancer-induced cardiac injury via STAT3” 的研究论文,阐明了STAT3在自发性运动对抗乳腺癌导致的心脏损伤中的具体机制,为该疾病的防治提供了临床转化的新思路与治疗靶点。

首先,为探讨自发性运动对乳腺癌小鼠的心脏形态及功能的保护作用,研究者将12周龄的同窝MMTV-PyMT阳性小鼠和MMTV-PyMT阴性小鼠分别分组为静息组和运动组,运动组进行4周的自发性跑轮运动,并测定分组后的小鼠单位时间的耗氧量。实验开始前和实验结束后分别测定每组小鼠的心肌收缩功能和心肌舒张功能。研究发现虽然其心肌射血分数和部分舒张功能参数组间无明显差异,但阳性小鼠的心肌质量、心肌收缩应变、心室壁厚度、心室内径和等容舒张期较阴性小鼠有所改变,且运动可以改善阳性小鼠心功能参数。实验结束后再测定小鼠心肌纤维化面积、心肌细胞大小、细胞存活率及血浆中TNF-α的含量,发现阳性小鼠较阴性小鼠有明显的损伤,且运动可以改善这些指标。
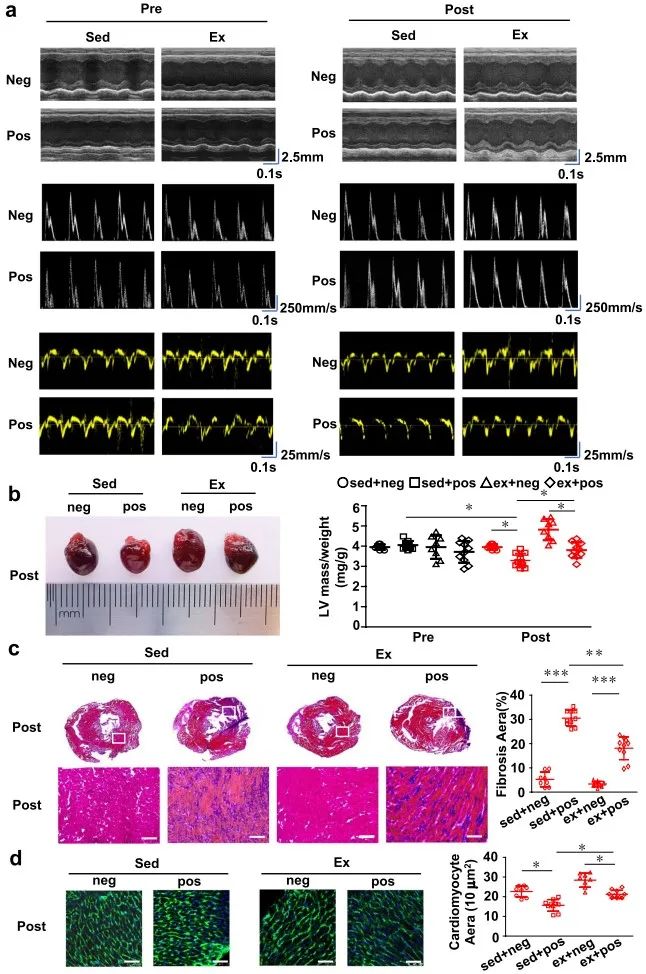
其次,为了探究STAT3和microRNA在运动对抗乳腺癌导致的心脏损伤产生心肌保护效应中的作用,研究者对心肌细胞的STAT3蛋白及其相关的蛋白表达进行测定,并进行microRNA测序。研究者发现自发性运动后心肌细胞内STAT3的705磷酸化水平增高,并伴随miR-181a-5p上调和miR-130b-3p的下调。进一步在动物实验中,研究者通过腺相关病毒心肌多点注射实验证明了STAT3参与自发性运动对抗的乳腺癌导致的心肌损伤。
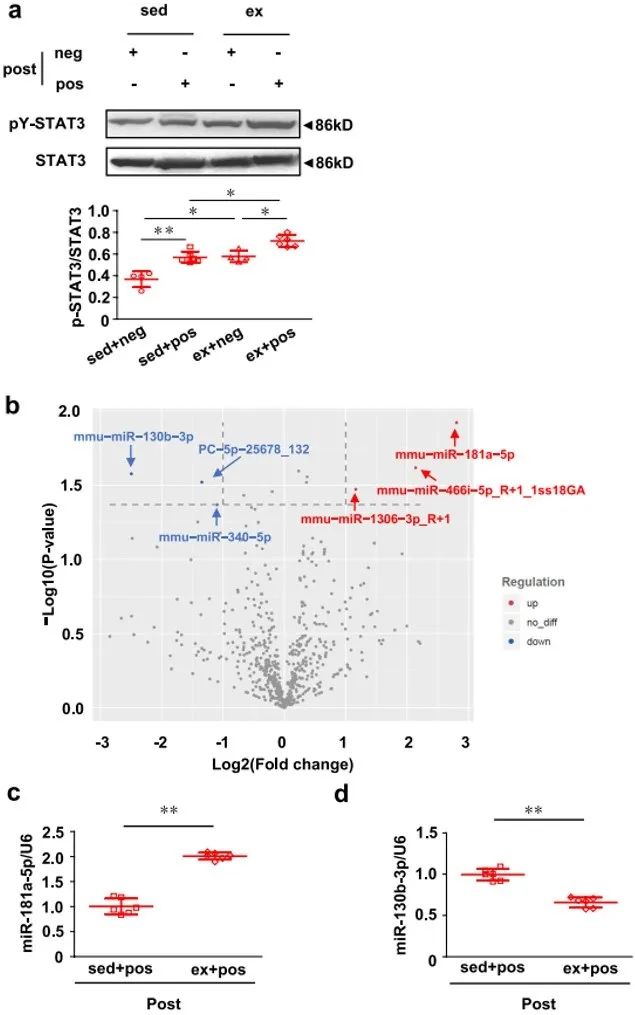
再次,为了阐明STAT3-microRNA的调控机制及下游作用靶蛋白在心肌保护中的机制,研究者在小鼠心肌细胞中通过生物信息学预测和免疫染色质共沉淀验证了STAT3可以作为上游转录因子调控pre-miR-181a和HOTAIR的表达。进一步在AC16心肌细胞系中,研究者通过生物信息学预测和双荧光素酶报告实验验证了miR-181a-5p的下游靶蛋白是PTEN (抑制心肌存活蛋白)、HOTAIR可以通过海绵吸附miR-130b-3p使其下调以及miR-130b-3p下游的靶蛋白是Zbtb20 (促进心肌收缩蛋白)。
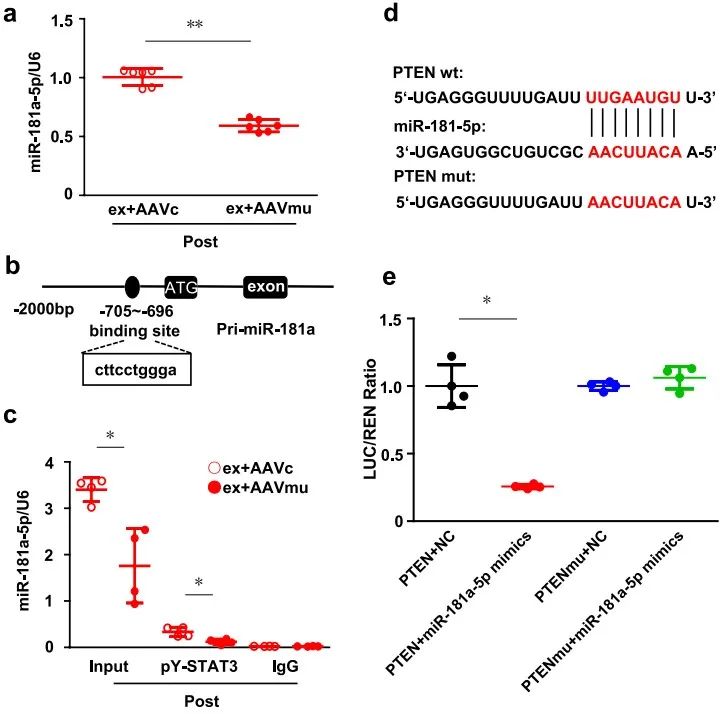
综上所述,该研究揭示了STAT3在乳腺癌导致的心脏损伤中发挥保护作用的分子机制。乳腺癌可诱发心肌损伤,而自发性运动可以通过激活STAT3上调miR-181a-5p靶向PTEN改善心肌存活,以及通过上调HOTAIR吸附miR-130b-3p靶向Zbtb20改善心肌收缩功能从而产生心肌保护效应,为乳腺癌导致的心脏损伤的临床防治提供了新思路与潜在靶点。
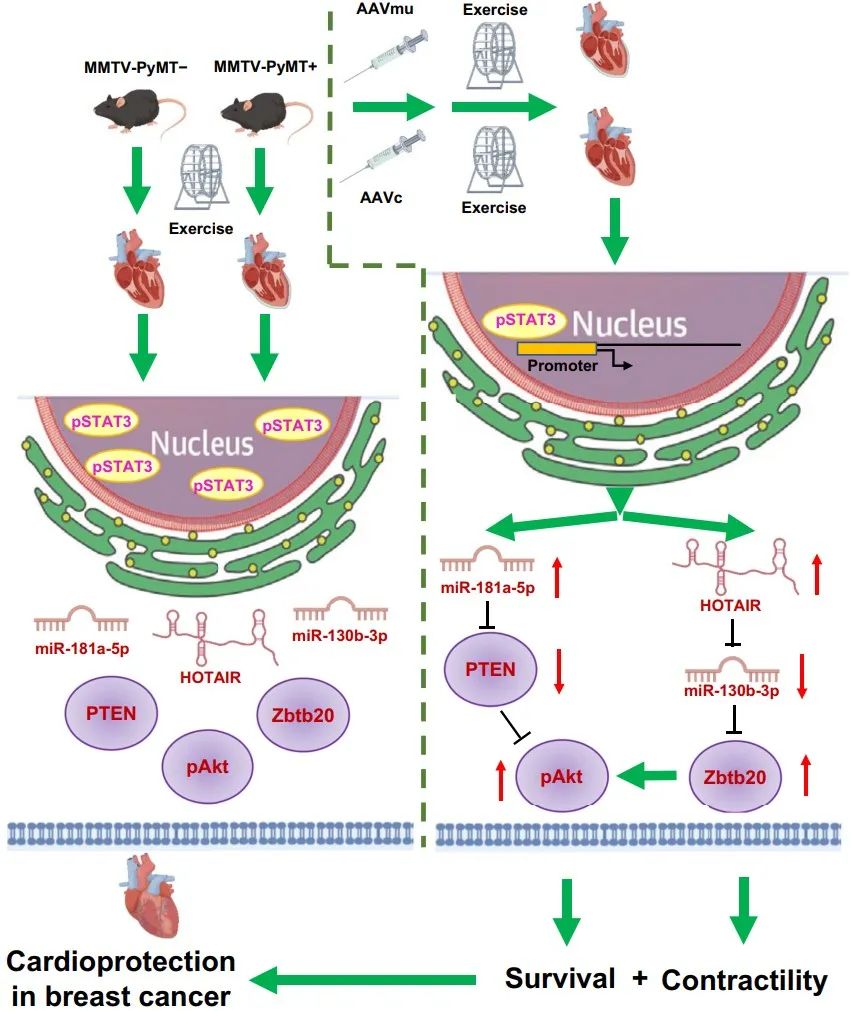
该研究由上海健康医学院上海市分子影像学重点实验室黄钢教授、基础医学院/附属周浦医院吴兰副教授、医学技术学院李延飞副教授为共同通讯作者。基础医学院/附属周浦医院吴兰副教授为该文章的第一作者,哈佛大学麻省总医院心血管科的Emeli Chatterjee博士为论文修改提供宝贵意见。该工作得到了国家自然科学基金、上海市卫生健康委员会临床专项、上海市分子影像学重点实验室建设项目,上海健康医学院地方高水平大学建设项目的支持。
原文链接
https://link.springer.com/article/10.1007/s00395-024-01076-8


