读书报告|ECMO和非ECMO急性呼吸窘迫综合征幸存者的功能恢复
时间:2024-09-06 06:01:08 热度:37.1℃ 作者:网络

背景
静脉-静脉体外膜肺氧合 (ECMO) 是一种挽救疗法,部分用于伴有严重低氧血症的ARDS患者。对于严重的ARDS,使用ECMO干预,可以纠正致命的低氧血症,并减轻机械通气的潜在危害。2023年欧洲重症监护医学会(ESICM)关于ARDS的指南强烈建议在ECMO中心对重症COVID-19和非COVID-19 ARDS患者进行ECMO。
对ARDS幸存者的研究表明,虽然大多数患者的肺活量测定和肺容积在1年后恢复正常,但肺一氧化碳弥散能力( DLCO)、6分钟步行试验(6MWT)和心理创伤持续受损长达5年。既往研究探讨了ECMO幸存者的功能和肺部恢复情况,发现其与未接受ECMO治疗的ARDS患者相当。但这些研究早于当前ARDS的实践模式及COVID-19大流行之前,COVID-19大流行导致住院和ICU住院时间总体延长,ECMO持续时间延长。
鉴于ECMO作为一种资源的稀缺性、成本和潜在发病率,研究其院内死亡率以外的结果非常重要,以便更好地为ECMO分配和利用的决策提供信息。我们报告了接受ECMO治疗的当今严重ARDS幸存者与未接受ECMO治疗的ARDS患者队列的长期肺部、身体和神经认知恢复情况。
方法
这项研究于2020年1月至2023年1月进行。这项研究被马里兰大学和R Adams Cowley休克创伤中心内部审查委员会 (IRB)确定为豁免。
患者选择
所有患者都是马里兰大学医学中心(UMMC)、R Adams Cowley 休克创伤中心和马里兰大学巴尔的摩华盛顿医学中心(BWMC)的危重病幸存者(包括ECMO幸存者),并在UMMC或BWMC ICU后诊所接受随访。
马里兰大学ECMO标准
虽然在整个COVID-19大流行期间,ECMO插管的标准略有不同,但总的来说,马里兰大学利用以下指南来确定谁应该考虑插管:①高碳酸血症 (PaCO2>60 mmHg,pH<7.25或平台压<30 cmH2O时无法维持通气);②严重低氧血症 (P/F<50 mmHg,FiO2>80% ,>3小时;P/F<80%,FiO2 80 mmHg,>6小时不能纠正)。
ECMO的相对禁忌证明:年龄>60岁;BMI > 40 kg/m2;机械通气>10天;家庭需氧疗;严重的神经损伤;终末期疾病,1年生存率低;严重基础肝病;急性肝衰竭;耶和华见证人(不愿接受血);艾滋病;基线功能状态差。
数据提取
从电子病历中提取人口统计学、入院序贯器官功能评估(SOFA)评分、ARDS病因、呼吸机参数、血管加压药要求、实验室数据、住院ARDS治疗(即皮质类固醇、俯卧位、机械通气)、治疗持续时间和临床结果。在到达UMMC、休克创伤或 BWMC后24小时内和ECMO插管之前提取呼吸机参数。报告最差参数,由最高PEEP或需要气道压力释放通气(APRV)定义,在前24小时内。
数据分析
我们比较了ECMO和非ECMO患者,对分类变量使用独立性卡方检验,对离散变量使用Mann-Whitney U检验。感兴趣的主要结局是将ECMO与非ECMO患者进行比较时预测的用力肺活量(FVC)%。预测的 FVC% 被选为限制性肺生理学的肺活量替代物。
次要结局包括肺活量测定、肺容积、DLCO、6MWT、HADS、PCL-5和MoCA。
我们进行了单因素和多因素回归,对每个临床协变量拟合了单变量模型,并确定了在P=0.25水平上显著的预测因子。在每个步骤中,根据P值、省略高度共线变量以及临床和生物学合理性添加变量。Akaiki 信息准则(AIC)用于对最终模型中包含的变量总数设置限制。我们重复了上述分析,将我们的患者限制在一组COVID-19患者中。
结果
从2020年1月到2022年12月,马里兰大学医学中心、R Adams Cowley休克创伤中心和马里兰大学巴尔的摩华盛顿医学中心成人急诊科或ICU就诊了3005例患者,P/F比为≤300 mmHg。在同一时期,211例符合柏林ARDS标准并伴有难治性低氧血症的患者在马里兰大学医学中心/R Adams Cowley休克创伤中心插管进行 VV-ECMO。在P/F≤300 mmHg的3005例患者中,有1997例在出院时存活,其中包括141例插管ECMO的患者。共有110例患者在需要VV-ECMO或因ARDS入住ICU后生存并接受ICU后随访;这些患者是本分析的重点(图1)。
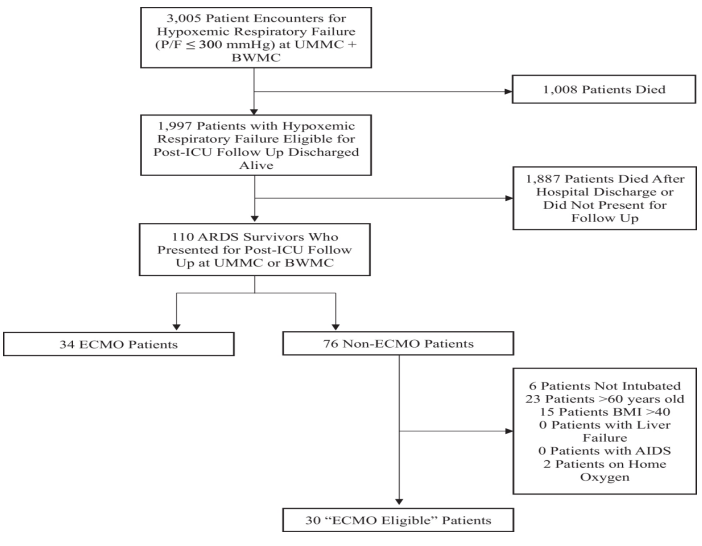
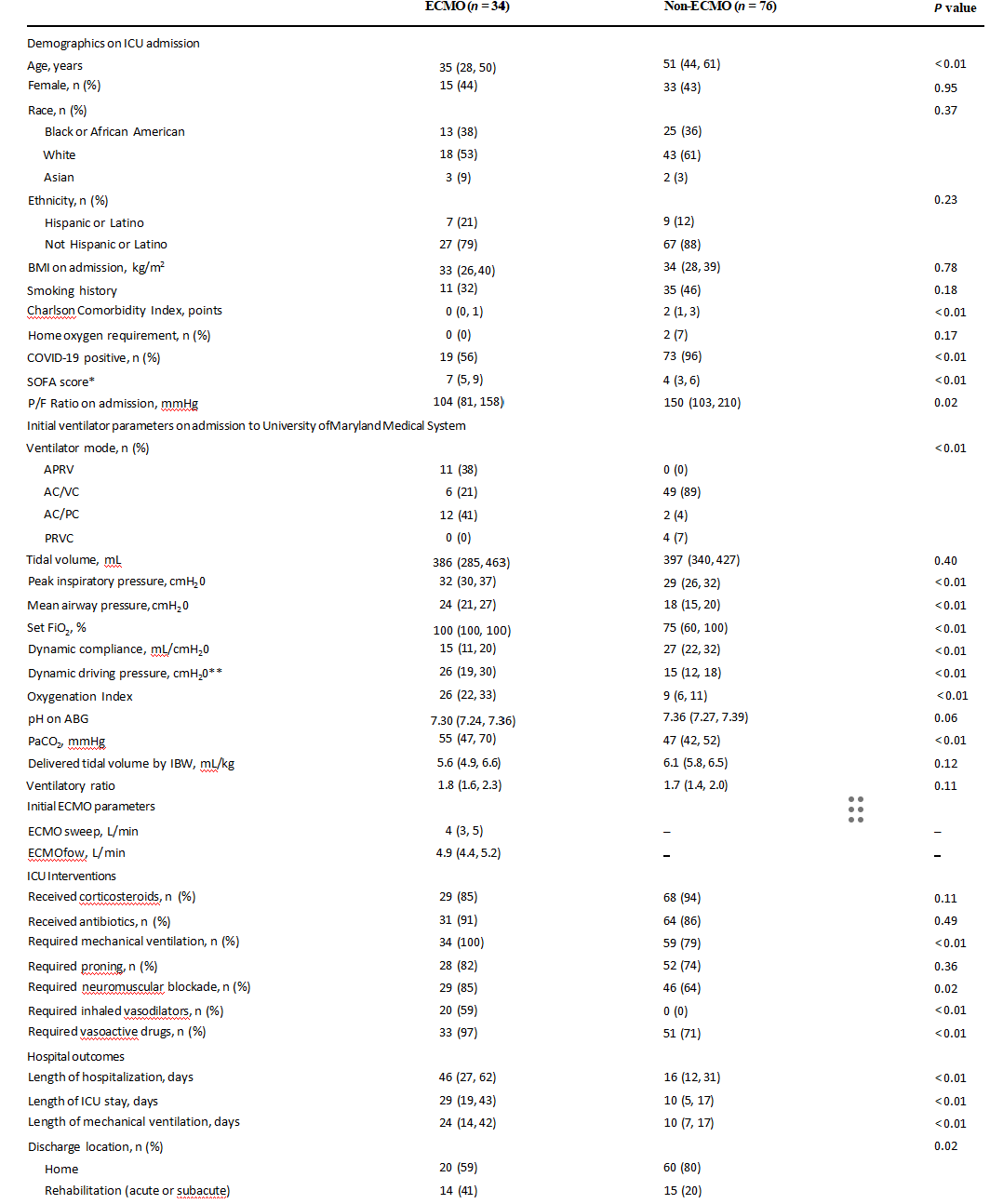
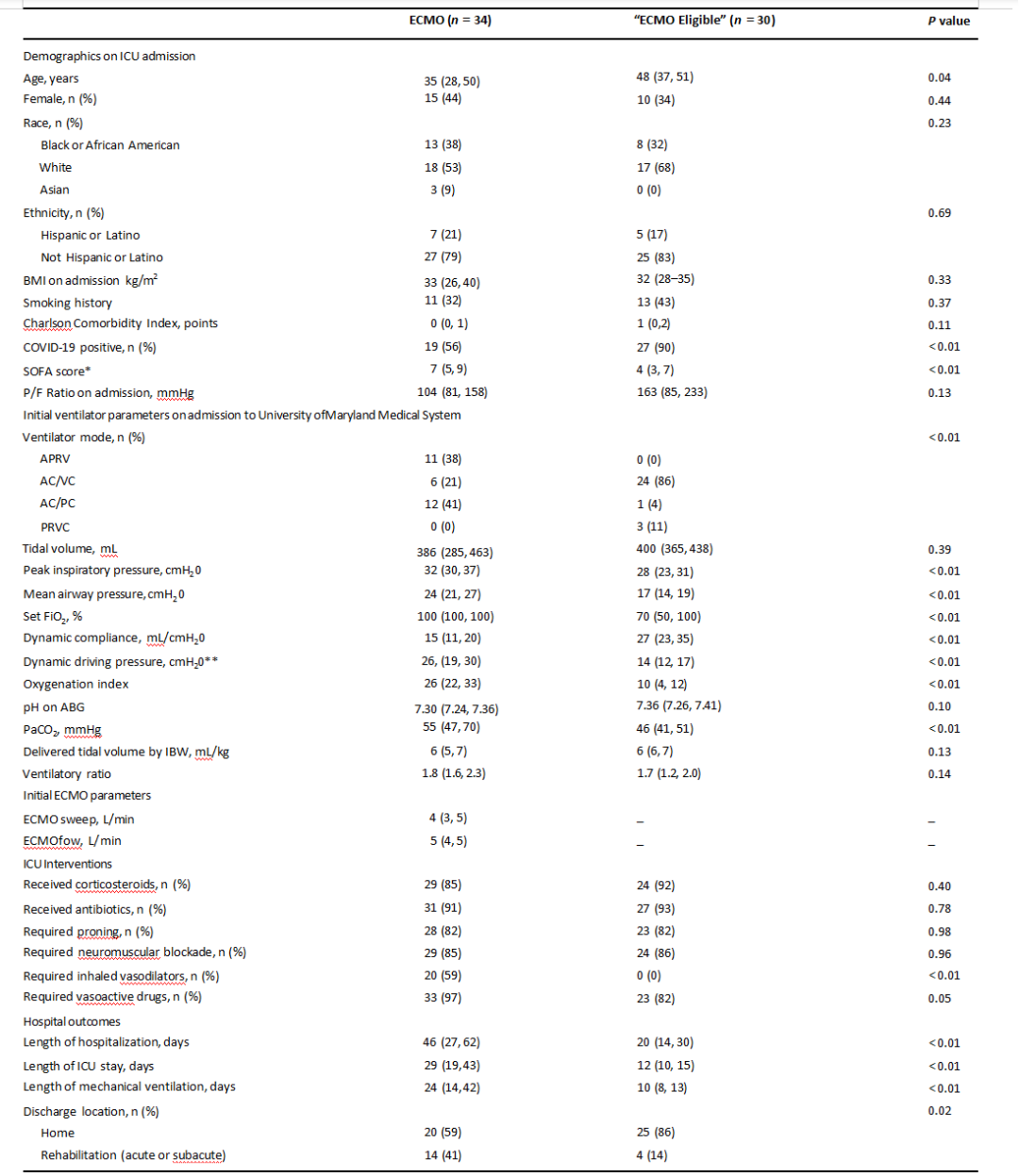
表1描述了纳入的110例患者在初次就诊到ICU时的人群特征、基于ICU的干预措施和医院结局。当将ECMO(n=34)与非ECMO(n=76)队列进行比较时,ECMO患者更年轻,ECMO组的COVID-19患者比例较小(56%,P< 0.01)。ECMO队列中ARDS的病因总结见附加文件1,表1。接受ECMO治疗的患者入院时SOFA评分较高[7(5,9)vs. 4(3,6),P<0.01],入院PaO2较低/FiO2比值[104(81,158)mmHg vs. 150(103,210)mmHg,P=0.02]。接受ECMO治疗的患者更可能处于挽救性通气模式,并且吸气峰值压、平均气道压力、动态驱动压力、FiO2显著更高要求和 PaCO2。ECMO患者的动态顺应性也显著降低,氧合指数较高。与非ECMO组相比,ECMO组插管、接受神经肌肉阻滞、吸入血管扩张剂和血管活性药物的患者明显更多。ECMO组的中位住院时间[46(27,62)天 vs. 16(12,31)天,P<0.01]、ICU住院时间[29(19,43)天 vs. 10(5,17)天,P<0.01]和机械通气天数[24(14,42)天vs. 10(7,17)天,P<0.01](表1)。
Table S1. Etiologies of ARDS in ECMO patients
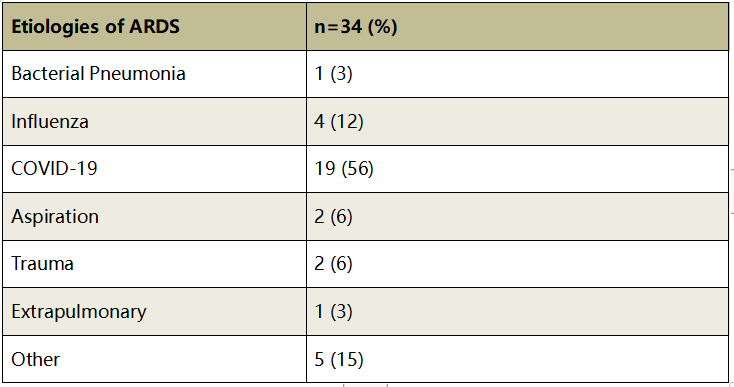
表1 ECMO状态分层患者基线人群特征
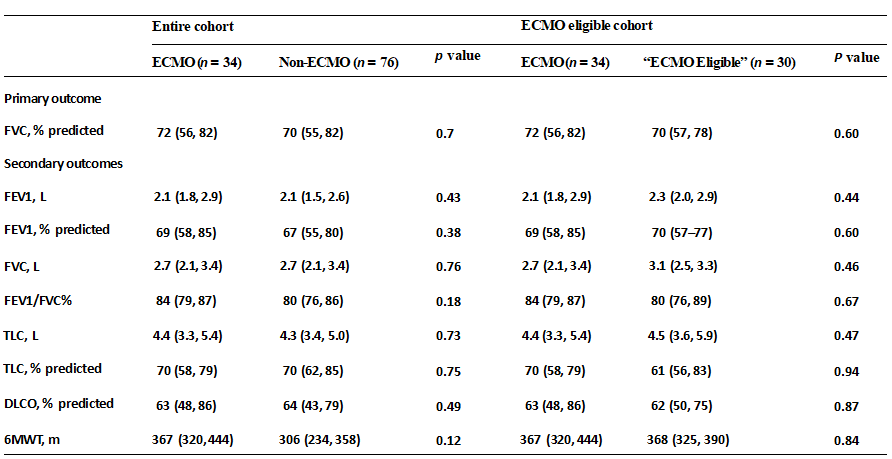
ECMO治疗与非ECMO治疗患者的肺功能
平均在出院后100天进行肺功能检查。ECMO组与非ECMO组预测的FVC%无显著差异。ECMO组和非ECMO组的患者均表现出基于FVC%预测值和总肺活量(TLC)的轻度限制。ECMO和非ECMO队列的DLCO和6MWT均有适度降低。将使用ECMO管理的患者与未接受ECMO的患者进行比较时,任何肺活量计参数,肺容积,DLCO或6MWT均无显著差异。
在单因素回归分析中,与非ECMO相比,使用ECMO并未预测肺活量测定、肺容积、DLCO或6MWT有任何显著差异。在调整年龄时,未观察到肺功能指标的显著差异。同样,在根据年龄、SOFA、住院时间(LoS)和COVID-19状态进行调整的多变量分析中,与未接受ECMO的患者相比,使用ECMO并未预测肺恢复的任何变化。
表2 肺活量测定、肺容积和6分钟步行试验的差异
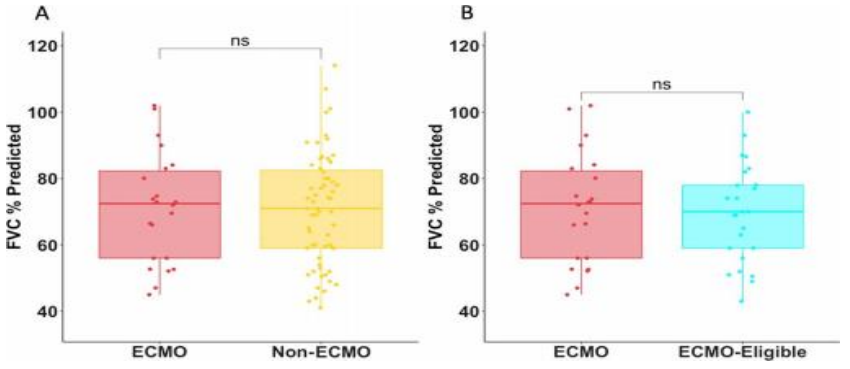
预测将(A)ECMO(红色)与非ECMO(黄色)患者进行比较的FVC%;(B)ECMO(红色)至“符合 ECMO 条件”(蓝绿色)患者。ns=Mann-Whitney U检验不显著。
ECMO治疗与非ECMO治疗患者的神经认知和心理恢复
对神经认知和心理后遗症的探索性分析见表S2:将ECMO与非ECMO队列进行比较时,MoCA、HADS或PCL-5评分没有差异。
Table S2. Psychological Health Outcomes.

MOCA评分≥26分被认为是正常的,18~25分为轻度认知障碍,10~17分为中度认知障碍,<17分为重度认知障碍。
HADS评分是焦虑和抑郁得分的总和。焦虑21分,抑郁21分。分量表(焦虑或抑郁)0~7分正常,8~10分为边缘,≥11分提示临床病例。
创伤后应激障碍 (PTSD) 使用 DSM-5的PTSD检查表(PCL-5),总分范围为0~80分,0~20分表示没有或很少的症状,分数越高,症状越重。
COVID-19人群
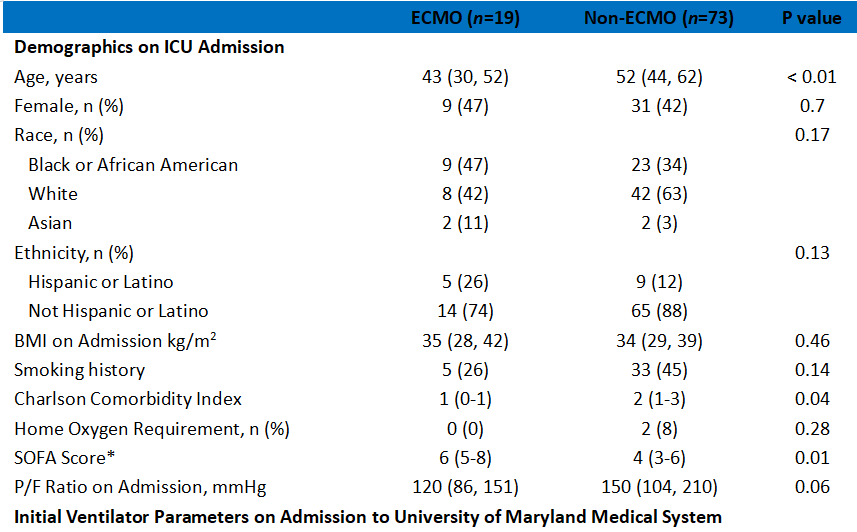
研究人群包括92例因诊断为COVID-19 ARDS而需要ECMO或入住ICU的患者,其中19例接受了ECMO治疗,其中73例未接受治疗。与非ECMO组相比,接受ECMO治疗的患者明显更年轻[43(30,52)岁 vs. 52(44,62)岁,P<0.01],Charlson合并症指数较低[1分(0,1)vs. 2 分(1,3),P=0.04]和更高的 SOFA 评分[6(5,8)vs. 4(3,6),P=0.01]。 与COVID-19非ECMO队列相比,COVID-19 ECMO患者对呼吸机的要求明显更高,住院时间更长[56(38,66)天 vs. 16(11,31)天,P<0.01]、ICU 住院时间[40(27,61)天 vs. 10(5,17)天,P<0.01]和需要机械通气的天数[35(27,46)天 vs. 10(7,16)天,P<0.01]。

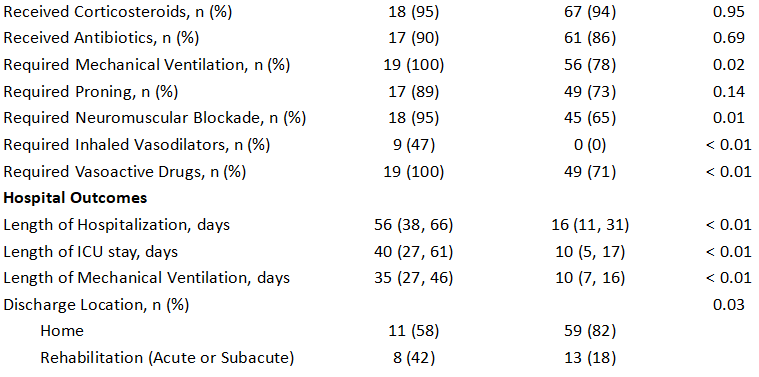
ECMO与非ECMO治疗COVID-19患者的肺功能
在COVID-19队列中,ECMO患者的6MWT距离更长(381 m vs. 294 m,P=0.02)。将COVID-19 ECMO队列与COVID-19 非ECMO队列进行比较时,肺活量测定或肺容量没有其他显著差异。ECMO在单变量分析或调整年龄的分析中没有预测肺功能的任何差异。一项针对年龄、SOFA和医院LoS进行调整的多变量分析显示,与非ECMO组 (P=0.03) 相比,ECMO与预测的FEV1%增加16.4% (CI 1.5~31.4)相关 (P=0.03),这在考虑多重比较时不符合统计学意义(COVID-19患者肺活量测定、肺容积和6分钟步行试验的差异)。
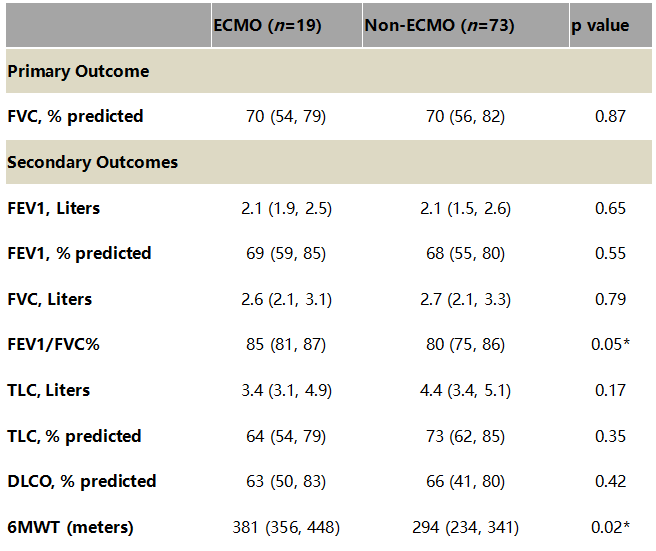
注:除非另有说明,否则数据以中位数(Q1-Q3)表示。*<0.00625,基于Bonferroni的多重比较校正,< 0.00625被认为是显著的。
< style="color: rgba(0, 0, 0, 0.9);">“符合ECMO条件”的人群 < style="color: rgba(0, 0, 0, 0.9);">为了将接受ECMO治疗的患者与年龄相近、既往存在合并症和急性疾病严重程度的患者进行比较,我们确定了一组合格患者。与这些“符合ECMO条件”的患者相比,接受ECMO治疗的患者明显更年轻[35(28,50)岁 vs. 48(37,51)岁,P= 0.04],COVID-19阳性的可能性更低(56% vs. 90%,P<0.01), 并且SOFA评分更高[7(5,9)vs. 4(3,7),P<0.01]。ECMO患者需要更多的呼吸机支持,并且肺部生理功能异常,这从他们的吸气压、平均气道压力、动态驱动压力、呼吸机FiO2明显升高可以看出、氧化指数、PaCO2和较低的PaO2和动态顺应性(表4)。所有患者均采用机械通气,俯卧位或神经肌肉阻滞的使用无差异。与“符合ECMO条件”组相比,接受ECMO治疗的患者更频繁地需要吸入血管扩张剂和血管活性药物。ECMO患者的住院时间明显更长[46(27,62)天 vs. 20(14,30)天,P<0.01]、ICU住院时间[29(19,43)天 vs. 12(10,15)天,P<0.01]和需要机械通气的天数[24(14,42)天 vs. 10(8,13)天,P<0.01]( 表4)。
表4 接受ECMO治疗的患者与符合ECMO条件的患者的基线人群特征
ECMO与“符合ECMO条件”患者的肺功能:将插管ECMO的患者与“符合ECMO条件”的患者进行比较时,肺活量测定、肺容积、DLCO或6MWT无显著差异。
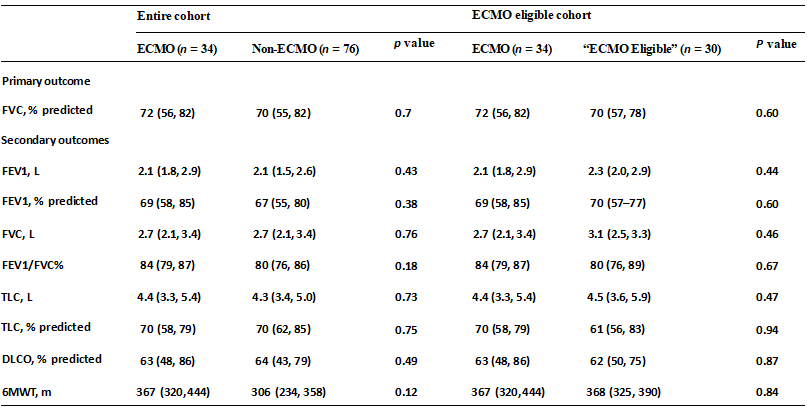
在针对年龄、SOFA、COVID-19和住院时间进行调整的单因素和多因素回归中,ECMO未预测肺活量测定、肺容量、DLCO或6MWT有任何显著差异。在针对年龄和COVID-19调整的敏感性分析中,这种相关性的缺乏仍然存在。
讨论
该研究报告了ECMO与不使用ECMO的ARDS幸存者相比的最大同时期功能结局比较。还报告了一项新的直接比较,根据回顾性评估,将使用ECMO的患者与符合ECMO条件但未插管的患者进行了新的直接比较。ECMO和非ECMO患者在出院后平均92天通过肺活量测定观察到轻度限制性通气障碍。非ECMO的预测中位FVC%为70%,而ECMO为72%。这一发现与Herridge等先前在ARDS幸存者中开展的研究结果一致,将ECMO与非ECMO幸存者进行比较时,即使调整年龄、SOFA、COVID-19状态和住院时间,任何恢复标志物均无统计学意义差异。
虽然该研究的样本量排除了倾向评分匹配方法的使用,但创建一个明确定义的“符合 ECMO 条件”的子集,并结合回归建模调整两个队列之间的基线差异,试图最大限度地减少混杂因素的影响。即使使用该对照组,基于较高的平均 SOFA 评分,需要使用更高压力、更高 FiO2,接受ECMO治疗的患者病情明显更重、受损的二氧化碳清除率、肺顺应性降低、ICU住院时间及总住院时间延长,吸入支气管扩张剂和血管加压药的使用率增加。这些因素中的每一个都有可能损害恢复。因此,可以预期,这个病情较重的ECMO群体的功能恢复会更差。然而,该研究结果表明,尽管ECMO患者的病情更严重,但ECMO的患者的功能恢复与非ECMO患者相似。
这是自Grasselli等发表的研究,于2013—2015年招募患者以来,首次将ECMO患者的肺、精神和神经认知功能与同期ARDS非ECMO幸存者进行比较,同时期非 ECMO 的使用确保了两组都暴露于相同的ARDS临床实践模式。马里兰大学是一个城市四级护理中心。该大学照顾被边缘化的患者(通常没有保险、缺乏初级保健、低收入和高度脆弱,在医疗护理方面存在无数障碍)。这些健康的社会决定因素可能会增加不良结果的风险。然而,该研究的结果表明,尽管这些患者通常缺乏资源并且在出院后遇到纵向护理障碍,但大多数幸存者在医院随访中仅表现出轻度至中度的肺功能损害,并且在医院随访中没有明显的神经认知或精神障碍。
预计FVC%被用作限制性肺生理学的替代物的主要结局。与非ECMO组或“符合 ECMO 条件”组相比,ECMO组预计FVC%没有差异,这表明该组没有更严重的限制性肺病。然而,重要的是要考虑到ECMO队列始终明显比非ECMO队列年轻。因此,如果这种程度的轻度限制持续存在,与年龄较大的非ECMO或”符合ECMO条件”的队列相比,ECMO患者将在更多的工作、生殖和功能寿命中承担这种疾病的负担。Herridge等的研究表明,在ARDS幸存者中,6个月时预计FVC%恢复正常。因此,需要进行纵向随访,以评估ECMO患者是否能看到这种轨迹。
该研究报告了ECMO与不使用ECMO的ARDS幸存者相比的最大同时期功能结局比较。还报告了一项新的直接比较,根据回顾性评估,将使用ECMO的患者与符合ECMO条件但未插管的患者进行了新的直接比较。ECMO和非ECMO患者在出院后平均92天通过肺活量测定观察到轻度限制性通气障碍。非ECMO队列的预测中位FVC%为70%,而ECMO队列为72%。这一发现与Herridge等先前在ARDS幸存者中开展的研究结果一致,将ECMO与非ECMO幸存者进行比较时,即使调整年龄、SOFA、COVID-19状态和住院时间,任何恢复标志物均无统计学意义差异。
局限性
其中最重要的是它的观察性。ECMO最初分配合并症和插管禁忌证较少的年轻患者,这些患者通常处于病程早期,揭示了固有的选择偏差,我们只能在回归分析中对其进行部分调整。
本研究还存在选择偏倚,因为该研究仅包括仍然活着且有能力、资源和愿望完成门诊长期随访和功能测试的个体,可能会遗漏病情最重、残疾最严重的患者以及康复率最高的患者。这项研究是在一家学术医疗中心进行的,因此这些数据可能高估了更广泛的ECMO人群的功能恢复。
肺活量测定是一种单维结果,在检测限制方面可能不敏感,可能受到ICU获得性肌无力的影响,并且不能量化整体功能障碍或必然转化为生活质量
本研究没有获得ECMO插管后患者的呼吸机参数。据推测,ECMO的益处是使用“超低容量通气”,这被认为可以避免肺顺应性差患者的额外呼吸机诱导的肺损伤。目前尚不清楚是否使用了该策略,以及该策略对随访时的肺功能有何影响。
大多数非ECMO患者有COVID-19。没有关于COVID-19患者感染的SARS CoV-2 (严重急性呼吸系统综合征冠状病毒2型)变体的数据。不同变异型导致不同的ARDS严重程度。COVID-19对ARDS后肺恢复的确切影响尚不清楚,但Hodgson等最近的研究表明,将COVID-19幸存者与非COVID-19 ARDS幸存者进行比较,在新发6个月的残疾、生活质量、神经认知或精神功能方面没有显著差异。
这项研究受到样本量相对较小以及数据缺失的限制,特别是与外部住院治疗以及神经认知和精神病学数据有关的一些细节。鉴于ARDS的高死亡率和对后续ICU康复诊所的巨大损失,ARDS幸存者的数量有限。
结论
在11例能够来到ICU随访门诊的当代ARDS患者的样本中,在比较接受ECMO治疗的ARDS幸存者与未接受ECMO治疗的患者时,我们没有发现肺功能、神经认知和心理恢复没有明显差异。
虽然这项研究的结果是接受ECMO治疗的ARDS幸存者与未接受ECMO治疗的患者时,没有发现肺功能、神经认知和心理恢复没有明显差异,但是也许是这种没有差异才会让医务人员在医疗过程中不会受到约束和限制,才能更好为患者提供医疗服务。
而ECMO作为一种救命神奇,但它一种高成本、高耗材、高技术的医疗资源,目前也就在部分三级医疗机构开展,这也就导致很多病人错过最佳治疗时机,希望随着医疗技术的成熟,ECMO可以在更多的基层医院落地生根。同样,他的高价格让很多普通家庭和患者望而却步,希望随着国家经济的发展,在国家和政府的支持下,可以给更多小城市的重症患者多一份生的希望。
可贺的是在2023年初,中国已有两台ECMO成功上市,虽然他可能离真正走进医院为患者提供服务还需要一段时间,但道虽远,行则将至;事虽难,做则必成。愿中国肺能早日走出一条康庄大道。


