Adv Sci:胡志成/唐冰/朱家源合作开发一种脂质纳米颗粒释放多功能水凝胶促进感染糖尿病伤口愈合
时间:2024-09-28 16:00:45 热度:37.1℃ 作者:网络
糖尿病伤口微环境的持续失衡是导致慢性不愈合的重要原因,表现为活性氧 (ROS) 过量积累与异常愈合之间的恶性循环。通过抑制伤口炎症、氧化应激和细菌感染来调节微环境是治疗糖尿病伤口的关键挑战。
2024年9月23日,中山大学胡志成、唐冰、朱家源共同通讯在Advanced Science 在线发表题为“A ROS-Responsive Lipid Nanoparticles Release Multifunctional Hydrogel Based on Microenvironment Regulation Promotes Infected Diabetic Wound Healing”的研究论文。该研究中,开发了由丝素蛋白甲基丙烯酸酯(SFMA)、改性胶原蛋白III型(rCol3MA)和脂质纳米颗粒(LNP)组成的ROS响应水凝胶。
新设计的水凝胶系统表现出稳定的物理化学性质和优异的生物相容性。此外,抗菌肽(AMP)和葛根素(PUE)的释放在消灭细菌、调节炎症反应和调节血管功能方面表现出显著的功效。这种多功能水凝胶是治疗慢性糖尿病感染伤口的一种简单有效的方法,具有巨大的未来临床应用潜力。

糖尿病的发病率逐年上升,且II型糖尿病患者越来越年轻化。慢性不愈合伤口是糖尿病的常见并发症,会带来重大风险,如住院时间延长、经济负担增加、感染、坏疽、截肢甚至死亡。然而,目前的干预措施并没有带来这些结果的实质性改善。因此,探索更有效的治疗方式来促进糖尿病患者的慢性伤口愈合势在必行。
糖尿病患者的慢性不愈合伤口极易受到细菌感染,导致渗出液和生物膜的形成,阻碍伤口愈合过程。慢性伤口的主要特征是炎症期的停滞,表现为炎症因子失衡、细胞增殖受抑制和血管生成障碍。这些表现破坏了伤口微环境并导致活性氧(ROS)的积累,而ROS的过度积累会加剧异常的愈合途径。因此,通过抑制炎症反应、诱导血管生成和消除细菌感染来改善伤口微环境对于慢性糖尿病伤口的治疗至关重要。然而,目前主要的临床治疗策略仍然依赖于单一靶点的方法,这可能既昂贵又无效。因此,需要一种多功能且高效的治疗方法来解决实际的临床问题。近年来,多功能水凝胶因其抗炎、抗菌、止血、反应刺激和药物递送能力而引起了广泛关注。由于其特定的多孔结构和膨胀特性,水凝胶在伤口愈合应用中具有独特的优势。其优异的渗透性有利于伤口渗出液的吸收、维持湿润环境、控制药物释放,最终促进伤口愈合。因此,开发装载有效药物的多功能水凝胶是慢性糖尿病伤口治疗的研究重点。
炎症期是糖尿病感染伤口的关键时期,早期抑制治疗对于确定伤口愈合率和疤痕形成至关重要。因此,多功能水凝胶的设计应优先考虑早期炎症环境的调节。近年来,抗菌肽(AMPs)因其抗菌、血管生成和免疫调节特性,已成为对抗细菌感染和促进皮肤再生的有前途的治疗剂。中药的免疫调节作用也已被证实。葛根素(PUE)是从葛根根中提取的,是一种具有抗炎、抗氧化和缓解氧化应激特性的传统中药。它已被用于治疗心肌梗塞、高血压和糖尿病。此外,PUE具有伤口愈合活性,用PUE配制的水凝胶已证明对皮肤伤口有治疗作用。基于生物材料的治疗策略提供了一种有前途的方法来调节活性药物的时空输送,从而减轻副作用、增强药效并减少所需剂量的频率和数量。这些特性最终提高了组织再生的治疗效果。考虑到糖尿病伤口微环境中ROS水平持续升高,设计一种对ROS敏感的药物运输和释放载体可以进一步提高药物利用率和治疗效果。
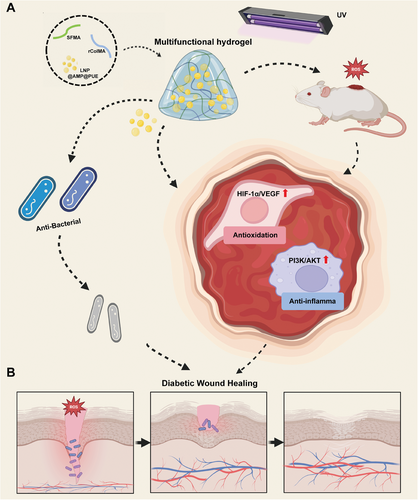
示意图(图源自Advanced Science )
建立一种能适应多种特性并能缓释的药物递送系统,改善伤口微环境,促进糖尿病伤口愈合,具有十分重要的意义。脂质体是一种由双层结构组成的纳米载体,具有制备简便、用途广泛、生物相容性高、可生物降解等特点,由于脂质体独特的结构,可以同时包裹亲水和疏水分子。苯基硼酸(PBA)是一类疏水性小分子化合物,由于其形成硼酸酯键,对ROS高度敏感。在低浓度的过氧化氢中,ROS可以作为亲核试剂与PBA选择性配位。在高浓度ROS的酸性环境中,基于硼酸酯键的载体可能会降解,从而实现药物的智能释放。因此,PBA可用于构建ROS响应递送系统。葡聚糖(DEX)是一种亲水性的天然多糖,由于其优异的生物相容性和生物降解性,在货物运输、医疗植入物、伤口敷料和组织工程等领域有着广泛的应用。通过将4-(羟甲基)-苯基硼酸哌哪醇酯(PBAP)通过羰基二咪唑(CDI)反应偶联到亲水性DEX侧链上,可以通过亲水和疏水自组装制备ROS响应性脂质体。脂质体在暴露于ROS后可以迅速崩解并溶解在水中,从而促进药物释放。
选择合适的水凝胶材料也很重要。III型胶原蛋白是一种细胞外基质蛋白,赋予皮肤弹性和结构支撑。由于其高生物活性,III型胶原蛋白在化妆品、伤口愈合和人造血管研究等生物医学领域越来越受欢迎。III型胶原蛋白可以调节I型胶原蛋白的产生,从而加速纤维化过程并调节其结构和功能特性。生物技术的应用使得能够创建能够有效缓解免疫反应的类似蛋白质和肽成为可能。然而,重组III型胶原蛋白(rCol3)的生产依赖于转基因微生物,这些微生物产生的产品具有与人类胶原蛋白更相似的分子结构和性质,使其适合大规模生产。为了获得可光聚合的材料,可以利用甲基丙烯酸酐(MA)对胶原蛋白进行化学改性,从而形成甲基丙烯酸化胶原蛋白(ColMA)。此外,丝素蛋白(SF)是生物医学领域广泛使用的材料,具有良好的生物相容性、可降解性和高拉伸强度等优点。用甘油甲基丙烯酸酯(GMA)改性SF形成的丝素蛋白甘油甲基丙烯酸酯(SFMA)可提高水凝胶的稳定性和光交联度。基于这些各自的优势特征,可以构建理想的水凝胶平台。
在本研究中,作者开发了一种新型多功能水凝胶,通过结合载有两种不同药物(AMP和PUE)的脂质纳米颗粒(LNPs)来加速糖尿病伤口愈合,从而在ROS微环境中实现持续药物释放,发挥抗菌、抗炎和促血管生成作用(图1)。作者表征了多功能水凝胶的物理和化学性质,并评估了其在体外和体内修复伤口的能力。本研究中提供的所有数据表明,SFMA/rColMA/LNP/@AMP@PUE水凝胶是一种很有前途的敷料,可促进慢性糖尿病伤口修复。
参考消息:
https://onlinelibrary.wiley.com/doi/10.1002/advs.202403219


