【JAMA】重磅综述:CAR-T和T细胞疗法治疗肿瘤的当前证据
时间:2024-11-08 19:00:38 热度:37.1℃ 作者:网络
细胞疗法
嵌合抗原受体CAR-T细胞是经基因工程改造的 T 淋巴细胞,可表达识别肿瘤细胞表面抗原的受体,并导致 T 细胞杀死肿瘤细胞。美国食品药品监督管理局 (FDA) 已经批准6种 CAR-T 细胞产品用于治疗6种血液系统恶性肿瘤:B细胞急性淋巴细胞白血病、大 B 细胞淋巴瘤、滤泡性淋巴瘤、套细胞淋巴瘤、慢性淋巴细胞白血病和多发性骨髓瘤。与标准化疗序贯干细胞移植相比,CAR-T细胞改善了大 B 细胞淋巴瘤患者的4年总生存率 (54.6% vs 46.0%)。儿童急性淋巴细胞白血病患者经 CAR-T 细胞治疗后可获得持久缓解,3年随访时48%的患者存活且无复发。在既往接受过1-4线非 CAR-T 细胞治疗的多发性骨髓瘤患者中,与标准治疗相比,CAR-T细胞治疗延长无治疗缓解时间(在1项研究中,CAR-T细胞治疗的无进展生存期为13.3个月,而标准治疗为4.4个月)。CAR-T细胞疗法可导致可逆性急性毒性,例如约40%-95%的患者出现细胞因子释放综合征,约15%-65%的患者出现神经系统疾病。正在开发的新型 CAR-T 细胞疗法旨在增加疗效、减少不良反应和治疗其他类型的肿瘤。
FDA尚未批准 CAR-T 细胞用于实体瘤,但近期另外2种基于T淋巴细胞的疗法获得批准:1种用于黑色素瘤,1种用于滑膜细胞肉瘤。其他细胞治疗也已在某些实体瘤中获得良好反应,包括儿童神经母细胞瘤、滑膜细胞肉瘤、黑色素瘤和人乳头瘤病毒相关肿瘤。
顶级期刊JAMA近日发表综述,阐述了肿瘤细胞免疫治疗的当前证据。现整理翻译供参考,部分附图来自其他综述,都备注了出处。

细胞免疫治疗基于免疫细胞,可识别和杀死恶性肿瘤细胞,被称为活药(living drugs)。CAR-T细胞由经基因工程改造的 T 细胞组成,可表达识别肿瘤细胞表面蛋白的非合成受体。肿瘤浸润淋巴细胞 (TIL) 是切除肿瘤离体生长的天然 T 细胞。T细胞受体 (TCR)T 细胞是一种表达天然 TCR 的基因工程 T 细胞,可重组细胞内蛋白(见图A-D和BOX)。
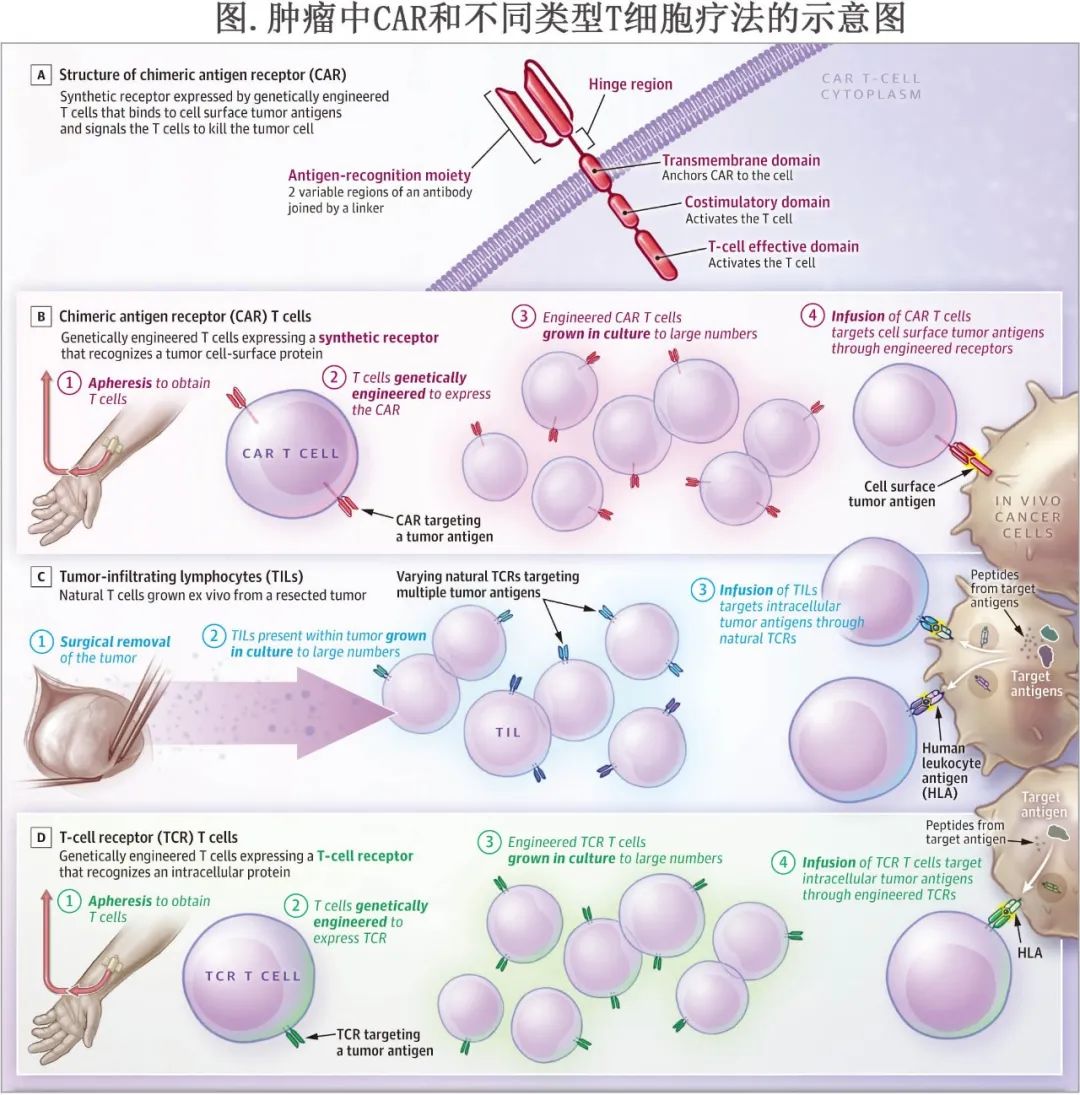
A、CAR的结构一般包括胞外抗原识别部分,通常由单克隆抗体的2个可变区(轻链和重链)组成,通过连接子连接。铰链和跨膜结构域连接抗原识别部分和细胞内组分。胞内共刺激结构域(通常为CD28或4-1BB)和T细胞活化结构域(通常为CD3ζ)可激活T细胞。
B、CAR-T细胞与TCR T细胞使用相同类型的基因工程流程制备。与TCR T细胞一样,它们具有确定的抗原特异性,最常靶向单一抗原。CAR与TCR的不同之处在于它们是单链嵌合蛋白,具有结合靶抗原和激活T细胞的独立能力。由于其抗体样抗原识别,CAR可靶向细胞表面抗原,一般无法靶向胞内抗原(例如大多数癌蛋白、突变基因产物和肿瘤胚系抗原等)。但CAR的优点在于,与 TCR不同的是,其靶标识别不需要特定的HLA分子,从而拓宽了可以接受特定疗法治疗的患者数量。
C、TIL是手术切除的新鲜肿瘤标本在实验室中生长的自体T细胞。该方法需要手术来获得肿瘤标本,一般需要数周才能长出细胞进行治疗。与CAR和TCR T细胞不同,TIL并非通过基因工程表达抗原受体。TIL细胞产物具有高度变异性;它们可能靶向任何数量的肿瘤抗原,也可能不靶向任何肿瘤抗原。TIL细胞产物中的T细胞通过其天然TCR与肿瘤细胞结合,TCR与HLA分子复合的肽结合。
D、TCR T细胞疗法利用基因工程改造的T细胞表达TCR并靶向肿瘤相关抗原。用于基因工程的T细胞是从通过单采程序(从血液中去除T细胞的方法)获得的外周血单核细胞中分离得到的。基因工程可以使用各种技术来完成,包括病毒载体、转座子或CRISPR-Cas9。TCR基因工程涉及TCRα-和β-链的转移。这些链与内源性 CD3分子(γ、δ、ε和ζ链)形成复合物,提供信号传导功能。工程化TCR T细胞与TIL T细胞一样,通过TCR与靶肽-HLA复合物结合。靶标复合物中的HLA分子必须与患者单倍型中的HLA分子匹配(例如,如果治疗性TCR靶向HLA-a*01:01呈递的肽,则患者必须具有HLA-a*01:01等位基因)。TCR T细胞与TIL T细胞不同,它们具有确定的特异性,多用于单靶点抗原。
BOX.关于肿瘤细胞治疗的常见问题
什么是CAR-T细胞疗法?
CAR-T 细胞是经基因工程改造的 T 淋巴细胞,表达可识别肿瘤细胞表面抗原的合成受体,使T细胞杀死肿瘤细胞。
CAR-T细胞疗法可以治疗哪些血液系统肿瘤?
目前美国FDA)批准的 CAR-T 细胞治疗适应症包括 B 细胞急性淋巴细胞白血病、大 B 细胞淋巴瘤、滤泡性淋巴瘤、套细胞淋巴瘤、慢性淋巴细胞白血病和多发性骨髓瘤。
实体瘤是否有可用的细胞疗法?
FDA 批准肿瘤浸润淋巴细胞 (TIL) 疗法 lifileucel 用于晚期黑色素瘤,批准 T 细胞受体 (TCR)T 细胞疗法 afamitresgene autoleucel 用于晚期滑膜肉瘤。FDA未批准其他细胞疗法用于实体瘤。
肿瘤细胞疗法的不良反应有哪些?
CAR-T 细胞疗法可引起细胞因子释放综合征,一种以发热、心动过速、低血压和缺氧为特征的炎性综合征,以及免疫效应细胞相关神经毒性综合征,一种以多种症状为特征的神经系统疾病,包括脑病、言语困难和警觉性降低。TIL和TCR T细胞治疗因与大剂量白细胞介素-2联合给药,可引起发热和毛细血管渗漏综合征。
细胞疗法和获批的CAR-T细胞疗法简介
CAR 蛋白是一种由基因工程 T 细胞表达的合成受体,可与肿瘤细胞上的细胞外恶性肿瘤相关抗原结合,从而向 T 细胞发出信号并杀死肿瘤细胞(图A)。CAR由2个主要组分组成:(1) 胞外抗原识别部分,通常来源于抗体的可变区,(2) 激活T细胞的胞内 T 细胞衍生组分,通常为CD3ζ T细胞活化结构域和共刺激结构域,通常为 CD28 或4-1BB(图A)。自体 T 细胞一般通过病毒载体进行永久性基因修饰,在细胞表面表达 CAR 蛋白(图B)。通常需要在CAR、TCR和 TIL T 细胞输注前给予化疗,如环磷酰胺和氟达拉滨,以耗竭可能抑制或与治疗细胞竞争的其他细胞,如 T 调节细胞或髓源性抑制细胞,并增加细胞因子的血清水平,如白细胞介素 (IL)7 和IL-15,其可增强 CAR-T 细胞活性;部分 TIL 和 TCR T 细胞治疗后给予大剂量 IL-2 输注可增强体内 T 细胞增殖。TIL 和 TCR T 细胞治疗的副作用包括预处理方案引起的骨髓抑制、细胞和大剂量 IL-2 的引起发热以及 IL-2 引起的毛细血管渗漏综合征,主要表现为液体潴留、肺水肿和肾功能不全。
目前,美国FDA已批准6种 CAR-T 细胞疗法并上市(表1)。CAR-T细胞产品由表达的CAR蛋白的结构、介导基因转移的病毒载体和细胞培养过程的要素来定义。
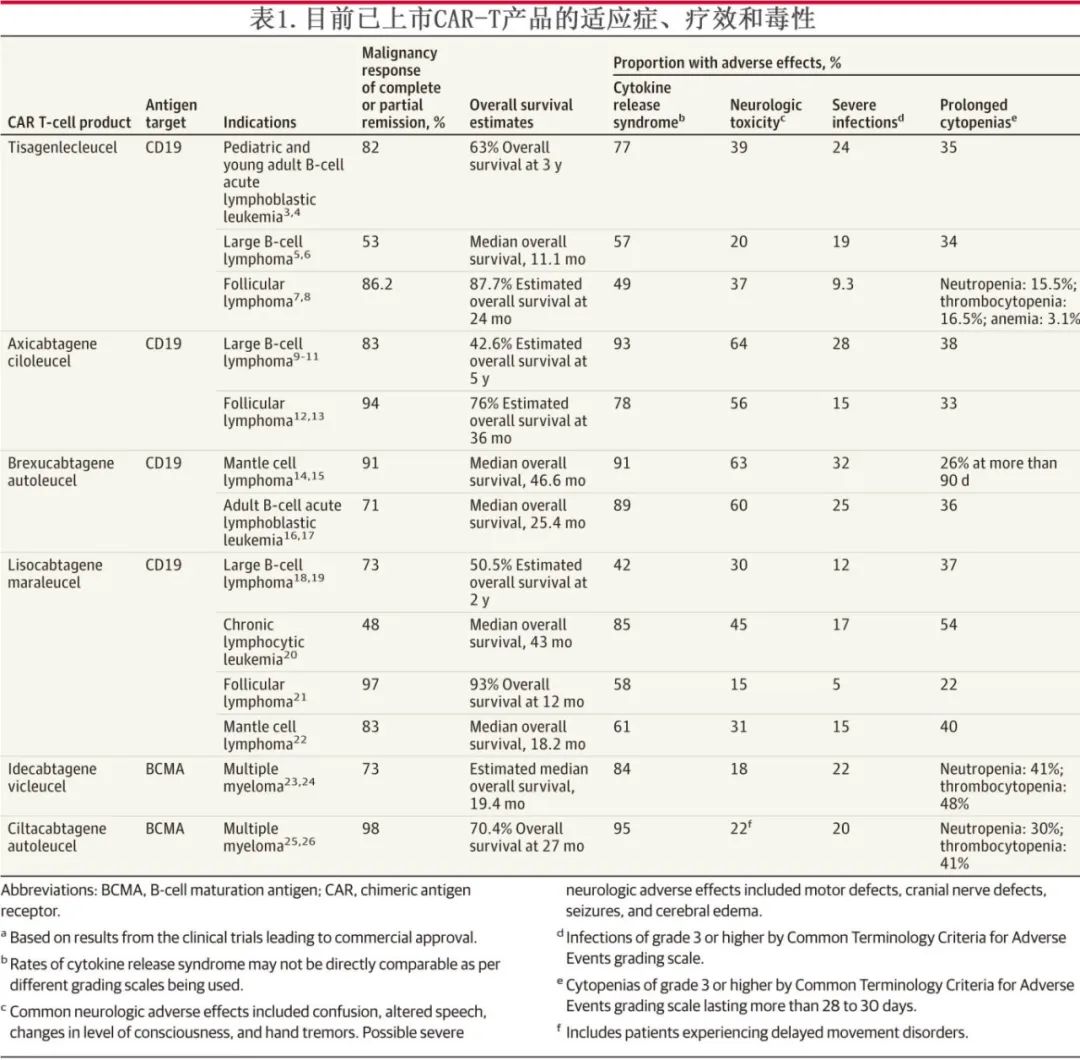
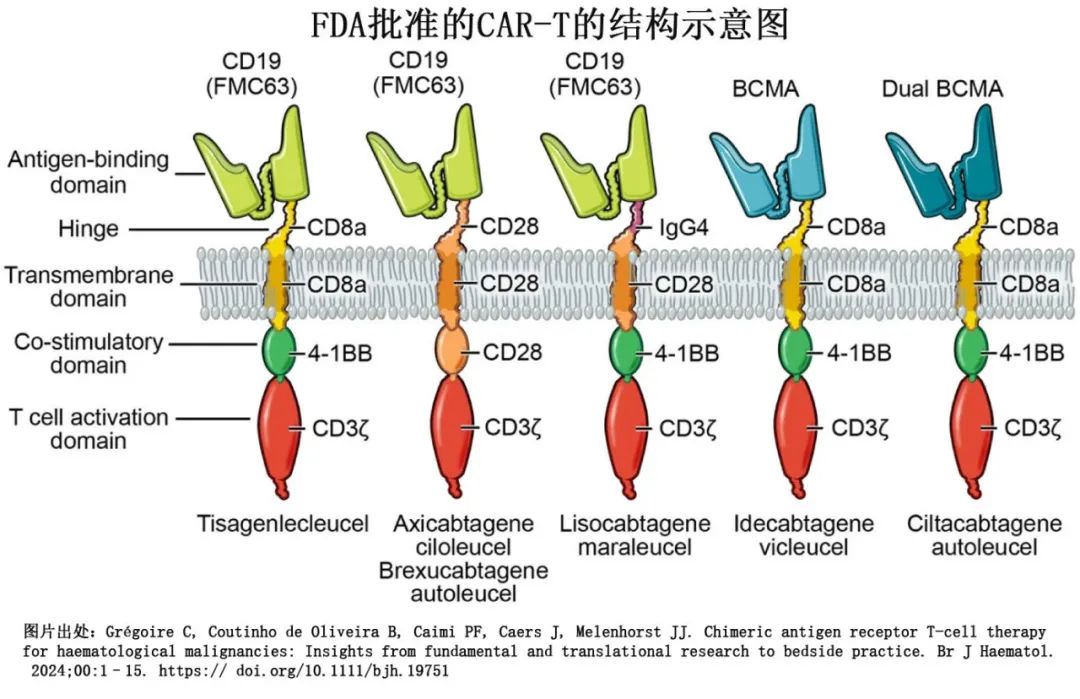
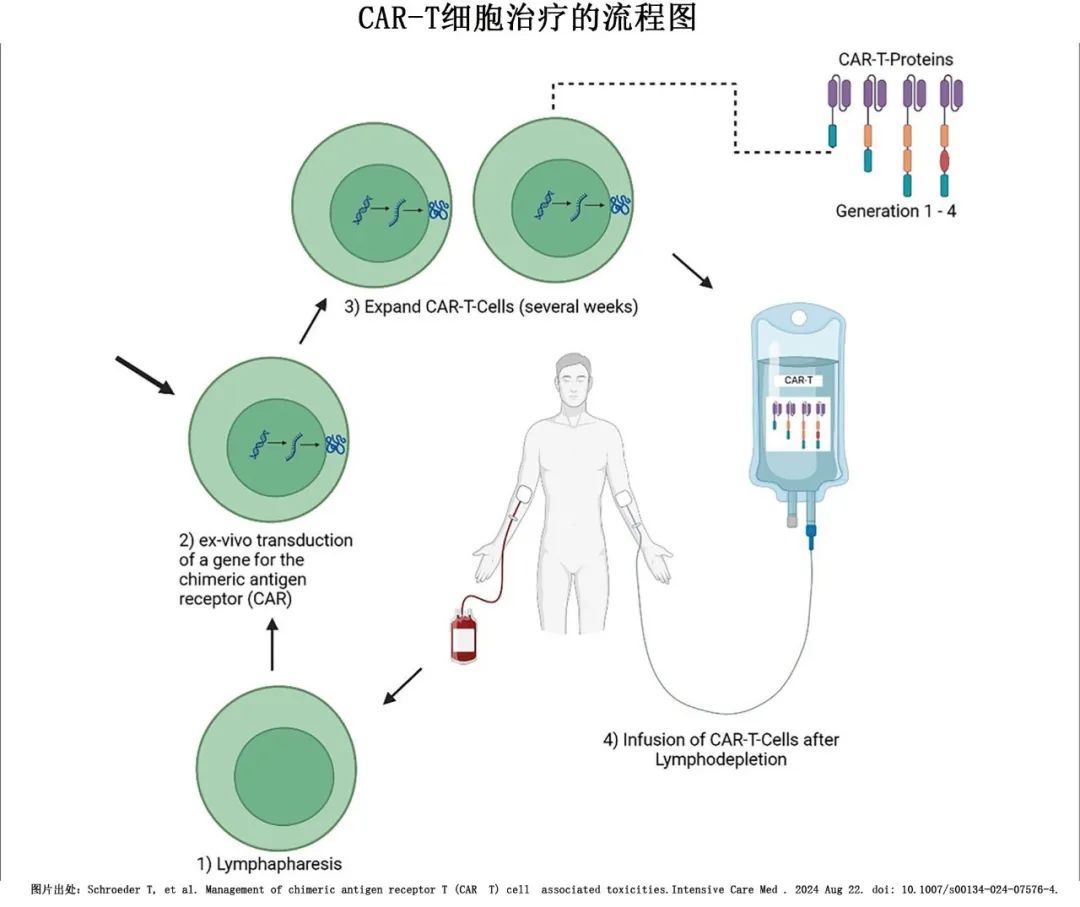
一般CAR-T 细胞产品通常有2个单词的名称:第一个表示基因组分,第二个表示细胞组分。第一个单词中的cabta 表示“细胞表达的抗体和 T 细胞活化”;来源于患者的自体 CAR-T 细胞产品名称通常有2个单词,第二个单词以 auto 开头,第二个单词cel作为结尾表示产品是一种细胞药物。Tislecagenleucel、axicabtagene ciloleucel、brexucabtagene autoleu-cel和lisocabtagene maraleucel都是经基因工程改造的细胞药物,可识别 B 细胞抗原CD19,并治疗特定B 细胞非霍奇金淋巴瘤、B细胞急性淋巴细胞白血病和慢性淋巴细胞白血病。Idecabtagene vicleucel和 ciltacabtagene autoleucel 靶向浆细胞相关蛋白 B 细胞成熟抗原 (BCMA) 并治疗多发性骨髓瘤。
Tisagen-lecleucel是首个市售细胞免疫疗法,于2017年获得 FDA 批准,用于25岁及以下的儿童和年轻成人 B 细胞急性淋巴细胞白血病。在急性淋巴细胞白血病患者的2期临床试验中,Tislecagenleucel 的缓解率为82%,3年随访期间的无复发生存率为48%。一项回顾性分析纳入511例患者,将 tisagenlecleucel 与标准治疗进行了比较,发现 tisagenlecleucel 显著改善2年总生存率 (59.5% vs 36.2%)。
在101例既往接受过治疗的大 B 细胞淋巴瘤患者中,axicabtagene ciloleucel治疗后的完全缓解率为54%,5年生存率为43%,而接受标准治疗的大 B 细胞淋巴瘤患者历史对照中2年总生存率为20%。axicabtagene ciloleucel和lisocabtagene maraleucel治疗首次标准化疗方案无应答或在初始缓解后12个月内进展的大 B 细胞淋巴瘤患者的随机临床试验数据表明,与二线化疗后自体干细胞移植的标准治疗相比,axicabtagene ciloleucel的无进展生存期更优,axicabtagene ciloleucel的总生存期更优。CD19 CAR-T 细胞治疗有可能治愈既往治疗无效的B 细胞恶性肿瘤患者。滤泡性淋巴瘤和套细胞淋巴瘤患者在 CAR-T 细胞治疗后也可获得长期缓解,axicabtagene ciloleucel和 Tislecagenleucel 治疗滤泡性淋巴瘤的2年无进展生存率分别为63%和57%,brexucabtagene autoleucel和 lisocabtagene maraleu-cel 治疗套细胞淋巴瘤的12个月无进展生存率分别为61%和53%。然而,CAR-T细胞治疗能否治愈这些恶性肿瘤仍不清楚。
在既往接受过6线治疗的多发性骨髓瘤患者中,idecabtagene vicleucel的缓解率为73%,ciltacabtagene autoleucel的缓解率为98%,中位无进展生存期分别为8.8个月和27个月。两项随机临床试验比较idecabtagene vicleucel或ciltacabtagene autoleu-cel与标准方案治疗对既往接受过1-4线治疗的多发性骨髓瘤,结果表明 CAR-T 细胞治疗的无进展生存期更优:与标准治疗的4.4个月相比,idecabtagene vicleucel的中位无进展生存期为13.3个月;在419例随机分配的来那度胺难治性多发性骨髓瘤患者中,ciltacabtagene autoleucel组的12个月无进展生存率为75.9%,而标准治疗组为48.6%。此外研究显示,21%的临床试验患者在 ciltacabtagene autoleucel 后的无进展生存期达到≥5年。目前尚不清楚这些 CAR-T 细胞疗法能否治愈多发性骨髓瘤。
与细胞疗法相关的挑战
血液系统肿瘤
CAR-T 细胞疗法治疗恶性血液病面临的挑战包括急性和长期不良反应、疗效和持久性有限、缺乏有效的挽救治疗、CAR-T细胞疗法等待时间长和可及性有限(表2)。

不良反应
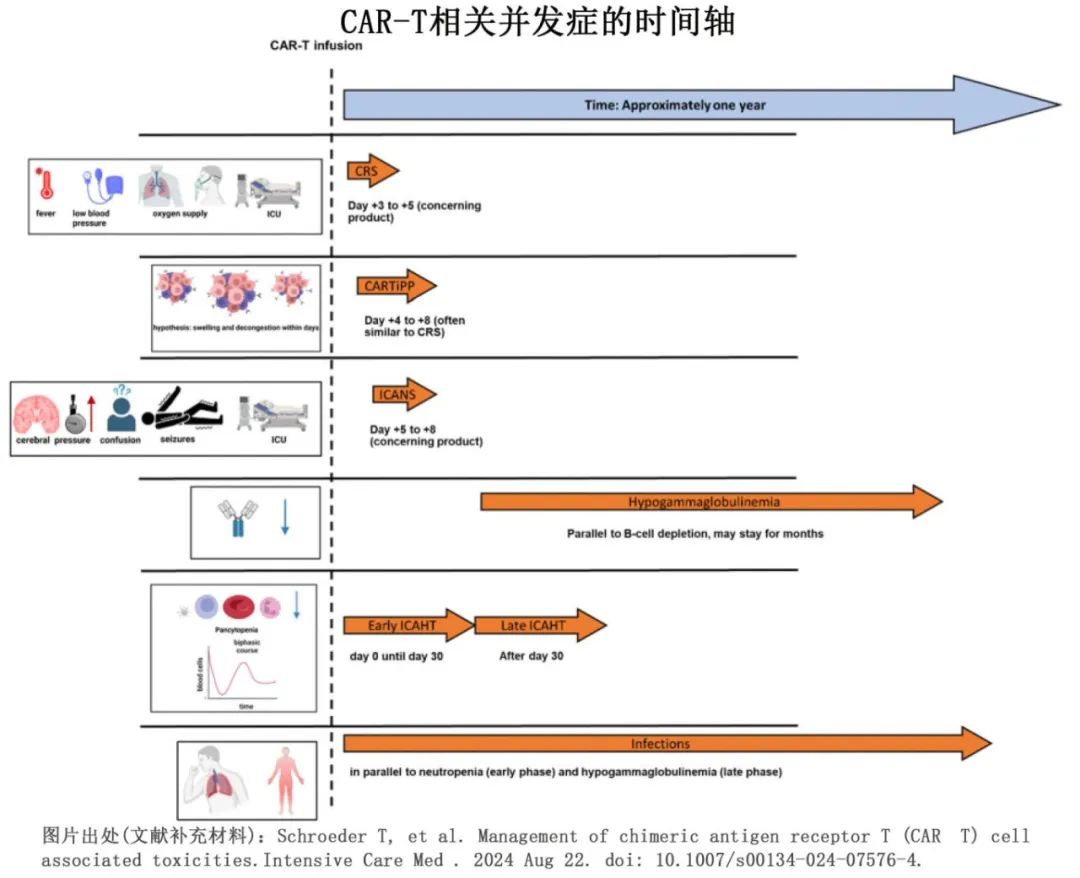
当用于治疗B细胞恶性肿瘤时,CD19 CAR-T细胞在受者体内的增殖通常高达1000倍,可升高多种细胞因子(如IL-6和干扰素-γ)和其他免疫蛋白的水平。这些升高的循环促炎物质可引起细胞因子释放综合征,表现为发热、低血压和凝血障碍,并可能危及生命。细胞因子释放综合征可通过在出现症状后给予托珠单抗来减轻,托珠单抗可阻断IL-6受体。糖皮质激素(如地塞米松)每6~12h给予10mg(相当于泼尼松66.7mg)可作为二线药物治疗细胞因子释放综合征,直至毒性降低。累积地塞米松等效剂量超过1000mg(泼尼松剂量>6600mg)已用于重度、难治性细胞因子释放综合征或神经毒性。CAR-T细胞可穿过血脑屏障,引起可逆性神经综合征,包括脑病、言语困难、警觉性降低、震颤以及更严重形式的局灶性运动缺陷、癫痫发作和脑水肿,这种神经毒性称为免疫效应细胞相关神经毒性综合征,糖皮质激素是其一线治疗。美国移植和细胞治疗学会委员会制定了共识分级量表,多个专业协会也发布了细胞因子释放综合征和免疫效应细胞相关神经毒性综合征管理指南。BCMA CAR-T 细胞治疗后数周至数月可能发生运动障碍,但目前仍知之甚少。由于管理细胞因子释放综合征和神经毒性需要专业技能,因此目前优先在有经验的三级医疗中心给予 CAR-T 细胞治疗,在临床试验中,仅9%-24%的CAR-T 细胞输注允许在门诊。
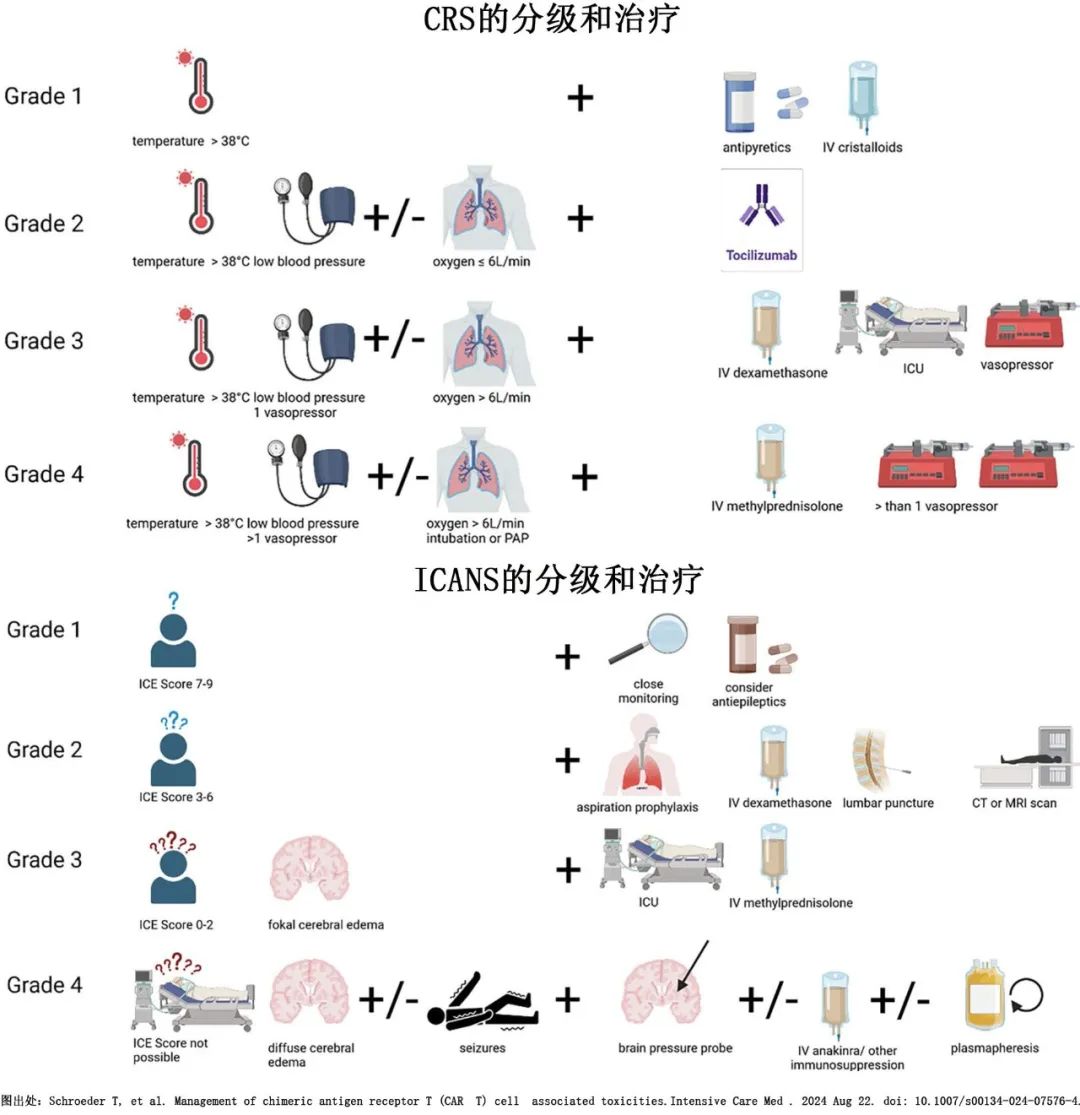
虽然细胞因子释放综合征可通过托珠单抗治疗,必要时再使用糖皮质激素治疗,而免疫效应细胞相关神经毒性综合征可通过增加糖皮质激素的剂量来控制,但大剂量累积糖皮质激素可能对 CAR-T 细胞功能产生不利影响,与无进展生存期和总生存期较差相关。但在一项纳入726例接受 CAR-T 细胞治疗的患者的英国回顾性分析中,随着早期使用托珠单抗和糖皮质激素治疗毒性,总生存率有所改善,高级别细胞因子释放综合征的发生率从约9%降至4%。在市售产品的临床试验中报告的治疗相关死亡率约为0%-6%。
CAR-T 细胞治疗的长期不良反应包括长期骨髓抑制(定义为高级别中性粒细胞减少症、贫血或血小板减少症持续超过28-30天,发生率约22%-54%)和免疫抑制(可能导致临床试验中5%-32%的患者发生重度感染)(表1)。CAR-T细胞输注后持续1个月以上的血细胞减少被认为是由升高的细胞因子所介导,但机制尚不明确。CD19 CAR-T 细胞(如 Tislecagenleucel 或axi-cabtagene ciloleucel)可消除正常表达 CD19 的 B 细胞,导致 B 细胞完全耗竭,称为 B 细胞再生障碍(aplasia)。B细胞再生障碍为on-target toxicity毒性,因为破坏的正常细胞所表达的抗原与 CAR-T 细胞靶向恶性肿瘤细胞的抗原是相同的。B细胞再生障碍和由此导致的低丙种球蛋白血症可以用免疫球蛋白替代治疗,但成人在 CD19 CAR-T 细胞治疗后可能不需要这些治疗,因其成熟浆细胞(不表达CD19)可以保留。由于 B 细胞再生障碍、CD4淋巴细胞减少和长期血细胞减少,患者在 CAR-T 细胞治疗后发生感染的风险较高,包括 SARS-CoV-2 引起的重度感染。细菌感染最常发生于CD19 CAR-T 细胞输注后一个月内。CAR-T细胞治疗1年后也可能发生病毒感染,尤其是呼吸道病毒感染。约8%的患者发生侵袭性真菌感染。念珠菌感染最常发生在治疗后的第一个月。曲霉菌和其他霉菌感染最常发生在治疗后的前90天内。
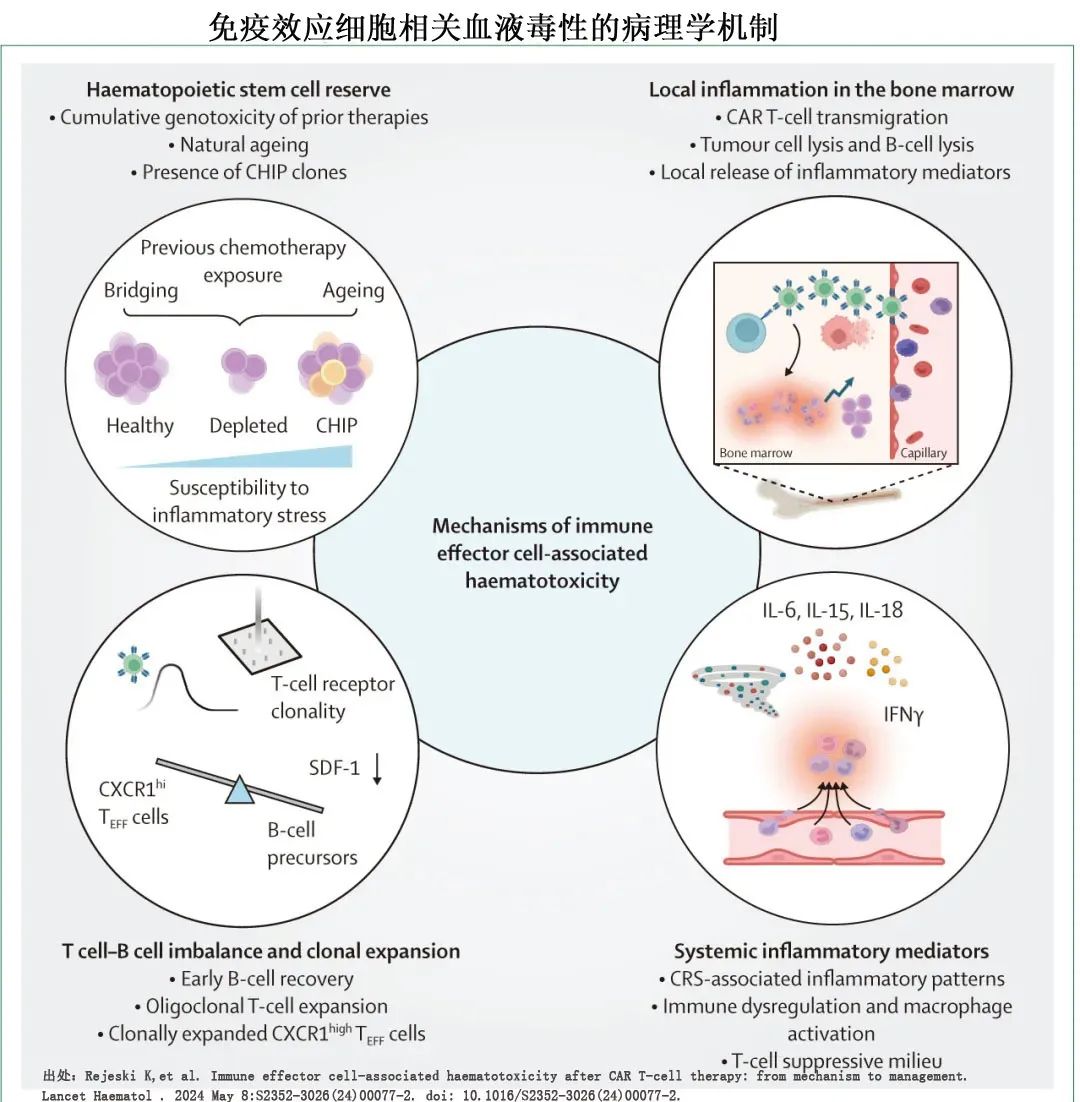
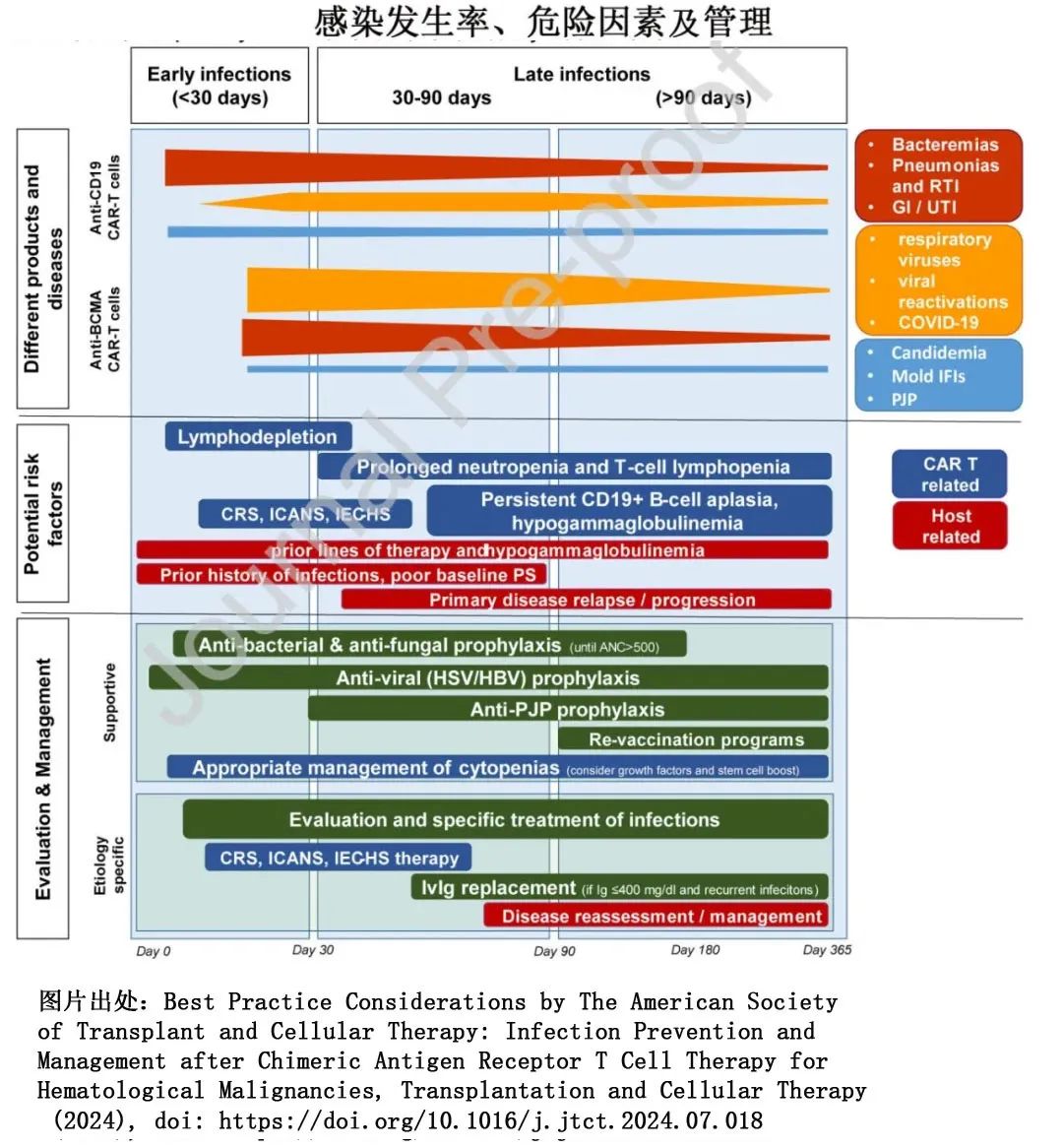
第二髓系恶性肿瘤(如急性髓性白血病和骨髓增生异常综合征)在CAR-T细胞输注后5年内发生率约为2%至10%。由于既往化疗的致突变性,包括在CAR-T细胞输注前立即接受的潜在化疗,患者已处于发生第二髓系恶性肿瘤的风险中。2023年12月,FDA批准了ciltacabtagene autoleucel说明书的最新黑框警告,称在接受CAR-T细胞产品治疗的患者中报告了第二血液系统恶性肿瘤,包括急性髓性白血病和骨髓增生异常综合征,在一项临床试验中,共有10%(10/97)的患者后续发生第二恶性肿瘤。然而这些患者接受过许多其他治疗,包括CAR-T细胞输注后的治疗,因此CAR-T细胞治疗是否会引起第二髓系恶性肿瘤仍不清楚。
CAR-T 细胞在引起 T 细胞恶性肿瘤中的作用仍在研究,在超过27000次治疗中至少报告了22例,包括3例表达 CAR 蛋白的 T 细胞恶性肿瘤。该结果引起了对基因工程过程可能导致 CAR-T 细胞恶变的关注,因为在控制 T 细胞生长的基因区域近端插入 CAR 基因的病毒可能通过插入突变过程引起恶性肿瘤。然而鉴于数千例患者因危及生命的血液恶性肿瘤而接受 CAR-T 细胞治疗,且这些事件较为罕见,CAR-T细胞治疗的获益是大于风险的。
疗效
即使对于潜在可治愈的恶性肿瘤,如大 B 细胞淋巴瘤和 B 细胞急性淋巴细胞白血病,许多患者经 CAR-T 细胞治疗也无法获得持久缓解。在使用 axicabtagene ciloleucel 治疗大 B 细胞淋巴瘤后,63%达到部分或完全缓解的患者出现复发、难治性恶性肿瘤或死亡,在使用 tisagenlecleucel 治疗 B 细胞急性淋巴细胞白血病后,缓解的患者中36%复发。复发的机制之一为恶性肿瘤进展,使其不再表达 CAR-T 细胞靶向的抗原、表达抗原的强度较低或以 CAR-T 细胞无法识别的改变形式表达抗原;该现象称为抗原逃逸,发生率:tisagenlecleucel治疗急性B细胞淋巴细胞白血病中约91%、axicabtagene ciloleucel 治疗大 B 细胞淋巴瘤中28%和 idecabtagene vicleucel 治疗多发性骨髓瘤中4%(表2)。CAR-T细胞治疗疗效较低的另一种机制是因为白细胞单采采集的自体 T 细胞质量较差,可导致生产的 CAR-T 细胞质量较差。未成熟 T 细胞(输注后保留更多的增殖能力)数量更多与更高的治疗缓解率和更持久的缓解相关。T细胞采集时T 细胞质量较差或功能较差的原因尚不完全清楚。既往接受过更多肿瘤治疗方案的患者发生T 细胞功能低下的风险更高,这些患者在回顾性研究中显示缓解率较低。对 CAR-T 细胞治疗耐药与预后较差相关。一项纳入550例大 B 细胞淋巴瘤患者的法国登记组分析显示,CD19 CAR-T 细胞治疗后未缓解或复发的患者的中位总生存期仅5.2个月。
治疗实施的挑战
对于已上市的 CAR-T 细胞产品,患者细胞白细胞单采和 CAR-T 细胞输注之间的等待时间(称为静脉-静脉时间)约为13-54天(表2)。在临床试验和已批准的 CAR-T 细胞疗法的商业化使用期间,0%-31%的患者由于细胞制备失败或恶性肿瘤进展(较常见,与等待期间临床状态恶化相关)而未接受 CAR-T 细胞输注。CAR-T细胞疗法花费也是治疗的重要障碍。
实体瘤
CAR-T 细胞治疗实体瘤的疗效有限,但已在某些肿瘤中观察到反应,此外其他类型的基于 T 淋巴细胞的治疗已获得 FDA 批准。在实验室研究中,将肿瘤植入小鼠以模拟肿瘤治疗,从而确定了影响疗效的 T 细胞相关因素,例如:CAR-T 细胞迁移至肿瘤、增殖并在患者体内存活的能力;克服抑制性因素,如充斥肿瘤微环境的转化生长因子β;维持其抗肿瘤功能。尚不清楚这些机制中的哪种(如有)限制人体的治疗疗效。细胞治疗和其他免疫疗法的主要限制可能是由于肿瘤细胞内在因素,如靶抗原表达、抗原呈递和对 T 细胞效应分子的敏感性。识别和靶向“干净”靶点(即癌细胞中可靶向且无重度毒性的分子结构)仍是重大挑战。
改善血液肿瘤的CAR-T细胞疗法
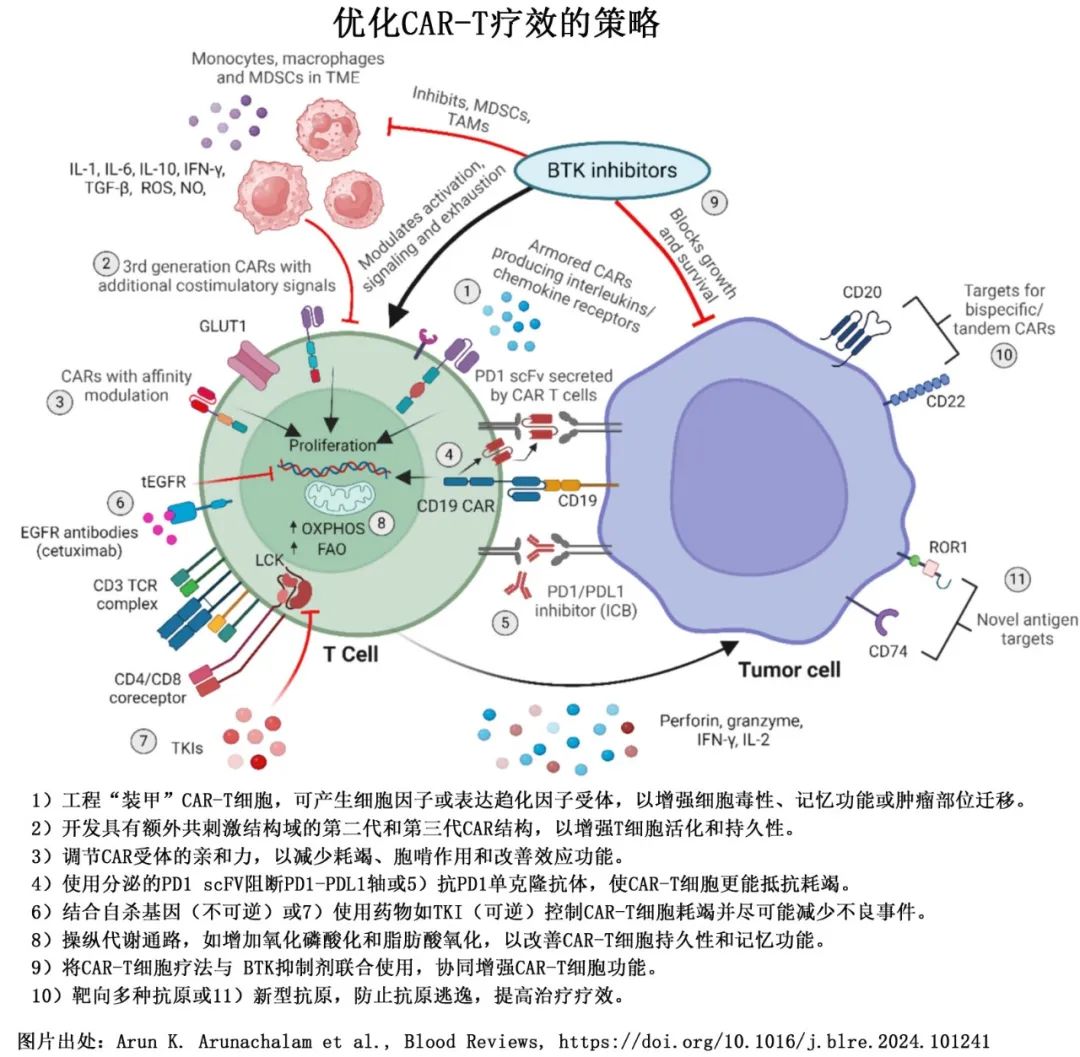
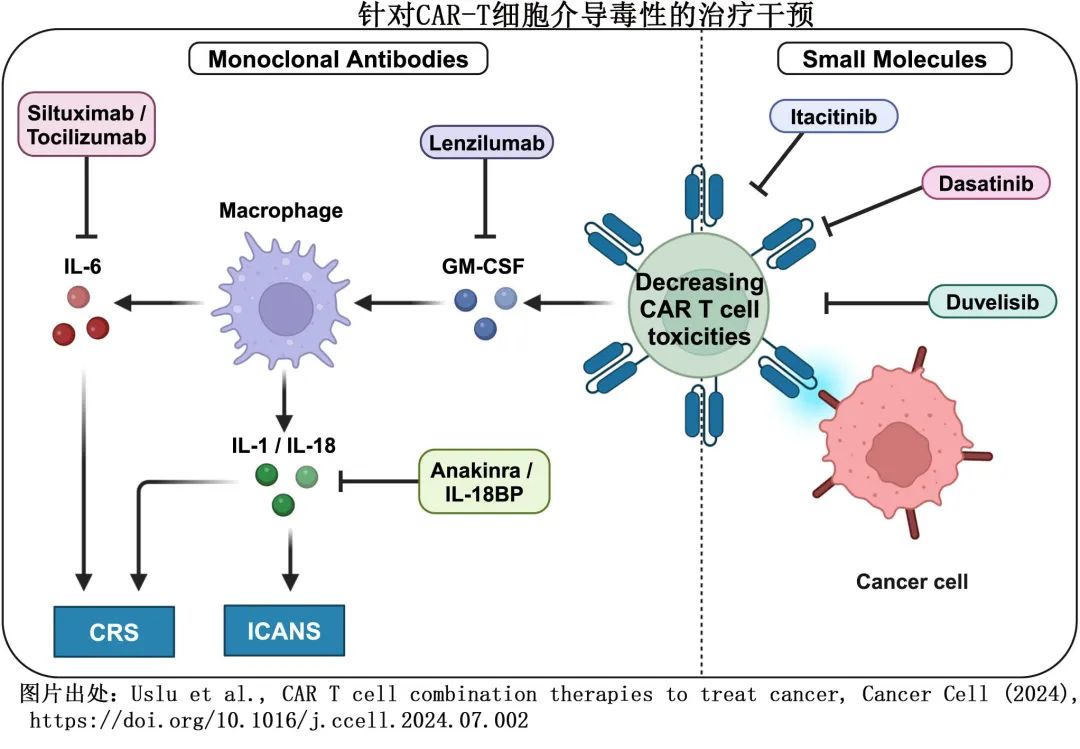
可通过降低毒性、提高疗效和扩大适合 CAR-T 治疗的患者人群来改善 CAR-T 细胞治疗。降低急性 CAR-T 细胞毒性的药物治疗正在不断发展,但尚未确定抗细胞因子治疗(如司妥昔单抗、anakinra或emapalumab)和小分子药物(如伊布替尼、达沙替尼或itacitinib)治疗 CAR-T 细胞毒性的获益。此外也很少有极好的 CAR-T 细胞毒性动物模型。细胞因子释放综合征和免疫效应细胞相关神经毒性综合征小鼠模型表明,阻断IL-1可预防或减少不良反应。小型前瞻性试验表明,预防性使用或早期干预托珠单抗、IL-1受体拮抗剂anakinra或低剂量糖皮质激素可预防重度细胞因子释放综合征和免疫效应细胞相关的神经毒性综合征毒性。抗细胞因子治疗(如 IL-6 拮抗剂司妥昔单抗、anakinra和干扰素-γ阻滞剂emapalumab)已超说明书使用作为糖皮质激素替代药物,并用于治疗对糖皮质激素无反应的毒性;然而这些治疗的推荐原则尚未在随机临床试验中进行研究(表2)。
改变 CAR 的结构可以改变 CAR-T 细胞的毒性特征,通常是通过减少 CAR-T 细胞和患者血液中其他免疫细胞分泌的细胞因子和其他免疫蛋白,而不降低 CAR 细胞的疗效。在临床试验中,通过改变抗原识别部分(图A)与肿瘤相关抗原的结合强度可降低细胞因子释放综合征和/或免疫效应细胞相关神经毒性综合征。降低毒性的其他手段包括:通过改变铰链和跨膜结构域(其链接胞外抗原识别部分与可活化 T 细胞的胞内组分;图A)的序列,以及通过改变CD3ζ T细胞活化结构域的结构(图A)。在临床试验中评价 CAR 结构修饰的 CAR-T 细胞并开发毒性较低的 CAR-T 细胞疗法可能有助于更广泛地使用 CAR-T 细胞疗法(表2)。
提高CAR-T细胞疗法的疗效和持久性
在早期临床试验中,CAR-T细胞增殖最多(称为细胞扩增)的患者的抗肿瘤反应最佳,该发现已在多种恶性肿瘤和多种 CAR-T 细胞产品中得到证实,包括在多发性骨髓瘤中使用的靶向 BCMA 产品。改善 CAR-T 细胞疗效和增加扩增及其体内疗效的潜在策略包括修改细胞培养过程以选择分化程度较低的表型 T 细胞,从而提高抗恶性肿瘤疗效。与BTK抑制剂(如伊布替尼)联合治疗可改善 CAR-T 细胞扩增并促进更有效的 CAR-T 细胞表型,但证据并不一致。CAR-T细胞疗法联合免疫检查点抑制剂,或免疫检查点抑制剂作为 CAR-T 细胞疗法失败或复发的挽救疗法,可改善体内 CAR-T 细胞功能恶化,但临床试验显示疗效较低。
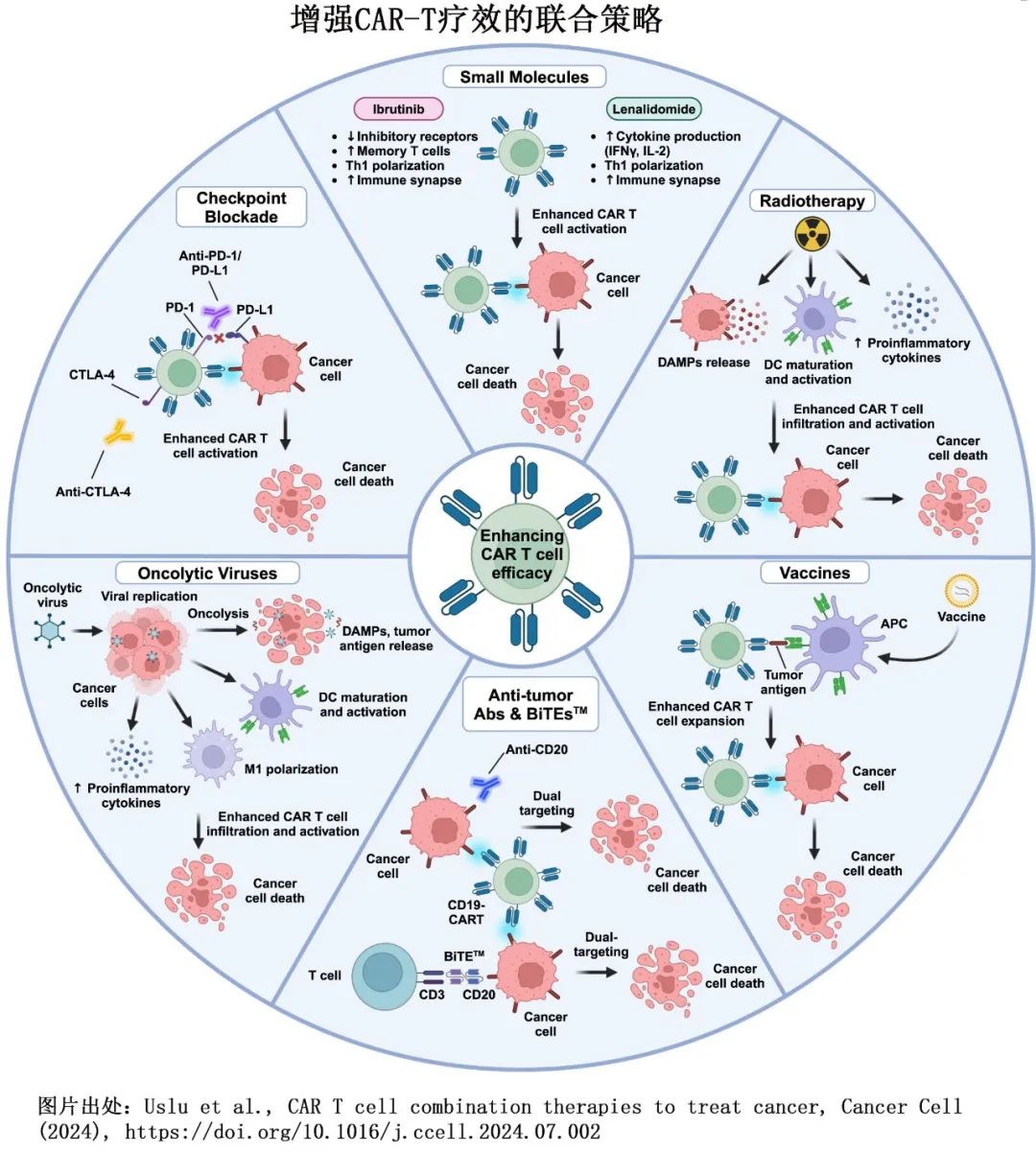
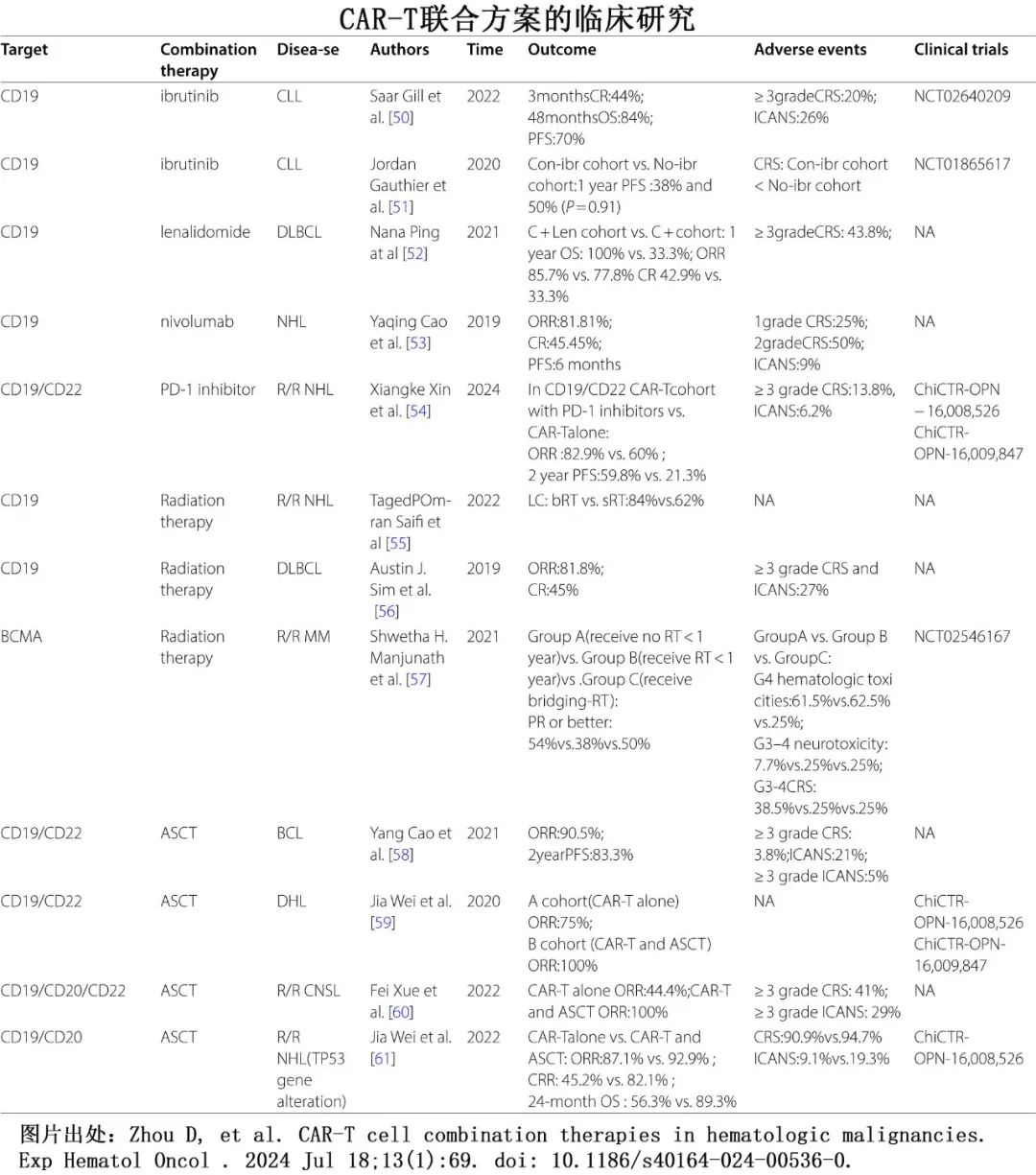
治疗一线CAR-T后抗原逃逸的CAR-T 细胞正在开发中,实例包括靶向 B 细胞抗原 CD22 的 CAR-T 细胞,用于治疗CD19 CAR-T 细胞治疗后不再表达 CD19 的 B 细胞急性淋巴细胞白血病。临床试验中CD22 CAR-T 细胞治疗显示出初步疗效,在一项 I 期剂量递增研究中,既往中位6线治疗的17例多发性骨髓瘤患者接受靶向GPRC5D的 CAR-T 细胞,证实BCMA CAR-T 细胞治疗后复发的患者中具有早期疗效。目前正在进行早期临床试验的淋巴瘤替代抗原 CAR-T 细胞疗法包括 CD79b 和CD37。同时靶向多种抗原以防止抗原逃逸,例如靶向 B细胞淋巴瘤的 CD19 和 CD20 的 CAR-T 细胞,也在进行研究。
市售 CAR-T 细胞疗法已获批作为血液恶性肿瘤的二线或后续疗法(表1)。临床试验正在评价 CAR-T 细胞疗法作为一线疗法,或用于已获批适应症的早线治疗。在使用 axicabtagene ciloleucel 治疗高危大 B 细胞淋巴瘤的 ZUMA-12 临床试验中,40例患者在接受2个周期一线标准化疗未达到缓解后接受 CAR-T 细胞治疗;与评价 axicabtagene ciloleucel 作为三线或后线治疗的 ZUMA-1 试验相比,输注前 CAR-T 细胞分化程度较低、增殖程度较高的 T 细胞比例较高。治疗早期给予 CAR-T 细胞治疗可能会增强 CAR-T 细胞功能,可能是由于 T 细胞先前暴露于较少的细胞损伤性化疗。
目前FDA批准的 CAR-T 细胞产品及晚期试验的CAR-T产品均为自体 T 细胞,但早期试验也研究了从正常健康供者采集并储存至使用的 CAR-T 细胞(称为现货型 CAR-T 细胞)。通常使用基因编辑技术(如转录激活因子样效应核酸酶或成簇的规则间隔的短回文重复序列)去除 T 细胞受体,以预防移植物抗宿主病。由于异基因细胞可能被宿主免疫系统排斥,给予较高剂量的化疗和(某些情况下)输注抗 CD52 单抗可延长 T 细胞耗竭,从而促进供者细胞的扩增。基因编辑技术可删除 T 细胞标志物(如CD52),因此 T 细胞耗竭预处理治疗不会杀死供者来源的 CAR-T 细胞。这些 CAR-T 细胞产品的使用不需要进行供者和受者之间人类白细胞抗原(HLA)配型。抗 CD19 和抗 BCMA 现货型 CAR-T 细胞的早期疗效显示,与市售 CAR-T 细胞相比,细胞采集和 CAR-T 细胞回输之间的时间更短。然而T细胞耗竭预处理会增加 T 细胞耗竭导致的长期免疫抑制率,并增加机会性病毒感染(如巨细胞病毒)的发生率。
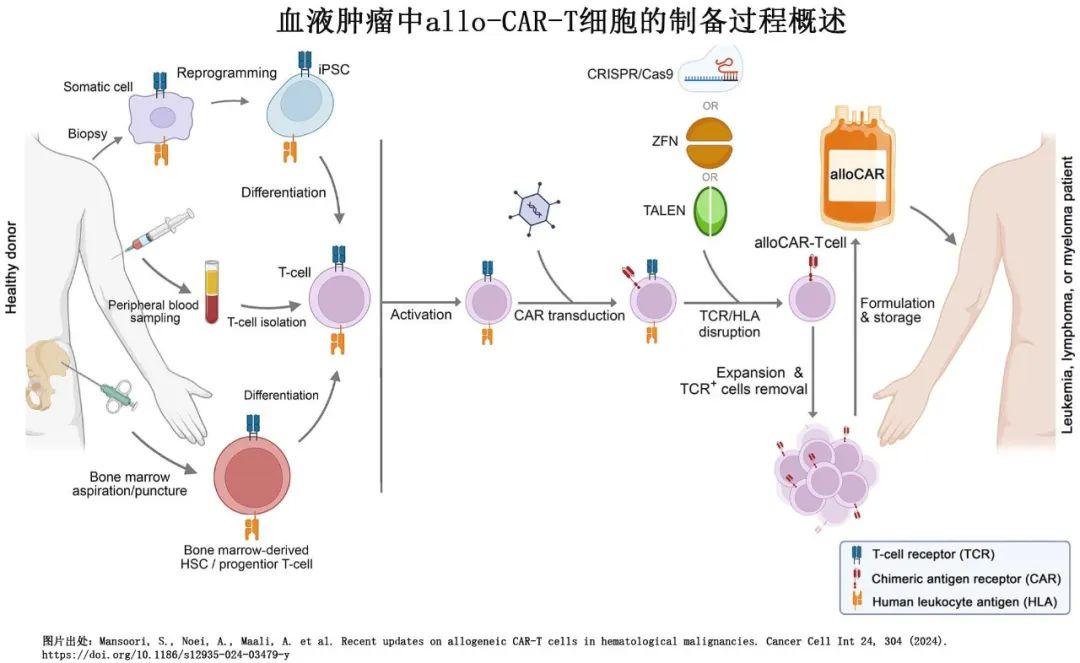
实体瘤中的细胞治疗
TIL疗法
实体瘤的细胞疗法主要是TIL,即从切除的肿瘤中离体生长的天然 T 细胞(图C;表3)。TIL疗法 lifileucel 已获得 FDA 加速批准,用于治疗既往接受过至少1种全身治疗的不可切除或转移性黑色素瘤患者;该批准是基于总缓解率31.5%和中位缓解持续时间未达到。经TIL治疗的人乳头瘤病毒(HPV)相关肿瘤,18例宫颈癌患者中有5例(28%)缓解,11例其他HPV相关肿瘤(如口咽癌)患者中有2例(18%)缓解。2例宫颈癌患者在单次输注 TIL 细胞后完全缓解超过5年。FDA已授予 TIL 治疗宫颈癌的突破性疗法资格;突破性疗法是一种可提供实质性改善的治疗状态,可加快 FDA 审查。
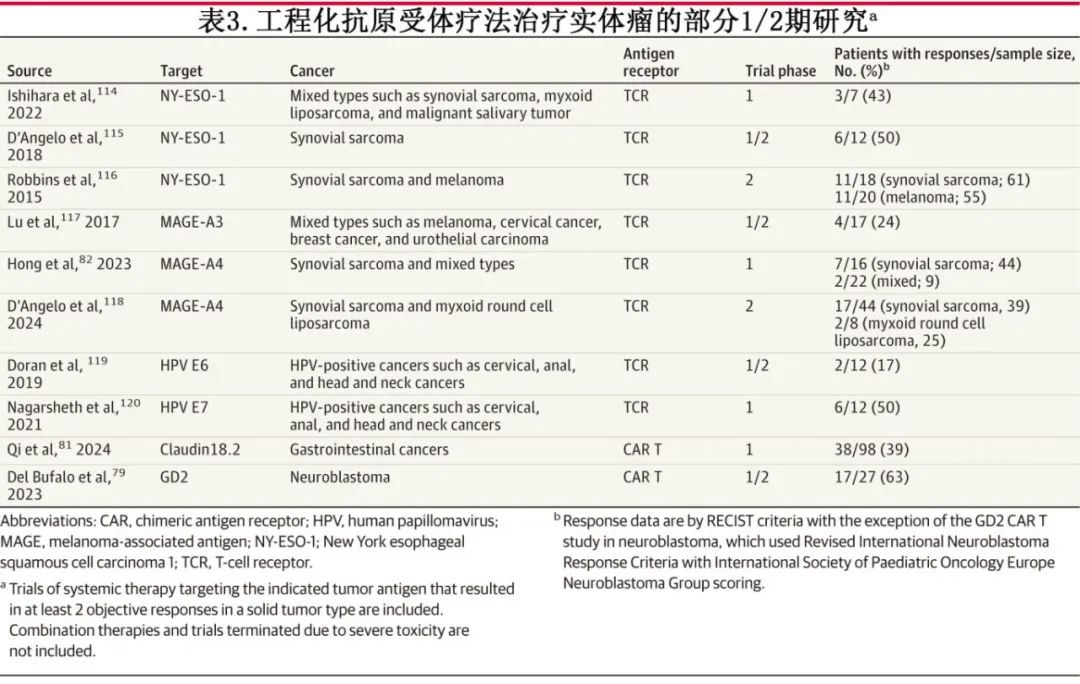
TCR T细胞疗法
TCR T 细胞治疗包括给予体外基因工程改造的 T 细胞,该T细胞可表达靶向肿瘤相关抗原的 TCR。它们与 TIL 不同,因为它们经过基因工程改造,具有靶向已知、已表征肿瘤相关抗原的已表征TCR,而 TIL 未经基因工程改造,具有靶向未知抗原的未表征天然TCR(图 C 和D)。TCR T细胞疗法 afamitresgene autoleucel 已获得 FDA 批准用于治疗既往化疗后的滑膜细胞肉瘤,其靶向抗原黑色素瘤相关抗原A4(MAGE-A4),这是一种来自癌症生殖系抗原类别的分子,在某些肿瘤、胚胎发育期间和生殖细胞中表达,但健康细胞不表达。该批准是基于一项单臂研究,总缓解率为39%,中位缓解持续时间为11.6个月。其他 TCR T 细胞疗法也在滑膜细胞肉瘤、黑色素瘤和 HPV相关肿瘤的早期临床试验中表现出良好抗肿瘤作用(表3)。黑色素瘤和滑膜细胞肉瘤的治疗是靶向胚系抗原,如 MAGE 家族成员和纽约食管鳞状细胞癌1(New York esophageal squamous cell carcinoma 1),缓解率为39%-61%。HPV相关肿瘤的治疗直接作用于 HPV 癌蛋白,即称为 E6 和 E7 的致癌病毒蛋白,其由癌症组成性表达,健康组织不表达。直接作用于 E7 的 TCR T 细胞在12例患者中的6例中表现出肿瘤反应,包括8例程序性细胞死亡蛋白1难治性肿瘤患者中的4例。治疗耐药主要是由于抗原呈递的肿瘤内在缺陷。参与干扰素应答和抗原呈递的基因丢失可作为预测性生物标志物。
CAR-T细胞疗法
CAR-T 细胞疗法一直难以用于实体瘤的治疗,部分原因在于 CAR 可以靶向的抗原有限,CAR通常只识别细胞表面抗原(图B)。部分用于实体瘤的 CAR-T 细胞疗法受到不良反应的限制,因为它们靶向肿瘤和健康组织共同表达的抗原;但也有令人鼓舞的结果。例如,根据修订的国际神经母细胞瘤反应标准,直接靶向双唾液酸神经节苷脂 GD2(disialoganglioside GD2)的 CAR-T 细胞在27例儿童神经母细胞瘤患者中的17例 (63%) 中获得缓解。前列腺癌中靶向前列腺特异性膜抗原的治疗显示前列腺特异性抗原减少,但1例患者在重度细胞因子释放综合征后死于败血症和多器官功能障碍。胃肠道肿瘤中靶向Claudin18.2的治疗显示98例患者中的38例 (39%) 部分或完全缓解,但缓解通常较短,且可能与 CAR-T 细胞输注前给予的化疗的抗恶性肿瘤活性有关。为了减少 CAR-T 细胞毒性,研究人员正在测试细胞直接进入肿瘤或肿瘤周围的局部治疗,尤其是在中枢神经系统肿瘤中。
总结
CAR-T 细胞疗法已获得 FDA 批准,可改善多发性骨髓瘤的无进展生存期,改善大 B 细胞淋巴瘤的总生存期,并使其他血液恶性肿瘤(如急性淋巴母细胞白血病、滤泡性淋巴瘤和套细胞淋巴瘤)获得较高的缓解率。最近 lifileucel 和 afamitresgene autoleucel 的批准也证明了基于 T 淋巴细胞的治疗改善实体瘤预后的潜力。
参考文献
Brudno JN, Maus MV, Hinrichs CS. CAR T Cells and T-Cell Therapies for Cancer: A Translational Science Review. JAMA. Published online November 04, 2024. doi:10.1001/jama.2024.19462


