好文推荐 | 同一家系ALS患者和正常人骨间肌组织的差异蛋白分析
时间:2025-02-27 12:36:04 热度:37.1℃ 作者:网络
摘要
目的 应用同位素标记相对和绝对定量技术(iTRAQ),筛选同一家系肌萎缩侧索硬化症(FALS)患者与正常组骨间肌中相关蛋白的差异表达,确定该家系的致病蛋白,为治疗打下基础。方法 提取同一家系所有受试者骨间肌组织,运用iTRAQ技术,对所有蛋白质进行定性定量分析,获得患病组与正常组蛋白质表达谱,生物信息学分析筛选与FALS发病相关蛋白质,运用基因注释(GO)分析细胞成分,对蛋白进行分类分析。结果 经质谱鉴定共获得453种蛋白质,GO分析患病组与正常组共筛选出14种差异蛋白(P<0.05):与正常组相比有5种蛋白低表达(Ratio<1);有9种蛋白高表达(Ratio>1)。结论 TRIM 72、NADH脱氢酶[泛醌]1β亚基1、膜联蛋白A1、核心蛋白聚糖、谷胱甘肽过氧化物酶3、胶原蛋白α-1(Ⅻ)链、胶原蛋白α-2(Ⅰ)的链和胶原蛋白Ⅰ型-α1-亚型CRA-a,与FALS高度相关。26 S蛋白酶体调节亚基8、层粘连蛋白亚基α2、富亮氨酸重复蛋白、原纤维蛋白1、肌球蛋白8和皮连蛋白,可能与FALS相关。
肌萎缩侧索硬化症(amyotrophic lateral sclerosis, ALS),在我国于2018年收录入由国家卫健委等部门制定的《第一批罕见病目录》中,分为家族性和散发性。ALS是由上、下运动神经元受损后引起的肌肉逐渐无力、萎缩的症状,最终呼吸衰竭而死亡的一种罕见病。由于ALS发病机制的复杂性及表型异质性,目前仍不能被治愈。本研究拟从罕见的家族性肌萎缩侧索硬化症(familial amyotrophic lateral sclerosis,FALS)患者中找到相关的蛋白,为临床治疗研究提供相关的资料,为未来治愈该疾病提供思路。
1 资料与方法
1.1 研究对象
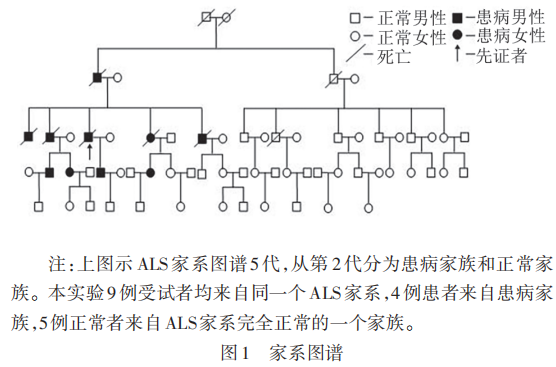
湖北省一个肌萎缩侧索硬化症家系,4例患者,其中男性2例,女性2例。年龄分别为35岁、45岁、39岁、44岁。临床表现以精神乏力,四肢麻木不同程度萎缩,食欲不振等为主,肌电图检查示广泛的运动神经元损害。5例同一个家系正常受试者,其中男性3例,女性2例。年龄分别为36岁、45岁、37岁、48岁、50岁,精神佳,四肢未见萎缩,四肢无麻木感,肌电图示正常。家系图谱见图1。
1.2 方法
9例受试者均进行任意手骨间肌组织的提取,提取后用生理盐水将肌肉组织冲洗至血色全无,滤纸沥干后用锡箔纸包裹好并编号,放入-80 ℃冰箱保存进行同位素标记相对和绝对定量技术(isobaric tags for relative and absolute quantitation,iTRAQ)实验。
1.3 iTRAQ实验方法
1.3.1 样品制备
取所有样品(9份),在液氮中研磨成粉末,迅速转移入1.5 ml离心管,每管加入0.5 ml SDT,100 ℃金属浴3 min。每份样品进行冰浴超声(80 W 2 s,间隔8 s,总超声时间5 min)。100 ℃金属浴3 min,14 000 g室温离心45 min,超声样本沸水浴3 min,20 ℃、14 000 g离心40 min,取上清并过0.22 μm滤膜,滤膜下清液即为样本蛋白质裂解液。蛋白质裂解液于-80 ℃冰箱中保存。
1.3.2 酶解
取9份样本各17 μg蛋白质等量合并成内标样本IS。取包括IS在内共10份样本各100 μg进行FASP酶解。每份样品加入200 μl UA buffer(8 M Urea,150 mm Tris-HCl pH8.5)混匀,14 000 g室温离心30 min,弃滤出液,重复3次。加入100 μl IAA(50 mm IAA in UA),600 r/min振荡混匀1 min,避光室温300 r/min孵育30 min,14 000 g室温离心30 min。加入100 μl UA buffer,室温14 000 g离心30 min,重复3次。加入100 μl 1/10 Dissolution buffer,室温14 000 g离心30 min,重复3次。最后弃滤出液并加入40 μl Trypsin buffer(2 μg Trypsin in 40 μl 1/10 Dissolution buffer),放置恒温混匀仪上 (300 r/min,18 h,37 ℃)。室温14 000 g离心30 min 收集滤出液,换新收集管,加入40 μl 25 mm 1/10 Dissolution buffer,室温14 000 g离心30 min,取滤液,OD280肽段定量。
1.3.3 肽段标记
各组样品分别取约17.5 μg, 按照AB公司试剂盒:iTRAQ Reagent-8 plex Multiplex Kit(AB SCIEX)说明书进行标记。
1.3.4 肽段的分离及鉴定
分别进行强阳离子交换层析分离、毛细管高效液相色谱分离、Q-Exactive质谱仪(Thermo Finnigan)进行质谱分析。
1.4 数据分析
质谱分析原始数据为RAW文件,用软件Protein Discovery 1.4进行查库鉴定、定量和数据分析。本次使用数据库:Uniprot_20150620_Homo sapiens_146 661.fasta(下载日期2015年6月20日,蛋白质序列146 661条)。软件抽提肽段报告离子峰强度值信息,肽段定量结果为参考样品所在标签的信号强度值与内标的信号强度值的比值。蛋白质定量结果为鉴定肽段定量结果的中位数。基因注释(gene ontology,GO)分析是通过生物信息学分析工具DAVID对鉴定蛋白质进行功能注释。蛋白质的GO功能注释包括3个方面内容:分子功能(molecular function)、生物过程(biological process)以及细胞分子(cellular component)。PATHWAY分析是通过 KEGG(Kyoto Encyclopedia of Genes and Genomes)数据库对鉴定的蛋白质进行通路分析。
2 实验结果
2.1 定量及SDS-PAGE电泳结果
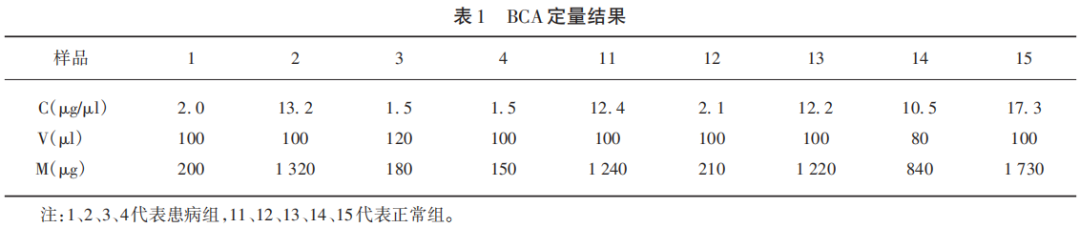
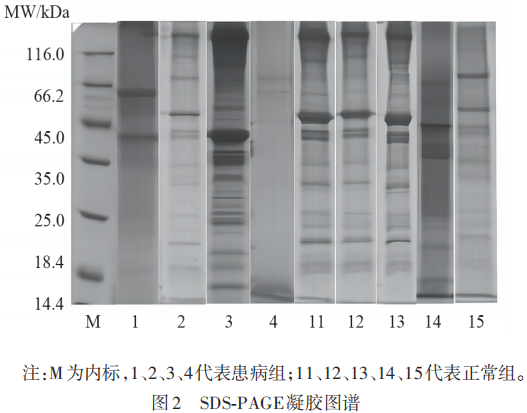
9例受试者蛋白BCA定量结果见表1,SDS-PAGE电泳结果见图2。
2.2 肽段及蛋白质定量结果
9例受试者肽段定量结果见表2,最终鉴定蛋白质组数目453个。

2.3 差异蛋白
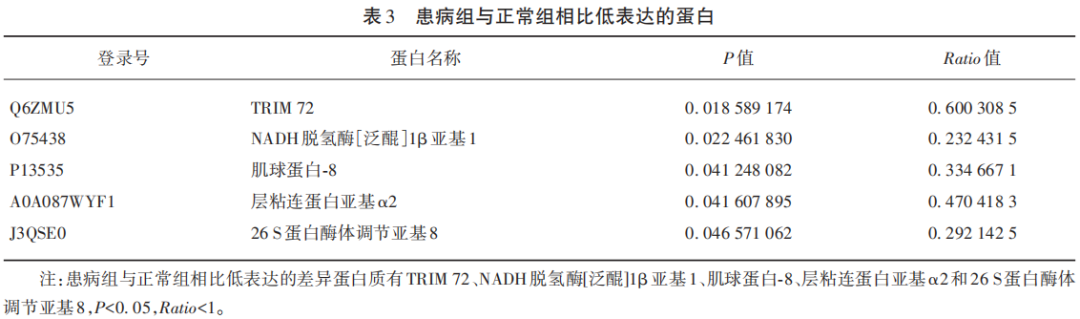
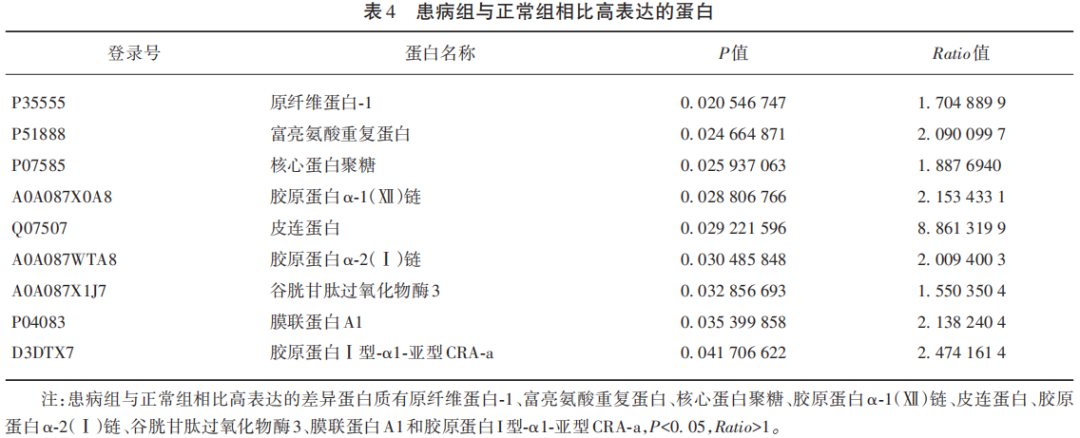
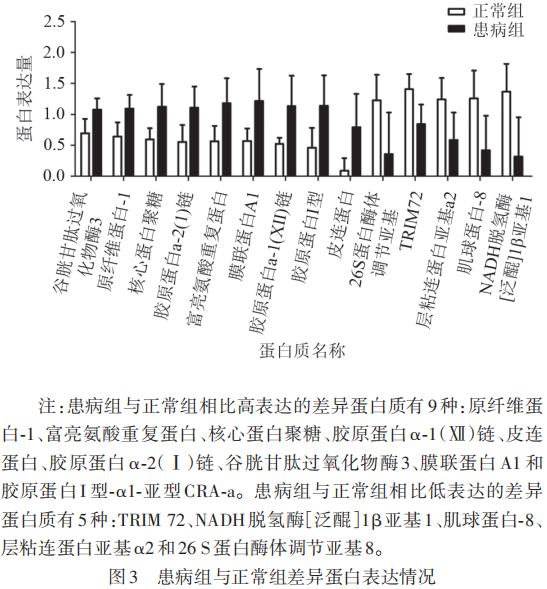
患病组与正常组对比共筛选出14个有差异的蛋白质(P<0.05),Ratio为患病组与正常组的比值,<1为低表达,>1为高表达。其中患病组与正常组相比低表达的蛋白质有5个,Ratio<1(见表3),患病组与正常组相比高表达的蛋白质有9个,Ratio>1(见表4)。患病组与正常组差异蛋白表达情况(见图3)。
2.4 患病组与正常组差异蛋白GO功能注释及Pathway分析
通过GO功能注释分析,患病组与正常组14个差异蛋白只有其中8个蛋白质是有功能注释的,分别是:高表达蛋白质:原纤维蛋白-1(fibrillin-1)、Prolargin富亮氨酸重复蛋白(PRELP)、核心蛋白聚糖(decorin)、皮连蛋白(dermatopontin)、膜联蛋白A1(annexin A1)。低表达蛋白质TRIM 72(tripartite motif-containing protein 72)、NADH脱氢酶[泛醌]1β亚基1[NADH dehydrogenase(ubiquinone)1 beta subcomplex subunit 1]、肌球蛋白-8(myosin-8)。其每个蛋白质的GO-BP、GO-CC、GO-MF都有很多条目,参与的生物过程主要集中表现在氧化磷酸化、电子传递链、抗凋亡、多糖代谢过程、细胞黏附、骨骼系统的发育、肌肉系统的进程、肌肉器官发育等。此外通过GO功能注释找出有相同功能的蛋白质并归类:其中富亮氨酸重复蛋白(prolargin)、核心蛋白聚糖(decorin)、原纤维蛋白1(fibrillin-1)具有相同的细胞组分:细胞外区域部分。富亮氨酸重复蛋白(prolargin)、膜联蛋白A1(annexin A1)、原纤维蛋白1(fibrillin-1)、肌球蛋白8(myosin-8)具有相同的分子功能:结构分子活动。富亮氨酸重复蛋白(prolargin)、核心蛋白聚糖(decorin)具有3条相同的分子功能:糖胺聚糖结合、多糖结合、受体分布。富亮氨酸重复蛋白(prolargin)、原纤维蛋白1(fibrillin-1)具有相同的细胞组分:蛋白质的细胞外基质。
其中KEGG-PATHWAY分析显示NADH脱氢酶[泛醌]1β亚基1的4条通路途径,hsa00190:氧化磷酸化(oxidative phosphorylation),hsa05010:阿尔茨海默病(Alzheimer disease),hsa05012:帕金森病(Parkinson disease),hsa05016:亨廷顿氏舞蹈病(Huntington disease);核心蛋白聚糖的通路,hsa04350:TGF-β信号转导通路(TGF-beta signaling pathway);肌球蛋白-8通路,hsa04530:紧密连接(tight junction),hsa05416:病毒性心肌炎(viral myocarditis)。
3 讨 论
家族性肌萎缩侧索硬化症发病机制复杂,不能治愈,死亡率高。近几年,国内外关于肌萎缩侧索硬化症相关蛋白的研究大量涌现,总结于笔者的一篇综述。基于此,本实验以同一个家系患病者骨间肌为研究载体,以同一个家系的正常人为对照,用运高通量芯片技术筛选差异蛋白,以探讨与该家系ALS有关的蛋白,从而为今后治疗该疾病找到出口。
通过GO分析得知:NADH脱氢酶[泛醌]1β亚基1[NADH dehydrogenase(ubiquinone)1β subcomplex subunit 1]参与的生物过程有:前驱体代谢产物和能量的产生、氧化磷酸化、线粒体电子传递,NADH泛醌、磷代谢过程、磷酸盐代谢过程、能源推导氧化有机化合物、磷酸化、电子传递链、呼吸电子传递链、ATP合成耦合电子传递、线粒体ATP合成耦合电子传递、细胞呼吸、氧化还原。存在于线粒体内膜,是线粒体呼吸链的一组分。具有氧化还原酶活性、NADH脱氢酶活性,作用于NADH或NADPH。NADH脱氢酶为线粒体呼吸链复合物Ⅰ,是一种与能量代谢相关的蛋白质,由45~46个蛋白亚基组成。本实验结果中NADH脱氢酶[泛醌]1β亚基1低表达,则影响NADH脱氢酶活性、氧化还原酶活性。而1NADH可生成3ATP,若ATP产生的太少或没有ATP产生则可以引起神经细胞的死亡或凋亡。因此,患病组中低表达的NADH脱氢酶[泛醌]1β亚基1与FALS高度相关。
通过GO分析,膜联蛋白A1(Annexin A1)参与的生物过程有:脂质运输、抗凋亡、炎症反应、有机酸运输、花生四烯酸的分泌、细胞的生长分化及信号转导等。膜联蛋白A1的分子功能有:酶抑制剂活性、钙离子结合、磷脂结合等,因此它是一种钙离子调控的磷脂结合蛋白。Annexin A1为磷脂酶A2抑制蛋白,依赖Ca2+与细胞膜磷脂发生结合,阻断类二十烷酸合成而发挥功能,是一种重要的炎症内源性抑制调节因子。Annexin A1可抑制炎性因子产生与氧化应激反应。膜联蛋白A1可抑制NO合酶(NOS)和环氧合酶(COX-2)起到抗炎保护作用。而NO被认为在ALS的发病机制中起到了关键作用,NO通过NO合酶合成精氨酸,NO合酶也被认为是NO产物的限制因素,研究发现当在变异型SOD1(G93A)的ALS小鼠中可诱导NOS(iNOS)活化的神经胶质细胞增多时神经元NOS(iNOS)是一种主要存在于神经细胞中的酶,负责催化生成一氧化氮(NO)。当神经元NOS在变异型SOD1(G93A)的ALS小鼠表达减少时iNOS的正调节、运动神经元的丢失加剧,神经胶质细胞激活、瓜氨酸及NO的水平始终一致。变异型SOD1(G93A)的ALS小鼠服用左旋精氨酸能够减少运动神经元的剧烈消耗及神经胶质细胞的活化,这一研究聚焦于iNOS的抑制,而在本实验结果中膜联蛋白A1较正常组表达高,加剧抑制NOS,也就是NOS表达减少来抑制运动神经元的丢失,说明此时机体正在发生运动神经元的丢失,膜联蛋白A1的高表达是机体进行自我保护。
通过GO-BP分析,TRIM 72(tripartite motif-containing protein 72)蛋白质参与的生物过程包括:肌肉器官的发育、肌肉膜修复、细胞分泌、囊泡转运、蛋白寡聚化等。TRIM 72又称MG 53蛋白,与心肌和骨骼肌修复密切相关,是参与心肌(或骨骼肌)缺血预适应和后适应过程中肌修复的重要因子;也在多种非肌肉组织器官中表达,在细胞修复和减轻器官损伤中起到至关重要的作用;骨骼肌是TRIM 72表达的重要部位,在骨骼肌中,细胞膜修复缺陷会导致肌细胞死亡、肌肉损伤和营养不良。TRIM 72能减轻脂多糖诱导的小鼠海马神经元细胞氧化损伤,为TRIM 72应用于神经性损伤的保护和修复提供了实验依据。研究发现TRIM 72基因敲除小鼠能够表现进行性肌营养不良症,在肌营养不良mdx鼠模型中注射重组表达人源TRIM 72蛋白可减弱病症。而本实验结果中TRIM 72蛋白表达低,从而加剧了ALS疾病的发生发展,与文献报道一致。若将重组表达人源TRIM 72蛋白注射入ALS模型鼠中是否也会减轻病症?可以是今后的一个研究方向进行试验验证。
通过GO分析,核心蛋白聚糖(decorin)参与的生物过程包括:多糖代谢过程、氨基聚糖的代谢过程、硫酸软骨素蛋白多糖的代谢过程、肽丝氨酸修饰、硫酸软骨素的代谢过程等。核心蛋白聚糖是蛋白质的细胞外基质的一组分,具有的分子功能有:受体分布、胶原蛋白结合、糖胺聚糖结合、蛋白N端结合、细胞外基质结合、碳水化合物结合。通过KEGG-PATHWAY分析:核心蛋白聚糖参与了转化生长因子-β(TGF-β)信号通路。核心蛋白聚糖(decorin)广泛存在于哺乳动物细胞外基质中,分子量小,其结构中富含亮氨酸,是体内自然存在的转化生长因子-β(TGF-β)抑制剂,能够中和以及灭活多种细胞因子包括TGF-β。TGF-β信号通路不仅通过影响上下神经元、炎症细胞与突触生长参与ALS疾病的发生,还可通过直接作用于肌肉细胞使肌肉组织纤维化而影响ALS疾病的严重程度。邹等对中国10个家族性ALS患者,202个散发性ALS患者和151例健康对照者进行筛查,在散发性ALS患者中发现了一种新的错义突变,c.379G>A(p.V103I),血管生成因子(angiogenic factor,ANG)突变占所有ALS患者中的0.5%,认为不同种群之间存在差异,ANG突变可能参与中国汉族人群ALS的发病。如果确定ANG突变能够引起中国汉族人群ALS发病则血管生成因子表达异常会导致TGF-β表达异常,进一步导致核心蛋白聚糖(decorin)表达异常。而本实验的结果核心蛋白聚糖表达高与这一理论相合,因此核心蛋白聚糖表达高与这一个家系ALS的发病高度相关。
谷胱甘肽过氧化物酶是人体内重要的一种酶,可以去除过氧化氢(H2O2)和许多有机氢过氧化物。当不良因素侵袭机体时,大量活性氮自由基(RNS)、活性氧自由基(ROS)和其他高活性分子会产生,此时,氧化物的去除率不及氧化程度时,就会使氧化、抗氧化系统失去平衡,从而引起机体组织损伤的病理状态。谷胱甘肽过氧化物酶3染色体定位为Chr.5q23,相对分子质量为25 552,主要在哺乳动物肾脏中表达并且包括附睾在内的其他多组织中低水平表达。如果在ALS患者体内检测出各类分子过氧化产物,就可以证实ALS病程的发展过程中存在氧化应激反应。本实验结果中谷胱甘肽过氧化物酶3在骨间肌组织中表达高,猜测机体正在受到过量自由基的侵害,需要大量过氧化物的产生,所以认为实验结果中谷胱甘肽过氧化物酶3的高表达与患者机体氧化应激反应有关。
胶原蛋白α-2(Ⅰ)链、胶原蛋白α-1(Ⅻ)链、胶原蛋白Ⅰ型-α1-亚型CRA-a这3种蛋白质通过GO功能注释分析,发现目前还没有研究人员对这3种蛋白质进行功能的分析。但是有证据显示来自关岛和其他地方的sALS患者的骨胶原蛋白是异常的。从ALS患者身上找到一批不同模式改变的胶原蛋白,这些和对照组身上的不一样,并且随着病情的进展会加重变化。有趣的是,一些来自关岛地区的对照组患者同样也表现出真皮组织的不规范变化,这并不是非关岛地区的个例。有研究发现ALS患者身上许多胶原蛋白的异常,总胶原蛋白含量在ALS患者皮肤和脊髓中都下降,并且胶原束也进一步分开和混乱,在血清和皮肤中,Ⅳ型胶原蛋白水平降低,而Ⅲ型前胶原蛋白和Ⅰ型胶原蛋白的含量则增加。因此,研究认为,胶原蛋白α-2(Ⅰ)链、胶原蛋白α-1(Ⅻ)链、胶原蛋白Ⅰ型-α1-亚型CRA-a高表达与该家系肌萎缩侧索硬化症相关。
通过GO分析,富亮氨酸重复蛋白(proline and arginine rich end leucine rich repeat protein,PRELP)参与的生物过程包括:骨骼系统发育、老化、细胞衰老。具有的分子功能有:糖胺聚糖结合、肝素结合、细胞外基质结构成分等。肌球蛋白-8(myosin-8)参与的生物过程包括:肌肉系统进程、肌肉收缩等。细胞组分包括:细胞骨架、肌球蛋白复合物、肌动蛋白细胞骨架、肌球蛋白Ⅱ复合体等。参与的分子功能包括:核苷酸结合、肌动蛋白结合、钙调素结合、细胞骨架蛋白结合等。肌球蛋白-8通路,hsa04530:紧密连接(tight junction),hsa05416:病毒性心肌炎(viral myocarditis)。近年来越来越多证据强调除了运动神经元(motor neurons,MNs),其他细胞如星形胶质细胞、小角质细胞、少突胶质细胞和肌肉细胞也积极参与ALS疾病的过程,如神经炎症和肌肉变性,因此本实验结果肌球蛋白8低表达可能与ALS相关。而膜联蛋白A1、富亮氨酸重复蛋白、原纤维蛋白1、肌球蛋白8具有相同的分子功能:结构分子活动。富亮氨酸重复蛋白、核心蛋白聚糖具有3条相同的分子功能:糖胺聚糖结合、多糖结合、受体分布。富亮氨酸重复蛋白、原纤维蛋白1具有相同的细胞组份:蛋白质的细胞外基质。因此,本实验富亮氨酸重复蛋白、原纤维蛋白1高表达可能与ALS相关,但目前尚无相关文献支持。调节亚基和核心区是26 S蛋白酶体的组成部分,许多亚单位存在调节亚基上,具有ATP酶活性的有6个。而26 S蛋白酶体调节亚基8、层粘连蛋白亚基α2,皮连蛋白目前没有GO功能注释分析,说明现在还没有研究人员对该蛋白进行功能方向的研究因此,我们猜测可能与该家系肌萎缩侧索硬化症相关。
本研究认为,与该FALS高度相关的蛋白质为:TRIM 72、NADH脱氢酶[泛醌]1β亚基1、膜联蛋白A1、核心蛋白聚糖、谷胱甘肽过氧化物酶3、胶原蛋白α-1(Ⅻ)链、胶原蛋白α-2(Ⅰ)链和胶原蛋白Ⅰ型-α1-亚型CRA-a。在疾病中膜联蛋白A1、核心蛋白聚糖、胶原蛋白α-1(Ⅻ)链、胶原蛋白α-2(Ⅰ)链、胶原蛋白Ⅰ型-α1-亚型CRA-a高表达促进神经细胞的细胞死亡或凋亡,而NADH脱氢酶[泛醌]1β亚基1为细胞呼吸链Ⅰ的组成成分,TRIM 72低表达,促使线粒体呼吸链损伤,能量代谢障碍,最终引起神经细胞功能异常或死亡。这8种蛋白质表达的变化均与FALS的发生密切相关。26 S蛋白酶体调节亚基8、层粘连蛋白亚基α2、富亮氨酸重复蛋白、原纤维蛋白1、肌球蛋白8和皮连蛋白,这6种蛋白质可能与该家系ALS相关。因此,我们以此结果为参考,为FALS疾病的预防及后续治疗等相关研究提供线索,从而可提高ALS患者的寿命达到ALS的靶向治疗。
参考文献
[1]李玲, 黄银兰, 马腾. 国内外肌萎缩性侧索硬化症发病相关蛋白研究进展[J]. 中风与神经疾病杂志, 2014, 31(10): 953-955.
[2]Du H, Yan SS. Mitochondrial permeability transition pore in Alzheimer’s disease): cyclophilin D and amyloid beta[J]. Biochim Biophys Acta, 2010, 1802(1): 198-204.
[3]Abdulwahid Arif I, Khan HA. Environmental toxins and Parkinson’s disease): putative roles of impaired electron transport chain and oxidative stress[J]. Toxicol Ind Health, 2010, 26(2): 121-128.
[4]Sinniah A, Yazid S, Bena S, et al. Endogenous annexin-A1 negatively regulates mast cell-mediated allergic reactions[J]. Front Pharmacol, 2019, 10): 1313.
[5]李川, 钟育武, 赵展庆. 膜联蛋白A1对冠心病模型大鼠心肌损伤及中性粒细胞胞外诱捕网形成的影响[J]. 中国老年学杂志, 2024, 44(12): 2950-2956.
[6]王春莹, 刘俊, 林镯, 等. 膜联蛋白Ⅰ在大鼠肝纤维化组织中的表达及意义[J]. 临床肝胆病杂志, 2011, 27(6): 628-631.
[7]Lee J, Ryu H, Kowall NW. Differential regulation of neuronal and inducible nitric oxide synthase (NOS) in the spinal cord of mutant SOD1 (G93A) ALS mice[J]. Biochem Biophys Res Commun, 2009, 387(1): 202-206.
[8]张进,杨丽丽,康静,等.MG53/TRIM72 蛋白的功能及作用机制研究进展[J].生理科学进展,2024,1079(7).doi.org/10.20059/.cnki.pps.2024.07.1079.
[9]龙香花, 鲁跃, 裴昌贞. MG53改善脂多糖诱导小鼠抑郁样行为的实验研究[J]. 新疆医科大学学报, 2022, 45(3): 259-264.
[10]Waddell LB, Lemckert FA, Zheng XF, et al. Dysferlin, annexin A1, and mitsugumin 53 are upregulated in muscular dystrophy and localize to longitudinal tubules of the T-system with stretch[J]. J Neuropathol Exp Neurol, 2011, 70(4): 302-313.
[11]Weisleder N, Takizawa N, Lin P, et al. Recombinant MG53 protein modulates therapeutic cell membrane repair in treatment of muscular dystrophy[J]. Sci Transl Med, 2012, 4(139): 139ra85.
[12]Burkin DJ, Wuebbles RD. A molecular bandage for diseased muscle[J]. Sci Transl Med, 2012, 4(139): 139fs19.
[13]杜彩霞. 核心蛋白聚糖对哮喘小鼠气道重塑的影响[D]. 青岛): 青岛大学, 2013.
[14]芦怡, 张立涵, 潘煦一, 等. TGF-β信号通路在神经退行性疾病中的作用研究进展[J]. 中国细胞生物学学报, 2022, 44(10): 1995-2005.
[15]Zou ZY, Wang XN, Liu MS, et al. Identification of a novel missense mutation in angiogenin in a Chinese amyotrophic lateral sclerosis cohort[J]. Amyotroph Lateral Scler, 2012, 13(3): 270-275.
[16]刘美之, 常丽萍, 郎艳松, 等. 外膜滋养血管在动脉粥样硬化中的作用[J]. 中国老年学杂志, 2014, 34(6): 1691-1694.
[17]刘新, 李建远. 附睾抗氧化系统中的谷胱甘肽过氧化物酶家族蛋白[J]. 检验医学与临床, 2011, 8(4): 470-472.
[18]马腾, 黄银兰, 李玲. 中西医对肌萎缩侧索硬化症病因病机的研究进展[J]. 时珍国医国药, 2015, 26(12): 2990-2992.
[19]Field NC, Caller TA, Stommel EW. An explanation for the changes in collagen in sporadic amyotrophic lateral sclerosis[J]. Med Hypotheses, 2011, 77(4): 565-567.
[20]Robberecht W, Philips T. The changing scene of amyotrophic lateral sclerosis[J]. Nat Rev Neurosci, 2013, 14(4): 248-264.
[21]费尔康, 范骏, 王洪枫, 等. 神经退行性疾病相关蛋白的翻译后修饰[J]. 中国科学技术大学学报, 2008, 38(8): 978-985.


