Neuro-Oncology:CAR-T细胞治疗45例CNS淋巴瘤的回顾性报道
时间:2023-07-09 09:08:51 热度:37.1℃ 作者:网络
CAR T于CNS淋巴瘤
CNS 淋巴瘤是指在初次诊断时无全身性疾病情况下局限于脑、脑膜、眼或脊髓的淋巴瘤(原发性CNS淋巴瘤,PCNSL)或全身性淋巴瘤转移至CNS(继发性CNS淋巴瘤,SCNSL)。CNS复发的淋巴瘤患者即使接受了积极治疗(包括放疗或化疗),其预后也不到12个月。因此迫切需要创新和更有效的治疗方法。
已有多个CAR T细胞疗法获批治疗复发/难治性大B细胞淋巴瘤,但其有显著的毒性负担,包括神经毒性症状,即免疫效应细胞相关神经毒性综合征 (ICANS) ,其范围介于轻度意识模糊至潜在致死性脑水肿。考虑到靶抗原存在于 CNS 内时神经毒性增加以及 CAR T 细胞跨血脑屏障转运受损,几乎所有其他研究均排除了伴原发性和继发性 CNS 受累的淋巴瘤患者。在活动性 CNS 疾病背景下,CAR T 细胞输注后的缓解数据及 CNS 特异性毒性数据有限,但仍有研究提示有颅内活性。
马萨诸塞州总医院神经科Jorg Dietrich教授近日于《Neuro-Oncology》(IF=15.9)发表一项回顾性研究,分享了CD19 CAR T 细胞治疗CNS 淋巴瘤患者的47例机构经验,描述了 CAR T 细胞输注后的临床过程和遇到的神经毒性副作用,以及它们与炎症血清标志物的相关性,还探索了 CNS 特异性反应模式和临床结局的预测因素,包括桥接治疗和类固醇使用。

1、CD19 CAR T 细胞在 CNS 淋巴瘤中似乎是安全的,全身基线炎症与 ICANS 相关。
2、69%的患者可达到CNS缓解;清淋期间较低的类固醇剂量和伊布替尼桥接与结局改善相关。
研究结果
该研究为回顾性研究,分析了2018-2022年在该机构接受CD19 CAR T细胞治疗的连续CNS淋巴瘤患者(神经影像学或CSF确认),且需要可以评估缓解
基线患者特征
45例因 CNS 淋巴瘤输注 CAR T 细胞(表1),包括17例 PCNSL 患者和27例 SCNSL 患者,1例 PCNSL 患者在16个月后因疾病进展接受了第二次 CAR T 细胞输注。基础疾病包括:DLBCL(PCNSL:18/18例,100%;SCNSL:19/27例,70.4%)、转化型淋巴瘤(滤泡性淋巴瘤、粘膜相关淋巴组织淋巴瘤或套细胞淋巴瘤;SCNSL:7/27例,25.9%)和 Burkitt 淋巴瘤(SCNSL:1/27例,3.7%)。所有 PCNSL 患者和大多数 SCNSL 患者既往大剂量甲氨蝶呤治疗失败,每例患者均有复发性或难治性疾病,既往治疗的中位数为3。所有患者的MRI或 CSF 分析证实 CAR T 细胞输注前存在活动性 CNS 疾病:25例病例 (55.6%) 累及脑实质,8例病例 (17.8%) 累及软脑膜,并发脑实质及软脑膜病变12例 (26.7%)。全身 CT 或 PET检出活动性全身疾病13例 (28.9%)。从白细胞单采至 CAR T 细胞输注的平均时间为32.0±0.9天。伊布替尼最常用于 CAR T 细胞输注的桥接治疗(21/36例接受桥接治疗的患者,58.3%)。临床上可能时,停用类固醇剂量,直至 CAR T 细胞输注。清淋治疗,44例病例 (97.8%) 使用氟达拉滨和环磷酰胺,1例 SCNSL 患者 (2.2%) 使用苯达莫司汀联合治疗。所有患者均接受靶向 CD19(tisagenlecleucel、lisocabtagene maraleucel、axicabtagene ciloleucel)的三种市售 CAR T 细胞产品中的一种。
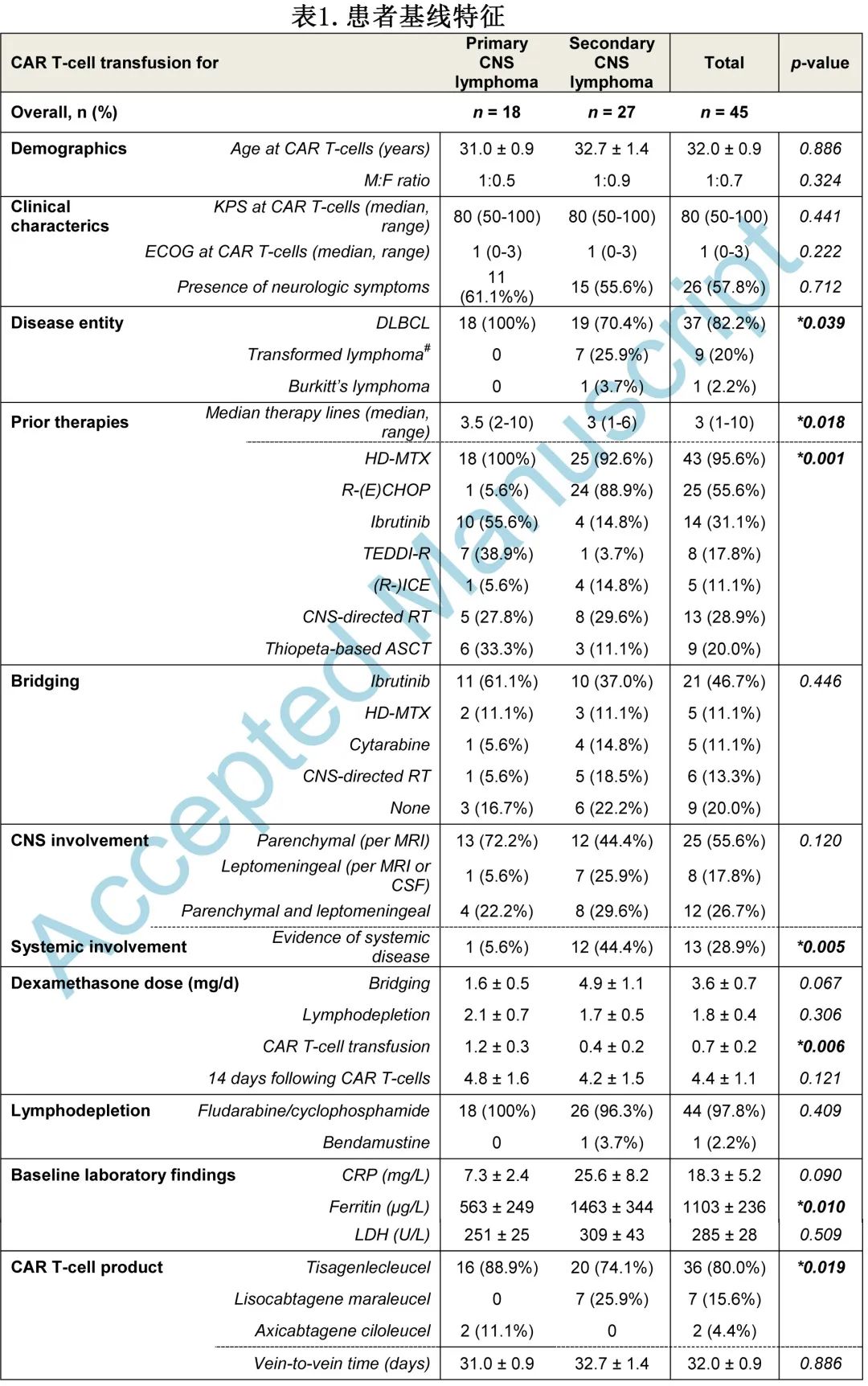
PCNSL 和 SCNSL 患者在人口统计学、CAR T细胞输注时的临床特征、CNS受累模式、桥接治疗或平均静脉-静脉时间方面无差异。值得注意的是,仅1例 PCNSL 患者(全身复发,但最初疾病局限于CNS)有全身受累,但12例 SCNSL 患者有全身受累;SCNSL 患者的基线血清炎症标志物 C-反应蛋白 (CRP) 和铁蛋白水平较高(PCNSL与 SCNSL 的CRP mg/L:7.3±2.4与25.6±8.2,p=0.090;铁蛋白μg/L:563±249与1463±344,p=0.010)。此外,在 CAR T 细胞输注时PCNSL患者使用的类固醇剂量略高于 SCNSL 患者,而在桥接、清淋或 CAR T 细胞输注后未观察到差异。
CAR T细胞输注后的神经和全身毒性
PCNSL 患者中8例病例 (44.4%)观察到 ICANS 症状,在中位2.5天后检测到首发症状(图1A)。尽管症状通常是一过性的,中位持续时间为5.5天,但发生了3例高级别神经毒性病例,包括1例在败血症死亡的4级 ICANS 患者。
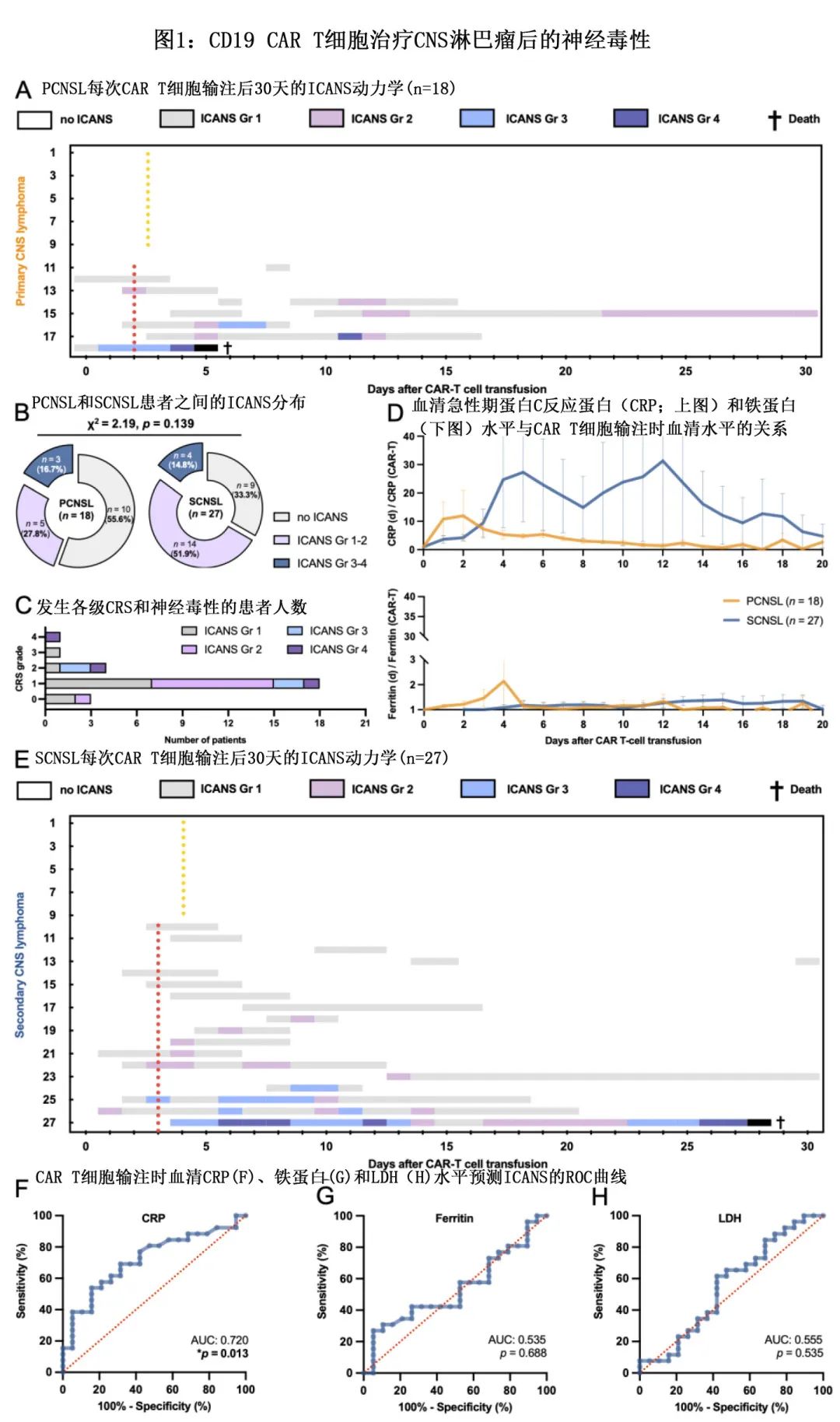
SCNSL 患者神经系统症状的中位发作和持续时间与 PCNSL 相似(发作:4天;持续时间:4.5天)。1例患者在重度神经毒性症状和并发败血症的情况下死亡(图1E)。此外,PCNSL和 SCNSL 患者的临床表型无差异,与既往报告一致:ICANS 1-2级表现为轻度脑病(头痛、失语、震颤、意识模糊),而 ICANS 3-4 级导致精神状态改变或意识水平降低。大多数患者使用左乙拉西坦预防癫痫发作。
然而,SCNSL患者中 ICANS 的相对频率有升高趋势,18例病例 (66.7%) 出现任何级别的神经毒性症状(图1B)。ICANS 与 CRS 密切相关,因为所有 ICANS 3-4 级的患者也均发生CRS(图1C);在 PCNSL 和 SCNSL 患者中,早发性发热≥38℃(CAR T细胞输注后3天内)通常先于神经毒性症状出现。与 CAR T 细胞输注后炎症负荷增加一致,与 PCNSL 患者相比,SCNSL患者的血清 CRP 水平显著升高且延长(图1D)。基线CRP(CAR T细胞输注时)可预测任何程度的ICANS(AUC:0.720,p = 0.013),而铁蛋白或 LDH无法预测。整个队列中,血清 CRP 水平 >4.9 mg/L识别后续发生 ICANS 的患者的灵敏度为69.2%,特异性为68.4%(图1F-G)。重要的是,当仅应用于 PCNSL 或 SCNSL 患者时,CRP临界值>4.9 mg/L也可区分 ICANS 患者 (PCNSL:χ2:3.7,p=0.001;SCNSL:χ2:5.2,p=0.001)。反过来说,单纯存在全身性疾病与CRS(χ2:1.2;p = 0.275) 和ICANS(χ2:1.0;p = 0.322) 均无关。
CNS复发的模式和发生率
所有患者均可获得 CAR T 细胞输注后的疾病分期。在脑实质和软脑膜受累的患者中均观察到对 CAR T 细胞输注的放射学反应(图2A,B)。68.9%(31/45)的患者观察到 CNS 缓解,其中18例显示完全缓解 (40.0%)(图2C,D)。大多数患者在中位1个月后达到最佳缓解(PCNSL:29天;SCNSL:28天),也有部分患者继续出现疾病消退,即使在没有额外抗肿瘤治疗的情况下也可在 CAR T 细胞输注后6个月达到完全缓解;在出现基线神经系统异常的患者中会伴随着症状稳定或改善,而疾病进展与症状恶化相关。在 CAR T 细胞后达到完全缓解的患者中,患者保持无 CNS 疾病的中位时间为11.4±4.5个月。中位随访12.0±5.6个月后,共有32例患者 CNS 内进展,中位CNS 无进展生存期为2.0±0.7个月(图2E),14例 PCNSL 患者 (77.8%) 和18例 SCNSL 患者 (66.7%)进展。PCNSL 和 SCNSL 患者的缓解模式或中位 CNS 无进展生存期均无差异(中位CNS-PFS:3.5 vs 2.0个月,HR=0.83,p=0.652)。
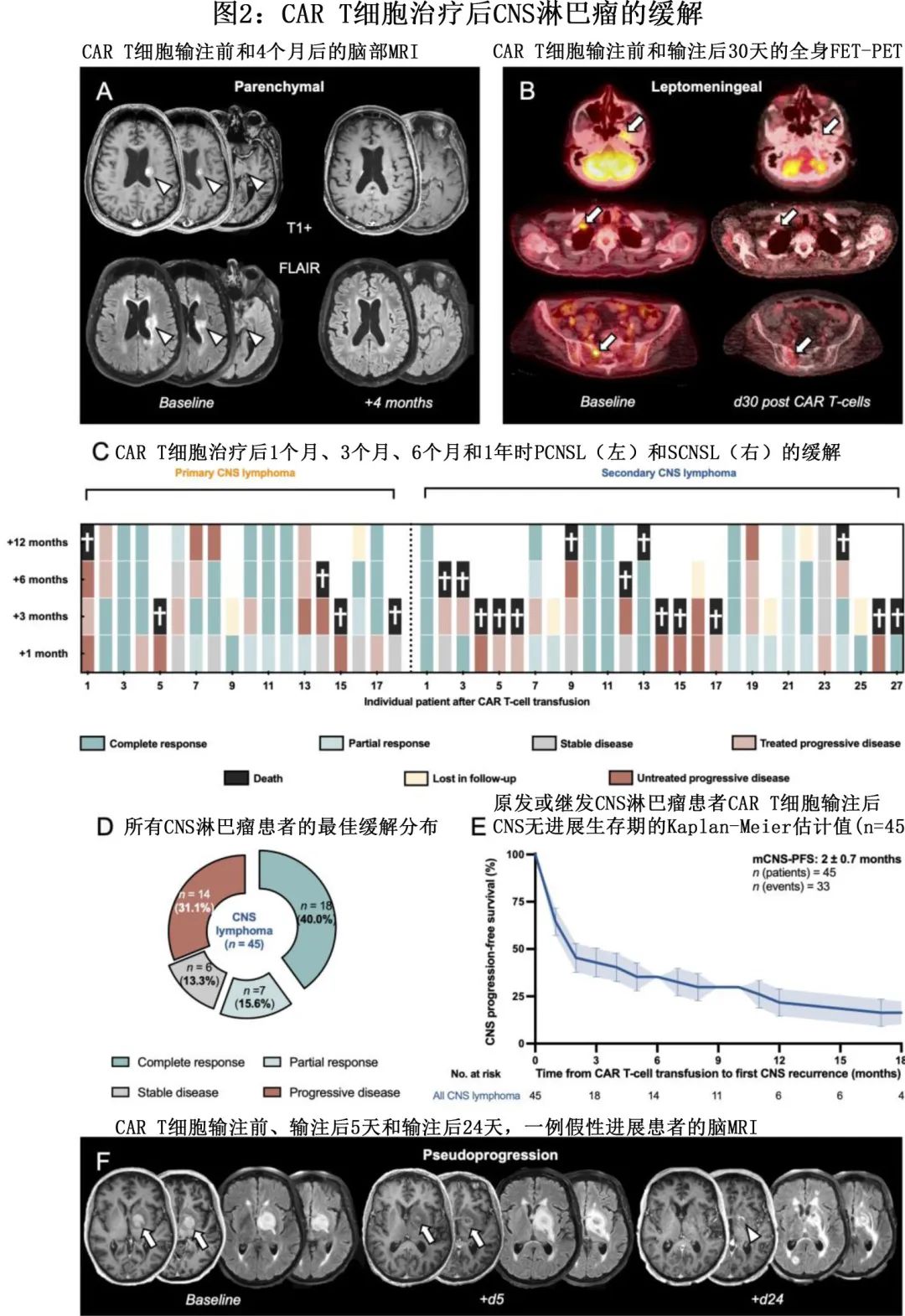
早期 MRI 怀疑4例PCNSL(22.2%) 和4例SCNSL(14.8%) 为假性进展,表现为已知 CNS 病灶的 T2/FLAIR 高信号或对比增强增强,但临床上大多保持惰性,除使用类固醇外,未接受抗肿瘤治疗即改善。值得注意的是1例 SCNSL 患者在 CAR T 细胞输注后4天发生重度ICANS,表现为癫痫发作和昏迷,MRI 显示左侧基底神经节内对比增强病变周围广泛水肿,解释为假性进展。大剂量类固醇治疗后患者大幅改善,影像学变化消退,但最终在4天后死于真菌性败血症,尸检证实无淋巴瘤(图2F)。需要注意的是,考虑到未进行基于组织的诊断,实际上不能排除一些接受假定进展治疗的病例实际上发生假性进展的可能性。然而,推测进展患者通常具有侵袭性临床病程,一般不支持假性进展。
临床变量与CNS结局的相关性:类固醇的作用、桥接治疗和受累模式
固醇通常用于改善疾病进展的临床症状,直至 CAR T 细胞输注,但由于假设皮质类固醇可能对 CAR T 细胞的预期抗肿瘤作用产生负面影响,因此尽可能逐渐减量(图3A,表1)。因此,作者记录了 CAR T 细胞输注前后不同时间间隔的每日地塞米松剂量(或当量),以描述其对 CNS 反应的特异性影响。通过单变量 Cox 比例风险回归模型预测,在清淋期间每增加 1mg/d 地塞米松,CNS进展的风险比呈指数增加(图3B),但在桥接期间、CAR T细胞输注期间或 CAR T 细胞输注后14天内未发现地塞米松剂量之间的相关性。在多变量分析中进行评价时,该观察结果也得以保留,并且预测在清淋期间每1mg/d 地塞米松的 HR 增加1.16(p=0.031)。值得注意的是,不同间隔的地塞米松剂量在主成分分析(PCA)上都是相互关联的(通过计算负荷,即数值估计多个变量之间的相关性,范围从-1到1),表明存在混杂因素(例如更具侵袭性疾病)接受地塞米松给药(PCA上地塞米松每日剂量的负荷:桥接时-0.78/淋巴细胞耗竭时-0.82/CAR T细胞输注时-0.72/CAR T细胞输注后14天-0.39)。由于清淋期间仅地塞米松剂量对 CNS 结局很重要,从而反驳了以下假设:较高的类固醇剂量只是固有预后较差的肿瘤(由于更具侵袭性生长或接近关键脑区)的替代标志物。根据清淋期间的地塞米松剂量将患者分层,发现 6-8 mg/日地塞米松的临界值,会转化为比仅使用最小剂量 0-1 mg/日地塞米松的患者更差的 CNS 结局(0-1 mg/日 vs 8 mg/日:4 vs 1个月,HR=0.11,p=0.047)(图3C)。
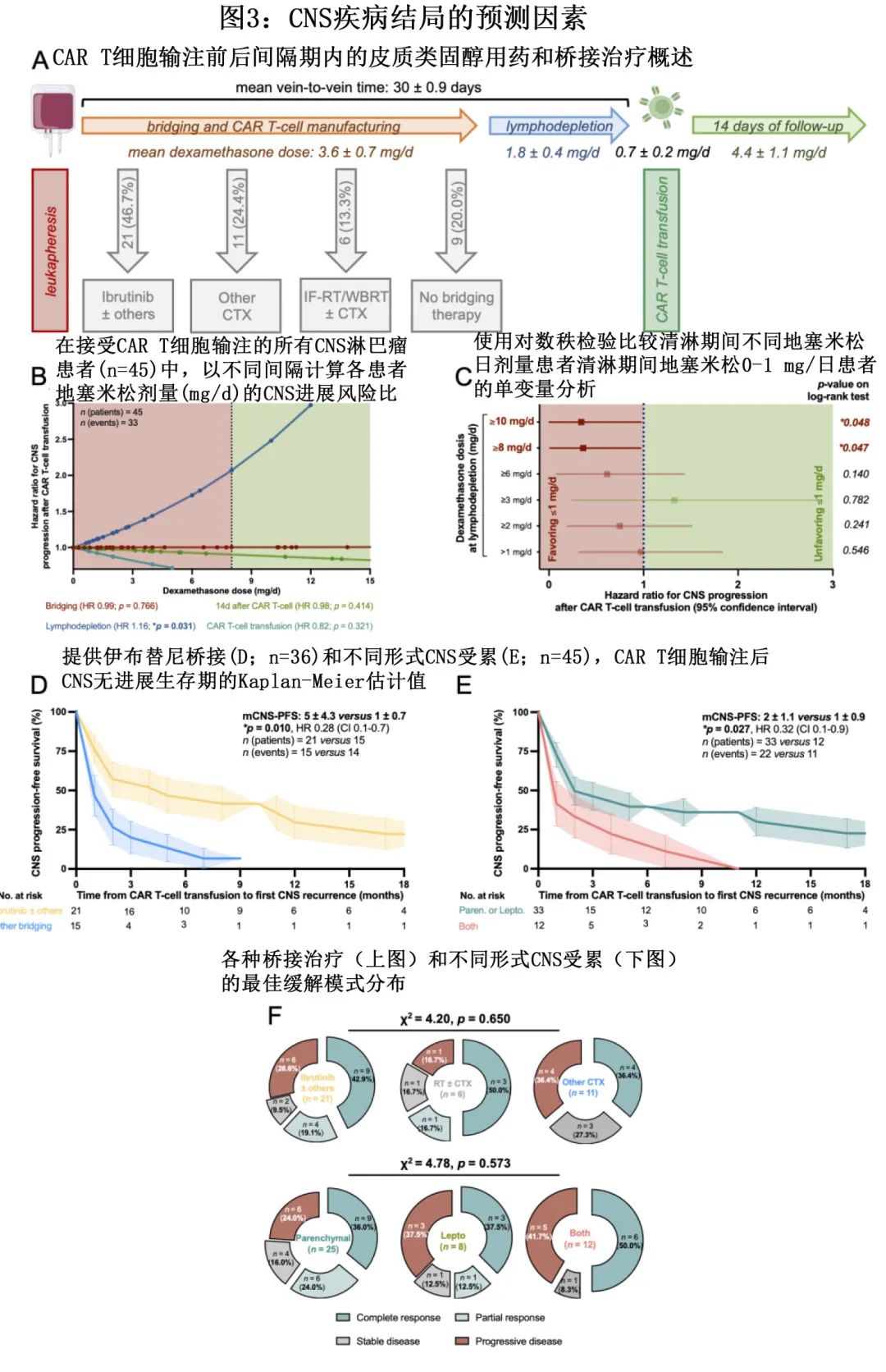 鉴于活动性 CNS 淋巴瘤的侵袭性,36例病例(80%;PCNSL:15/18例患者,83.3%;SCNSL:21/27例患者,77.8%)需要化疗、放疗或免疫治疗的桥接治疗。因此,桥接治疗本身的必要性似乎指定了更具侵袭性的疾病,其特征为 CNS 无进展生存期略短(2 vs 6.5个月,HR=1.58,p=0.399)。最佳桥接策略仍需评估,推测伊布替尼可增强 T 细胞功能和持久性,作者也确实发现,与不使用伊布替尼的其他桥接治疗相比,使用伊布替尼(单药或与其他治疗联合)与 CNS 无进展生存期延长相关(5 vs 1个月,HR=0.28,p=0.010)(图3D)。有趣的是,当比较脑实质或软脑膜受累的患者时,没有特定的缓解持续时间;然而,当 CAR T 细胞输注时同时存在脑实质和软脑膜疾病时,CNS无进展生存期缩短(1个月 vs 2 个月,HR=3.15,p=0.027),因此可能表明疾病更晚期(图3E)。尽管缓解持续时间受到有利影响,但伊布替尼与其他桥接治疗之间的初始缓解模式无差异(图3F)。
鉴于活动性 CNS 淋巴瘤的侵袭性,36例病例(80%;PCNSL:15/18例患者,83.3%;SCNSL:21/27例患者,77.8%)需要化疗、放疗或免疫治疗的桥接治疗。因此,桥接治疗本身的必要性似乎指定了更具侵袭性的疾病,其特征为 CNS 无进展生存期略短(2 vs 6.5个月,HR=1.58,p=0.399)。最佳桥接策略仍需评估,推测伊布替尼可增强 T 细胞功能和持久性,作者也确实发现,与不使用伊布替尼的其他桥接治疗相比,使用伊布替尼(单药或与其他治疗联合)与 CNS 无进展生存期延长相关(5 vs 1个月,HR=0.28,p=0.010)(图3D)。有趣的是,当比较脑实质或软脑膜受累的患者时,没有特定的缓解持续时间;然而,当 CAR T 细胞输注时同时存在脑实质和软脑膜疾病时,CNS无进展生存期缩短(1个月 vs 2 个月,HR=3.15,p=0.027),因此可能表明疾病更晚期(图3E)。尽管缓解持续时间受到有利影响,但伊布替尼与其他桥接治疗之间的初始缓解模式无差异(图3F)。
总结
本队列包括17例原发性 CNS 淋巴瘤(PCNSL;1例患者接受2次 CAR T 细胞输注)和27例继发性 CNS 淋巴瘤 (SCNSL) 患者。19/45例输注 (42.2%) 后发生轻度ICANS(1-2级),7/45例输注 (15.6%) 后发生重度ICANS(3-4级)。在 SCNSL 中检测到 C 反应蛋白 (CRP) 水平的更大增加和 ICANS 的发生率更高。早期发热和基线 C 反应蛋白水平与 ICANS 发生相关。31例病例 (68.9%) 达到CNS 缓解,包括18例病例 (40.0%)CNS疾病完全缓解,中位持续时间为11.4±4.5个月。清淋时的地塞米松剂量(而非 CAR T 细胞输注时或输注后)与 CNS 进展风险增加相关 (每mg/d的HR=1.16,p=0.031)。如果需要桥接治疗,使用伊布替尼可转化为有利的无CNS进展生存期(5 vs 1个月,HR=0.28,p=0.010)。
总的来说,CAR T 细胞在原发性和继发性 CNS 淋巴瘤患者中表现出令人鼓舞的抗肿瘤特性,它可能发生神经毒性症状,但也似乎反映出全身炎症的影响,而非CNS疾病本身的存在。皮质类固醇应慎用,尤其是在清淋期间。桥接治疗可能协同影响 CAR T 细胞治疗,其中伊布替尼或其他 BTK 抑制剂可能是进一步促进 CAR T 细胞成功的有前景的候选药物。
参考文献
Karschnia P,et al. Neurotoxicity and management of primary and secondary CNS lymphoma after adoptive immunotherapy with CD19-directed CAR T-cells.Neuro Oncol . 2023 Jul 4;noad118. doi: 10.1093/neuonc/noad118.


