科研动态丨从突变、机制到个体化治疗——姜玉武教授团队发表论文阐释GRIN2D基因突变与儿童癫痫脑病
时间:2019-11-06 22:26:48 热度:37.1℃ 作者:网络
发育性癫痫脑病是一组临床常见的儿童难治性癫痫综合征,其病因复杂、表型多变、治疗困难,预后较差,目前已发现数十种基因突变与该病相关。近日,我院姜玉武教授团队与美国Emory大学医学院Hongjie Yuan/Stephen F. Traynelis教授团队联合在BRAIN (IF=11.814) 期刊发表了题为“Heterogeneous clinical and functional features of GRIN2D-related developmental and epileptic encephalopathy”的Original Article文章。本文是继2016年首次发现GRIN2D基因为发育性癫痫脑病的致病基因之一后,全球第二篇有关GRIN2D基因与发育性癫痫脑病的研究文章。

科研动态
研究共收集了来自中国、美国、欧洲及中东等地区的8名基因突变患者,研究了NMDA受体亚基GRIN2D基因罕见突变导致发育性癫痫脑病患儿的临床特征、分子机制及潜在个体化治疗策略。8例GRIN2D患者年龄在9个月至34岁之间,其中女性4例,男性4例,均无明确神经系统疾病家族史及围产期病史。其中87.5%的患者癫痫起病年龄在1岁以内,50%的癫痫发作为痉挛发作 ,部分患者随着病情发展逐渐出现其他发作形式,例如局灶发作伴泛化、失张力发作,肌阵挛发作等。所有患者均有不同程度的智力障碍/发育迟滞,部分患者出现肌张力减退及运动障碍。
该研究共发现了6种既往未见文献报道的全新GRIN2D突变,分别为S573F、L670F、A675T、A678D、S1271L及R1313W,突变不耐受分析提示位于跨膜结构域的突变具有较高的致病可能。
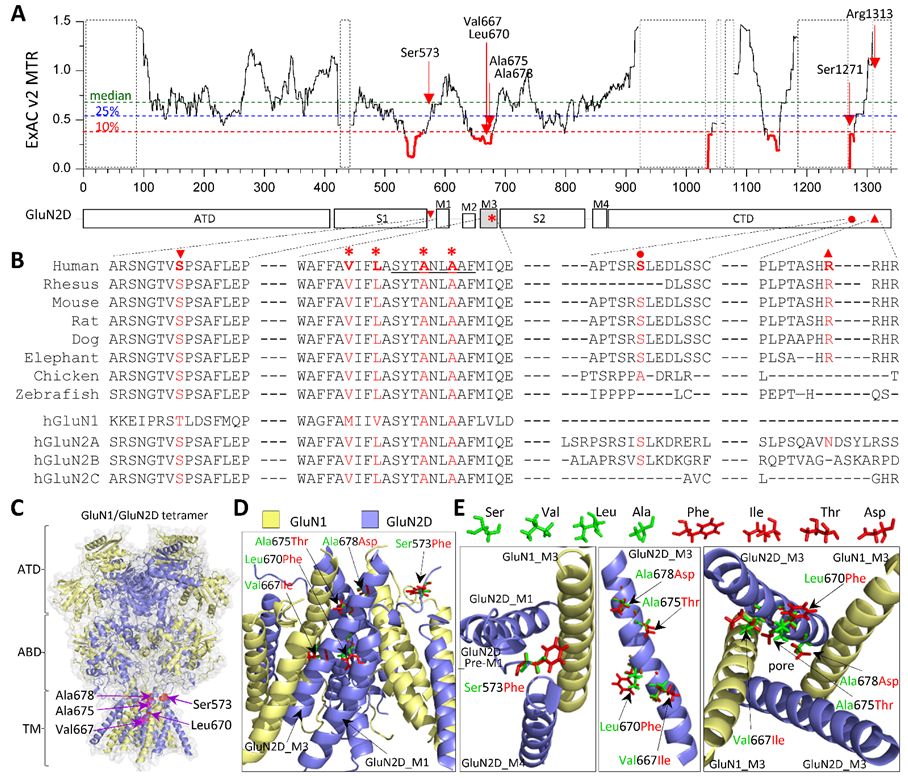
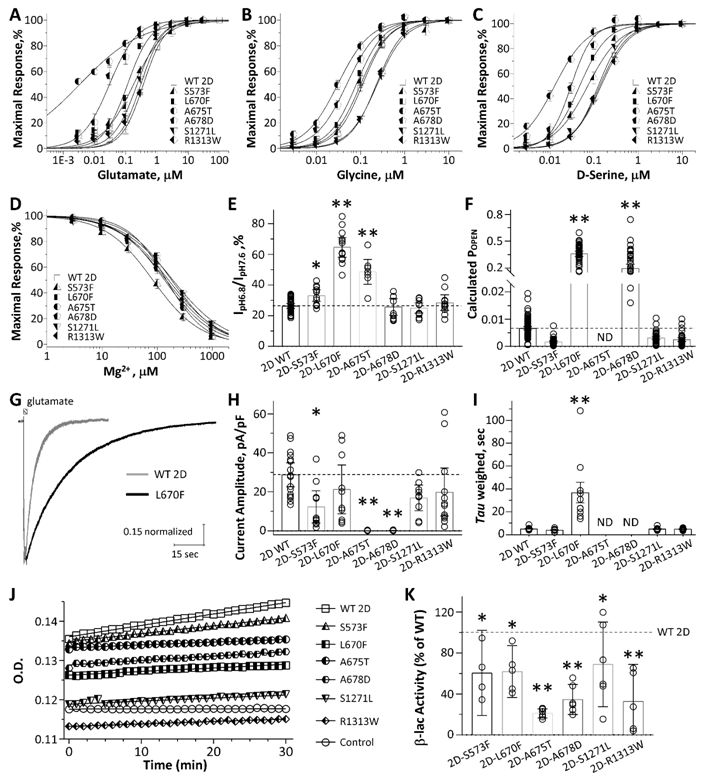
为评估突变受体的功能变化,研究记录了突变导致的多种通道激动剂效能、别构调节剂敏感性、通道开放率及谷氨酸失活时间变化情况。结果提示L670F、A675T及A678D导致受体功能增强,而S573F、S1271L及R1313W导致受体功能下降。研究进一步评估了突变受体蛋白表达量的变化。与野生型GluN2D受体相比,全部6种突变GluN2D受体的膜蛋白/总蛋白水平均有显著降低。
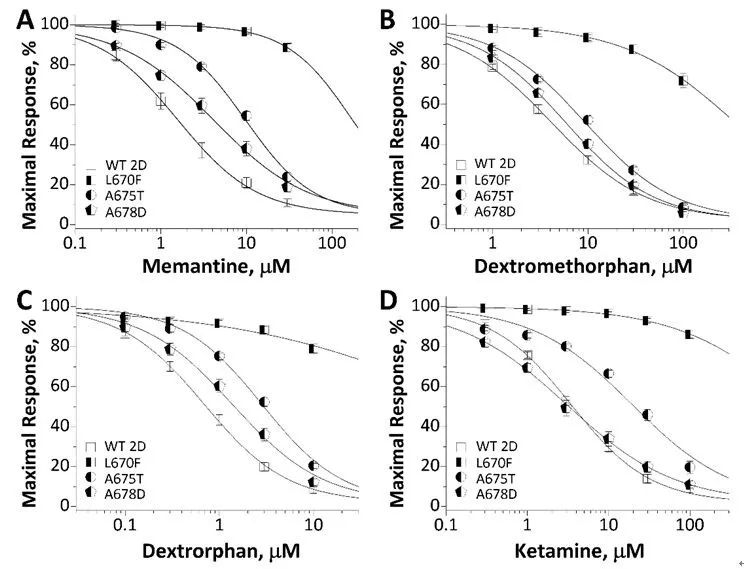
在突变分析、致病机制探究基础上,为进一步指导临床个体化治疗,该研究还在爪哇蟾蜍卵上针对导致受体电生理功能增强的3个突变L670F、A675T和A678D进行了一系列FDA批准上市的受体阻滞剂 (Memantine、Dextromethorphan、Dextrorphan和Ketamine) 的效能评估。结果显示,全部4种NMDA受体通道阻滞剂均能在不同程度上抑制野生型及突变型的GluN1/GluN2D受体。但4种药物对L670F 和A675T突变受体的抑制作用与野生型相比差异显著,提示4种药物如用于突变患者,所需剂量将远高于未突变患者;而A678D突变受体除Memantine外的3种药物的敏感性及最大剂量下的电流抑制率与野生型受体相比均没有显著差异,提示如常规抗癫痫药物无法控制A678D突变患者的癫痫发作,则Dextromethorphan及Ketamine可作为其临床个体化治疗的备选药物。
儿童神经专业
北大医院儿童神经专业一直居于国内领先地位,姜玉武教授团队多年来致力于癫痫及相关儿童神经发育障碍性疾病的致病机制及治疗研究,遗传性发育性癫痫脑病是该团队研究的方向之一,多年来已建立起一套临床诊断—遗传检测—功能验证—个体化精准治疗的诊疗研究应用一体化流程,并已建立起遗传性发育性癫痫脑病患者临床资料及样本(含iPS细胞及部分脑组织)库,某些领域已经达到国际先进水平。

论文的第一作者为北京大学第一医院博士、美国Emory大学医学院联合培养博士生相隗文殊,共同通讯作者为北京大学第一医院姜玉武教授和美国Emory大学医学院Hongjie Yuan助理教授。北京大学第一医院吴晔教授、包新华教授及张月华教授为本文共同作者。国家重点研发计划重点专项 (National Science and Technology Major Project of the Ministry of Science and Technology of China)、国家自然科学基金、北京市自然科学基金重点项目、美国NINDS、NIH、NICHD及中国国家留学基金委等项目支持。

图 文:科研处、儿科
编 辑:党院办
北京大学第一医院


