Stroke:白质增生与腔隙之间的空间关系——荷兰奈梅亨RUN DMC队列14年跟踪研究
时间:2022-10-14 14:59:02 热度:37.1℃ 作者:网络
大脑小血管疾病(SVD)是导致认知障碍和痴呆的最重要的血管因素,并导致高达25%的缺血性脑卒中。它经常出现在老年人的神经影像学中,例如白质增生(WMHs)和推定为血管来源的腔隙。从SVD的演变中下载的知识,如事件性裂隙,有助于更好地理解SVD的起源和后果。然而,导致事件性腔隙的潜在机制在很大程度上仍然是未知的。这是因为在散发性SVD的情况下,事件性裂隙是很难捕捉到的,因为它们通常是无症状的,而且发生率很低,因此需要大型的前瞻性磁共振成像(MRI)研究和长期随访。

图1: 论文封面图
新发裂隙的解剖位置可能提供有关潜在机制的额外信息。例如,基底节病变比半卵圆中心病变更常有近端栓塞源(如颈动脉狭窄、心房颤动),而位于半卵圆中心的事件性裂隙可能涉及灌注不足。同时,一项针对大脑常染色体显性动脉病伴皮层下梗塞和白质脑病(CADASIL)患者的研究发现,>90%的偶发腔隙发生在WMH的边界,这表明WMH和腔隙的发展存在联系。
然而,由于这项研究是在单基因SVD中进行的,因此外部有效性是有限的。作者试图在散发性SVD患者中证实他们的研究结果,但由于缺乏新发腔隙,这种关系只在旧腔隙中观察到。这是否可以推广到事件性裂隙中还不得而知。发生在原有的WMH中的低比例裂隙表明,WMH中只有极少数区域改变/转化为空洞,这被假设为皮质下白质裂隙的机制之一。这引起了人们的兴趣,即从其与WMH的空间关系来看,裂隙的不同病因迄今还没有被调查过。
因此,荷兰奈梅亨大学的Fang Yi等人,评估在一个随访14年的大型散发性SVD队列(RUN DMC)中发生的腔隙的空间分布模式,以及它们与WMH的关系。首先,他们描述了新发裂隙的特征,按其解剖位置和与先前存在的WMH的空间关系分层。其次,探究了基线SVD影像学标志物、WMH进展和发生裂隙之间的关系。
正在进行的前瞻性单中心Radboud University Nijmegen Diffusion 张量和磁共振队列(RUN DMC)中招募,2006年进行基线评估,2011年、2015年和2020年进行随访。2011年、2015年和2020年。382名接受过至少2次脑部MRI扫描的参与者被纳入。
系统地确定了新发腔隙,位于皮质下白质和WM的新发腔隙之间的空间关系。皮质下白质和WMH之间的空间关系用视觉评分表来确定。调整后的多元逻辑回归和 线性混合效应回归模型被用来评估基线小血管疾病标志物之间的关联。
WMH的进展和发生裂隙。多变量分析中排除了有心房颤动的参与者。结果:43名患者(平均年龄66.5±8.2岁,37.2%为女性)在平均11.2±3个月的随访中发现了80个偶发裂隙。随访时间为11.2±3.3年(发病率为10.0/1000人年)。
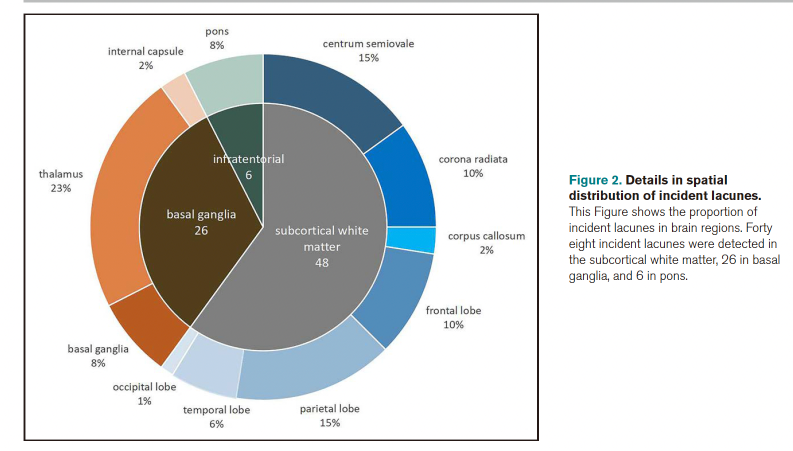
图2:论文结果图
60%发生的裂隙在白质中,其中48.9%与之前存在的WMH没有联系。基线WMH体积(HR=2.5[95%CI,1.6-4.2])。在调整了年龄、性别和血管危险因素后,可预测发生裂隙。WMH的进展与 独立于年龄、性别、基线WMH体积和血管危险因素(几率比,3.2[95%CI,1.5-6.9])。
基线WMH体积和进展率在接触预先存在的腔隙的参与者中更高。
WMH在位置或与先前存在的WMH的关系方面,没有观察到血管危险因素的差异。
该研究的重要意义在于发现了:腔隙与WMH关系的两种不同分布模式可能表明了不同的潜在机制,其中之一可能与WMH的类似病理生理学有更密切的联系。WMH和裂隙之间的纵向关系进一步支持了这两个关键标志物之间合理的共享机制。
原文出处:
Yi F, Cai M, Jacob MA, et al. Spatial Relation Between White Matter Hyperintensities and Incident Lacunes of Presumed Vascular Origin: A 14-Year Follow-Up Study. _Stroke_. Published online October 3, 2022:10.1161/STROKEAHA.122.039903. doi:[10.1161/STROKEAHA.122.039903](https://doi.org/10.1161/STROKEAHA.122.039903)


