尽管存在有效的疫苗,但乙型肝炎病毒(Hepatitis B virus, HBV)感染仍然是一个主要的全球卫生问题。大约2.4亿人患有慢性HBV感染,慢性乙型肝炎(chronic hepatitis B, CHB)患者发展为晚期肝病,包括肝硬化和肝细胞癌(hepatocellular carcinoma, HCC)的风险很高。病毒性肝炎的死亡率超过了结核病、艾滋病毒和疟疾,促使世界卫生组织宣布到2030年消除乙型和丙型肝炎的目标。
共价闭合环状DNA (covalently closed circular DNA,cccDNA)在受感染的肝细胞中的持久性是阻止现有治疗方法根除慢性乙型肝炎(chronic hepatitis B,CHB)患者病毒的主要障碍。迫切需要能够消除cccDNA的治疗药物来实现病毒根除,从而治愈HBV。
2022年12月29日,罗氏上海创新中心Lu Gao、John A.T. Young与Li Wang在Journal of Hepatology 杂志在线发表题为“Discovery of a first-in-class orally available HBV cccDNA inhibitor”的研究论文,这项研究报告了第一种口服HBV cccDNA抑制剂ccc_R08,该抑制剂是通过HBV感染原代人肝细胞(primary human hepatocytes,PHHs)高通量筛查(high-throughput screening,HTS)鉴定出来的。
在HBVcircle小鼠模型中,ccc_R08表现出降低血清中HBsAg、HBeAg、HBV DNA和pgRNA水平以及降低肝脏中cccDNA水平的强大能力。这些数据表明,ccc_R08是一种特异性的HBV cccDNA抑制剂,鼓励在临床中探索这类分子,以评估其完全治愈慢性HBV感染的潜力。总之,这项研究发现了一种可以降低HBV cccDNA水平的小分子cccDNA抑制剂。cccDNA抑制剂可能是一种完全治愈慢性HBV感染患者的新方法。

目前的指南明确了功能性治愈或HBsAg的丢失(无论是否HBsAg血清转化)作为CHB治疗的理想终点,因为持续的HBsAg丢失与发展为晚期肝病的风险显著降低相关。目前的护理标准(standards of care, SoCs),包括核酸(nucleos(t)ides, NUCs)和聚乙二醇化干扰素α (interferon α, IFNα),可以抑制HBV复制,但很少实现功能性治愈。迫切需要能够提高功能性治愈率甚至病毒根除率(定义为消除病毒cccDNA基因组)的治疗性疗法。
HBV是一种非细胞病变DNA病毒,在受感染的肝细胞的细胞核中产生共价闭合环状DNA (cccDNA)小染色体。cccDNA作为所有病毒前基因组RNA (pgRNAs)和病毒mRNA的转录模板,分别产生循环DNA病毒粒子和病毒抗原。HBV cccDNA半衰期长,感染细胞中的cccDNA库可通过新一轮感染和细胞内扩增进行补充。虽然NUCs的管理导致有效的病毒血症抑制,cccDNA在长期治疗后仍然存在。IFNα处理也不能消除cccDNA。当持续HBsAg缺失的患者接受化疗、免疫抑制治疗或造血干细胞移植时,会发生HBV再激活。因此,清除这种长寿命的病毒基因组库构成了阻止病毒根除的主要障碍。
针对cccDNA的多种抗病毒方法正在探索中。间接策略旨在通过使用进入抑制剂防止新一轮感染或阻断cccDNA形成的关键步骤来减少cccDNA池。据报道,HBV核心蛋白变构调节剂(core protein allosteric modulators, CpAMs)可以阻断HBV衣壳的正常组装,在感染的早期步骤抑制cccDNA的从头形成。CCC-0975是一种双取代磺胺(disubstituted sulfonamide, DSS)抑制剂,被发现可以通过干扰HepDE19/HepDES19细胞系中cccDNA从RC-DNA的转化来抑制cccDNA的形成。这些cccDNA形成抑制剂被证明可以阻止新合成的cccDNA的形成,但不影响已建立的cccDNA池。从感染细胞中清除已建立的cccDNA是实现cccDNA清除的更直接和有效的方法。
基因组编辑技术,包括锌指核酸酶(ZFNs)、转录激活剂样效应核酸酶(TALENs)和聚束规则间隔短回文重复序列/CRISPR相关(CRISPR/Cas)系统,已被探索用于编辑培养细胞中的cccDNA。基于CRISPR/ cas9的方法导致超过90%的cccDNA总分子发生突变和缺失,导致cccDNA失活。然而,一小部分cas9切割的cccDNA分子被框架内突变体修复。此外,这些基因组编辑方法还面临着传递到所有感染肝细胞的技术障碍、整合HBV DNA的切割、随后的染色体重排以及对宿主基因组的潜在脱靶效应的挑战。
其他可能消除cccDNA的方法包括使用抗病毒细胞因子淋巴毒素β受体(LTβR)激动剂、IFNα、IFNγ和TNFα治疗。因此,目前迫切需要发现一种有效的新型口服cccDNA抑制剂,可以减少cccDNA池并最终消除cccDNA。
在这项研究中,研究人员用HBV感染的原代人肝细胞(primary human hepatocytes,PHHs)进行表型试验,以筛选新的cccDNA抑制剂。采用HBVcircle小鼠模型和尿激酶型纤溶酶原激活剂-严重联合免疫缺陷(urokinase-type plasminogen activator-severe combined immunodeficiency,uPA-SCID)人源化肝脏小鼠模型来评估所发现的cccDNA抑制剂的抗HBV疗效。
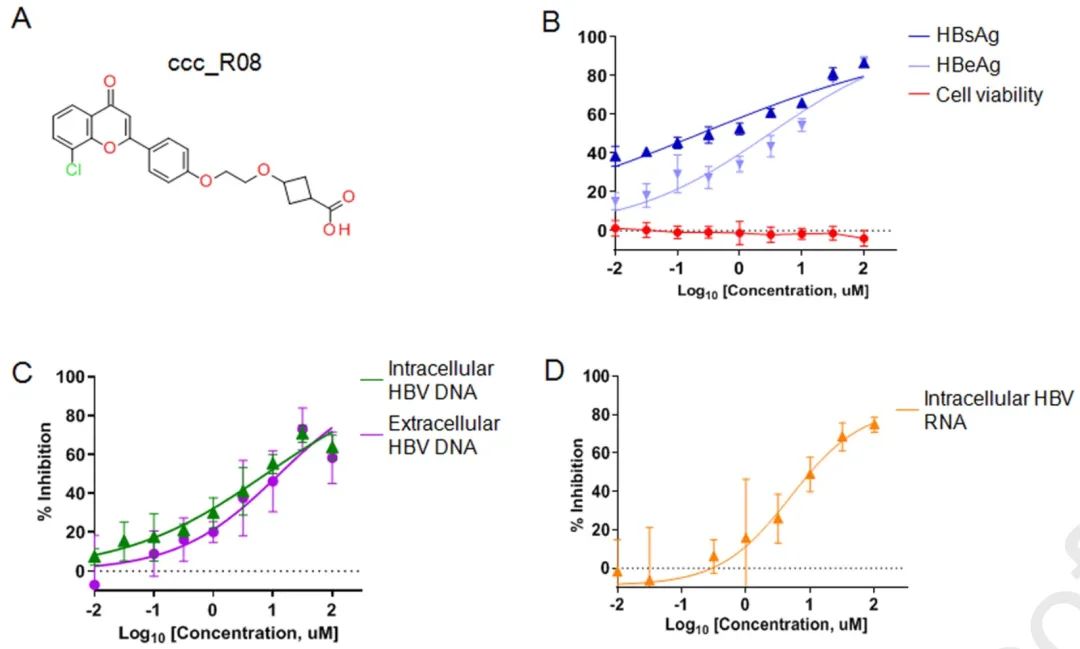
研究结果表明,在PHHs HBV感染两天后开始ccc_R08治疗后,细胞外HBV DNA、HBsAg和HBeAg水平实现了强有力的剂量依赖性降低。更重要的是,ccc_R08特异性降低了cccDNA水平,而对线粒体DNA没有明显影响。此外,ccc_R08在PHHs或多个增殖细胞系中没有显着的细胞毒性。
图1. ccc_R08对HBV感染PHHs的抗病毒作用(图源自Journal of Hepatology )
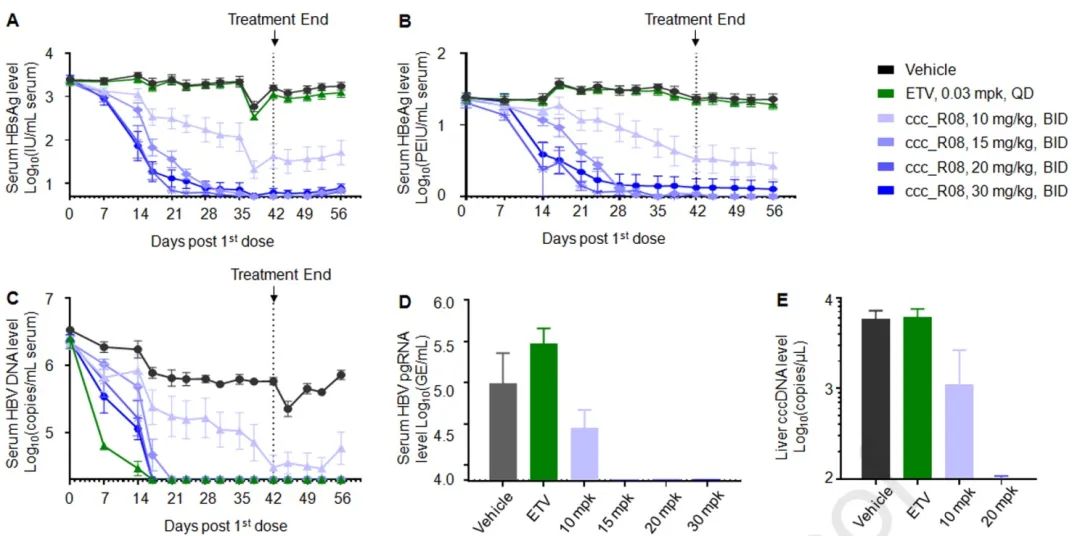
含有替代cccDNA分子的HBVcircle模型小鼠每天口服两次ccc_R08,显著降低了HBV DNA和抗原的血清水平,并且这些影响在非治疗随访期间持续。此外,在随访结束时,ccc_r08处理的HBVcircle小鼠肝脏中的替代cccDNA分子水平降低到定量下限(lower limit of quantification,LLOQ)以下。
图2. ccc_R08对HBVcircle小鼠模型血清pgRNA水平的影响(图源自Journal of Hepatology )
综上所述,cccDNA在HBV感染肝细胞中的持续存在是慢性乙型肝炎的根本原因。这项研究发现了一种新的小分子cccDNA抑制剂,可以特异性地降低HBV感染肝细胞中的cccDNA水平。这类分子为彻底治愈慢性HBV感染患者提供了一种新的途径。
原文链接:
https://doi.org/10.1016/j.jhep.2022.12.014