Nature子刊 | 山东大学刘联团队发现晚期胃癌的潜在治疗新方法
时间:2023-01-06 12:01:23 热度:37.1℃ 作者:网络
尽管进行了新辅助/转化化疗,但cT4a/bN+胃癌的预后较差。免疫检查点抑制剂(ICI)和抗血管生成药物在晚期胃癌中显示出活性,但它们在新辅助/转化情况下的疗效尚不清楚。
2023年1月3日,山东大学刘联团队在Nature Communications 在线发表题为“Neoadjuvant therapy with immune checkpoint blockade, antiangiogenesis, and chemotherapy for locally advanced gastric cancer”的研究论文,该研究进行了一项单臂性II期探索试验,评估了ICI (camrelizumab)、抗血管生成(apatinib)和化疗(S-1±奥沙利铂)联合应用于cT4a/bN+胃癌新辅助/转化治疗的疗效。
结果表明,完全和主要病理缓解率分别为15.8%和26.3%。病理反应与微卫星不稳定状态、PD-L1表达和肿瘤突变负荷显著相关。此外,多组学检查揭示了几种病理反应的假定生物标志物,包括RREB1和SSPO突变、免疫相关特征和外周T细胞扩增评分。多组学还证明了新辅助免疫治疗期间显性肿瘤亚克隆、免疫微环境和T细胞受体库的动态变化。毒性和术后并发症有限。这些数据支持在大型随机试验中进一步验证基于ICI和抗血管生成的新辅助/转化疗法,并提供候选生物标志物。

胃癌仍然是全球的主要杀手,发病率排名第五,死亡率排名第四。根治性切除是治疗和延长生存期的最佳选择。在之前的MAGIC和FFCD临床试验中,围手术期化疗的5年生存率高于单纯手术。与不使用紫杉醇的方案相比,FLOT方案进一步提高了R0切除术率,延长了总生存期(OS) 。然而,cT4患者在该试验中所占比例不到10%。
在最近的PRODIGY研究中,新辅助DOS方案(多西他赛、奥沙利铂和S-1[Tegafur/Gimestat/Oxonate])和辅助S-1显著提高了术后 S-1 的3年无进展生存期(PFS)率(66.3个月vs 59.8个月),并导致10.4%的病理完全缓解。虽然在本试验中70%的患者为cT4,但cT4a患者的比例高达89%。此外,cT4N+组的预后低于cT4N-和cT2-3N+组,并且没有单独针对cT4bN+患者的亚组分析。
最近,在三期随机对照试验中,免疫检查点抑制剂(ICIs)在晚期胃癌的三线治疗中取得了优于安慰剂的结果。在一线治疗中,在CheckMate 6498和ORIENT169中PD-L1 CPS≥5的患者中,联合ICI和化疗相比单独化疗延长了OS和PFS,并将死亡风险降低了20-35%。理论上,由于免疫系统完整,新抗原充足,肿瘤克隆性低,新辅助治疗环境是免疫治疗的最佳选择。基于ICI的新辅助治疗已成功用于可切除的非小细胞肺癌。在胃癌中,特别是在局部进展期胃癌中,化疗的作用仍未完全探索。
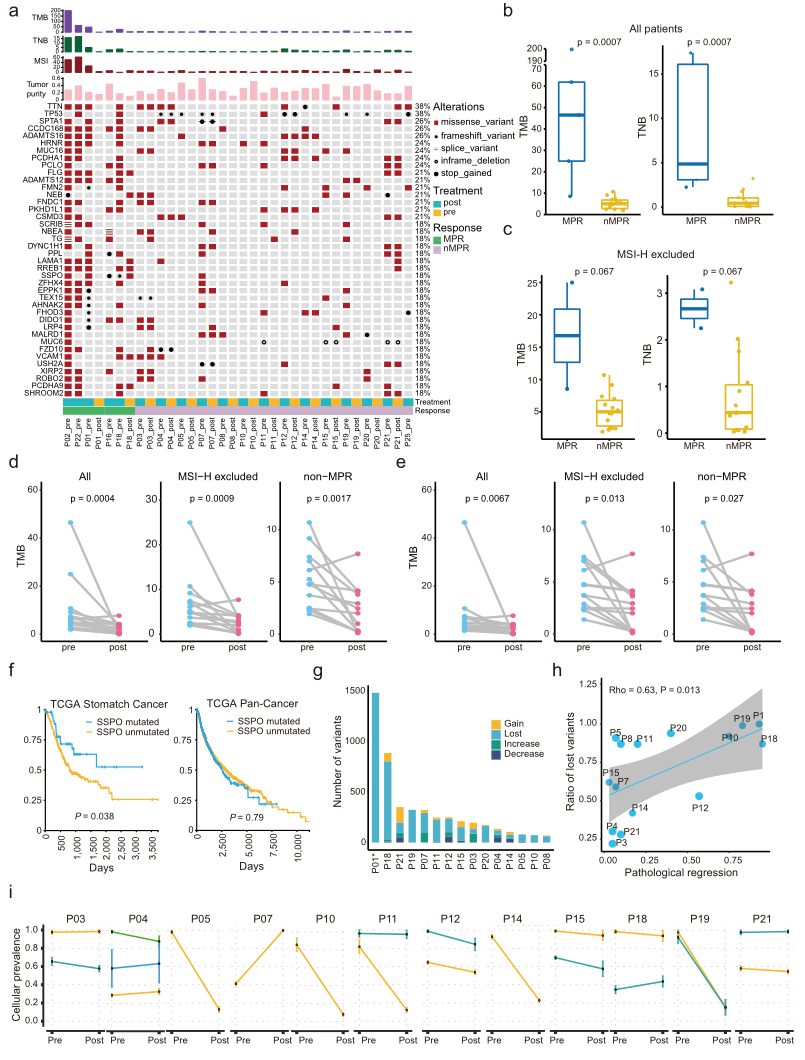
新辅助治疗后的基因组特征和克隆进化(图源自Nature Communications )
肿瘤血管生成在肿瘤发展过程中起着重要作用。与ICIs一样,抗血管生成药物靶向肿瘤微环境(TME)成分,而不是肿瘤细胞,并通过促进CD8+ T淋巴细胞浸润和激活与ICIs协同作用。Ramucirumab(一种抗VEGFR2抗体)和apatinib(一种VEGFR2酪氨酸激酶抑制剂)已被证明可延长OS,并分别被批准用于晚期胃癌的二线和三线治疗。在一些I/II期研究中,它们已被证明可以重编程TME,将免疫抑制逆转到炎症状态,并增强ICIs的疗效。因此,在ICIs加化疗方案中加入抗血管生成药物可能会增强新辅助治疗的疗效。
在这项II期试验中,作者的数据表明,基于ICI和抗血管生成的新辅助/转化治疗在cT4a/bN+胃癌,尤其是MSI-H和PD-L1阳性患者中具有良好的疗效和可行性。如何提高其在MSS和PD-L1阴性患者中的疗效有待进一步探索。多组学研究结果提供了一些候选的与疗效相关的生物标志物,并帮助理解治疗反应和耐药的机制。
原文链接:
https://www.nature.com/articles/s41467-022-35431-x


