Cell:厦门大学王科嘉揭示镇痛药通过脆弱性调节性T细胞引起戒断症状
时间:2023-01-26 15:01:53 热度:37.1℃ 作者:网络
阿片类药物是目前临床广泛使用的镇痛药物,能够劫持脑中的奖赏通路,引起成瘾。伏隔核(NAc)是协调奖赏和厌恶过程的主要脑区。吗啡诱导的NAc区域形态重塑与行为敏化、依赖和戒断有关。此外,吗啡可促进炎症因子的分泌,加重神经免疫反应。
调节性T细胞(Tregs )是一类控制体内自身免疫反应性的T细胞亚群,其标志物为叉头盒转录因子Foxp3,该功能性细胞群缺失后引起致命的自身免疫性疾病。Tregs细胞缺失神经纤毛蛋白1(Nrp1)引起该免疫细胞群功能脆弱,失去了免疫抑制作用,能够分泌干扰素-γ,这类细胞群被称为脆弱性Tregs细胞。

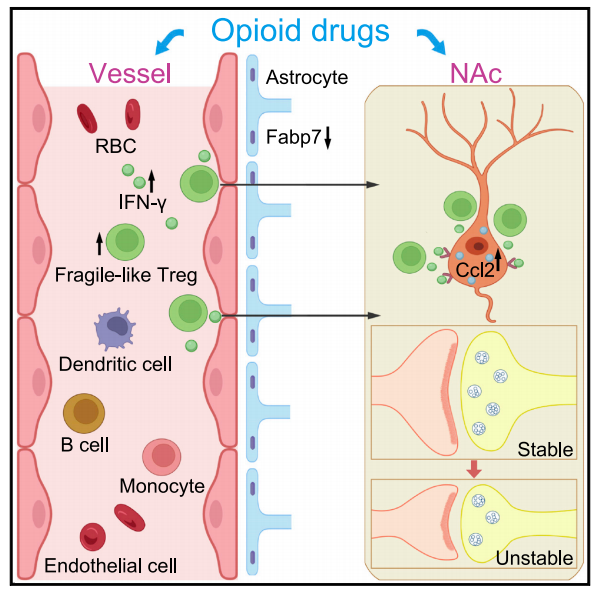
2023年1月20日厦门大学医学院王科嘉、梁青研究团队在Cell杂志上发表文章揭示了吗啡驱动外周脆弱Tregs细胞通过血脑屏障进入大脑,通过干扰素-γ引起NAc区域突触可塑性不良变化,引起戒断症状。
1
吗啡引起外周脆弱性Tregs细胞增加
研究人员通过对阿片类使用障碍患者血液进行分析,发现外周脆弱Tregs细胞数量增多,并且与患者戒断得分呈正相关。小鼠在接受吗啡处理后肝脏、血液、脾脏等多个外周器官中Tregs来源干扰素-γ水平升高,将这些脆弱性Tregs细胞与正常Tregs细胞离体培养后可明显增加正常Tregs细胞干扰素-γ水平,敲除干扰素-γ后可明显降低脆弱性Tregs细胞数量。进一步实验发现阿片类药物并不直接引起脆弱性Tregs细胞的出现,而是通过缺氧引起这一病理现象。
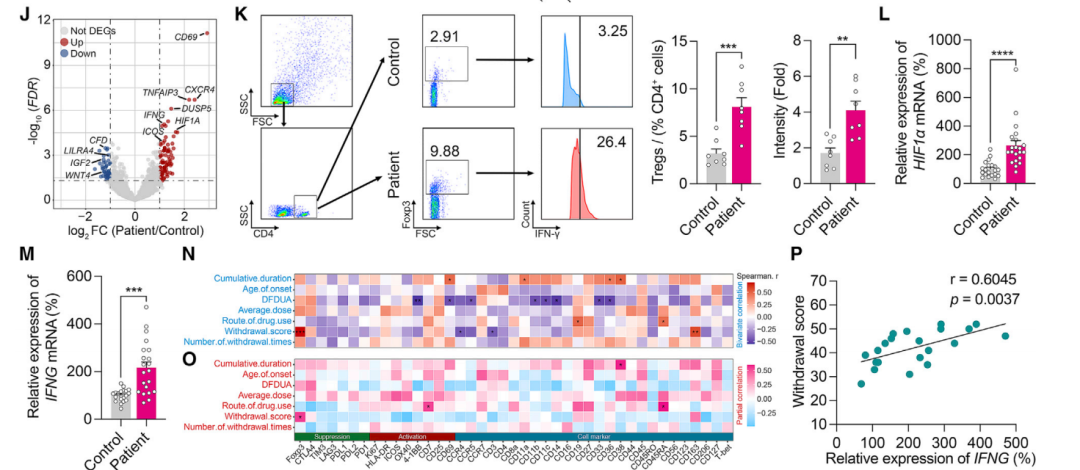
图1:吗啡引起外周脆弱性Tregs细胞增加
2
吗啡通过趋化因子募集外周性脆弱性
Tregs细胞进入NAc区域
小鼠在接受吗啡处理后NAc区域干扰素-γ水平升高,脆弱性Tregs细胞增多,这种增加并不是来自于NAc区域常驻Tregs细胞,而是来源于外周脆弱性Tregs细胞浸润。形态学实验表明吗啡引起NAc区域未成熟的突触数量增多,兴奋性突触功能减弱。敲除Ifng(编码干扰素-γ)能明显缓解吗啡引起NAc区域突触可塑性变化,并能改善戒断后症状。
已有研究表明Tregs细胞转运依赖于趋化因子Ccl12、Ccl19、Ccl21。研究人员发现吗啡引起NAc区域Ccl12水平增加,并不引起Ccl19和Ccl21水平的增加。通过特异性敲除Tregs细胞Ccr2(Ccl12受体)可明显减少外周脆弱性Tregs细胞浸润,并能改善戒断症状。
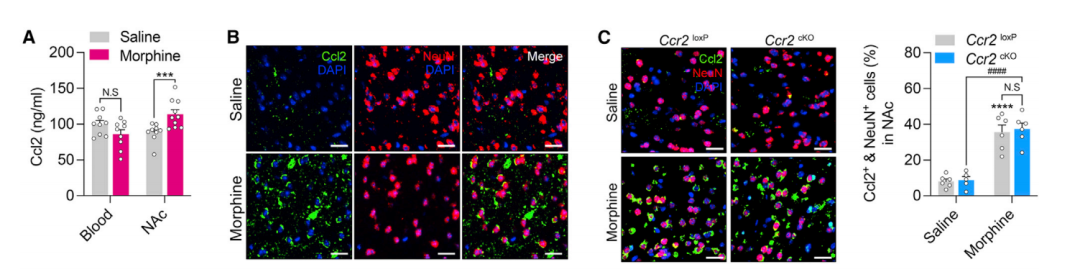
图2:吗啡通过趋化因子募集外源性脆弱性Tregs细胞进入NAc区域
3
吗啡通过Fabp7破坏血脑屏障促进T细胞浸润
正常生理状态下外周Tregs细胞无法通过血脑屏障进入大脑实质中,那么吗啡是如何引起血脑屏障通透性增加的尼?研究人员通过免疫荧光实验发现吗啡能够引起NAc区域血脑屏障障碍。单细胞测序发现脂肪酸结合蛋白7(Fabp7,调控血脑屏障通透性)是吗啡引起NAc区域差异性表达的基因。免疫荧光实验发现大脑星形胶质细胞是Fabp7的主要来源。
进一步通过实验发现吗啡引起NAc区域星形胶质细胞Fabp7表达降低,特异性增加星形胶质细胞Fabp7表达后能够降低该区域干扰素-γ水平,减少脆弱性Tregs细胞数量,也能够改善突触可塑性和戒断症状。这些结果表明Fabp7参与吗啡引起的血脑屏障功能障碍。

图3:吗啡通过Fabp7破坏血脑屏障促进T细胞浸润
总结
本文发现阿片类药物通过引起缺氧增加外源性脆弱性Tregs细胞数量,并增加大脑血脑屏障通透性,促进脆弱性Tregs细胞浸润到NAc区域,引起突触结构可塑性变化,调控戒断症状。
原始出处:
Zhu et al., Opioid-induced fragile-like regulatory T cells contribute to withdrawal, Cell (2023).


