【Br J Haematol】来那度胺联合R-ESHAP治疗R/R DLBCL的II期研究
时间:2023-08-07 13:30:38 热度:37.1℃ 作者:网络
LR-ESHAP
在过去三十年中,复发或难治性弥漫大B细胞淋巴瘤(R/R DLBCL)患者的标准治疗是大剂量化疗联合自体干细胞移植(ASCT),但其前提是患者对挽救性免疫化疗有反应。然而既往接受利妥昔单抗治疗的患者对标准挽救治疗方案的反应较差,超过半数的患者因治疗未能充分降低肿瘤负荷而未接受ASCT,因此这些患者需要进行纳入新药的前瞻性研究。
来那度胺单药或联合利妥昔单抗均在R/R DLBCL的挽救治疗中均显示了疗效,血液学和非血液学毒性的发生率可接受;基于临床前模型的体外协同作用,它也可能与ESHAP(依托泊苷、甲泼尼龙、阿糖胞苷、顺铂)方案发挥协同作用。这一发现得到1b期临床试验支持,显示来那度胺(10mg,21天/周期,第1~14天给药,作为最大耐受剂量)加用挽救性R-ESHAP(LR-ESHAP)是一种安全可行的方案,可获得有希望的缓解率和生存结局:完全缓解率和总有效率分别为47.4%和78.9%,中位随访24.6个月,2年无进展生存率和总生存率分别为44%和63%。
鉴于该结果,学者进一步开展了一项2期研究,旨在提供来那度胺联合R-ESHAP治疗难治性/复发性DLBCL患者的疗效和安全性的进一步信息。I/II期研究结果近日发表于《British Journal of Haematology》。

研究设计
该研究纳入患者要求包括:18-70岁,组织学确诊为DLBCL或基于局部组织学的3B级滤泡性淋巴瘤(FL),持续(一线治疗未完全缓解)或利妥昔单抗联合含蒽环类方案一线治疗后复发,有≥1个可测量病灶,基线PET显示阳性病灶,与计算机断层扫描(CT)确定的解剖肿瘤部位一致, ECOG体能状态为0-2,适合ASCT。
患者在每个21天/周期的第1-14天接受10mg来那度胺每日一次,联合标准剂量的R-ESHAP挽救化疗(利妥昔单抗第1天375mg/m2,依托泊苷第1-4天40mg/m2,顺铂第1-4天25mg/m2;阿糖胞苷第5天2000mg/m2和甲泼尼龙第1-5天500mg)。
所有患者均接受培非格司亭(第+ 6天6mg)或非格司亭(第+ 6天≥5 μg/kg/d,直至中性粒细胞恢复)。由治疗医生酌情提供抗血栓预防和支持治疗。在第2周期挽救治疗期间,用粒细胞集落刺激因子(G-CSF)动员干细胞并采集;如有必要,在第3个周期后进行第二次动员。3个周期LR-ESHAP后达到CR或部分缓解(PR)的患者接受BEAM(卡莫司汀、依托泊苷、阿糖胞苷和美法仑)预处理和ASCT。
研究结果
患者特征
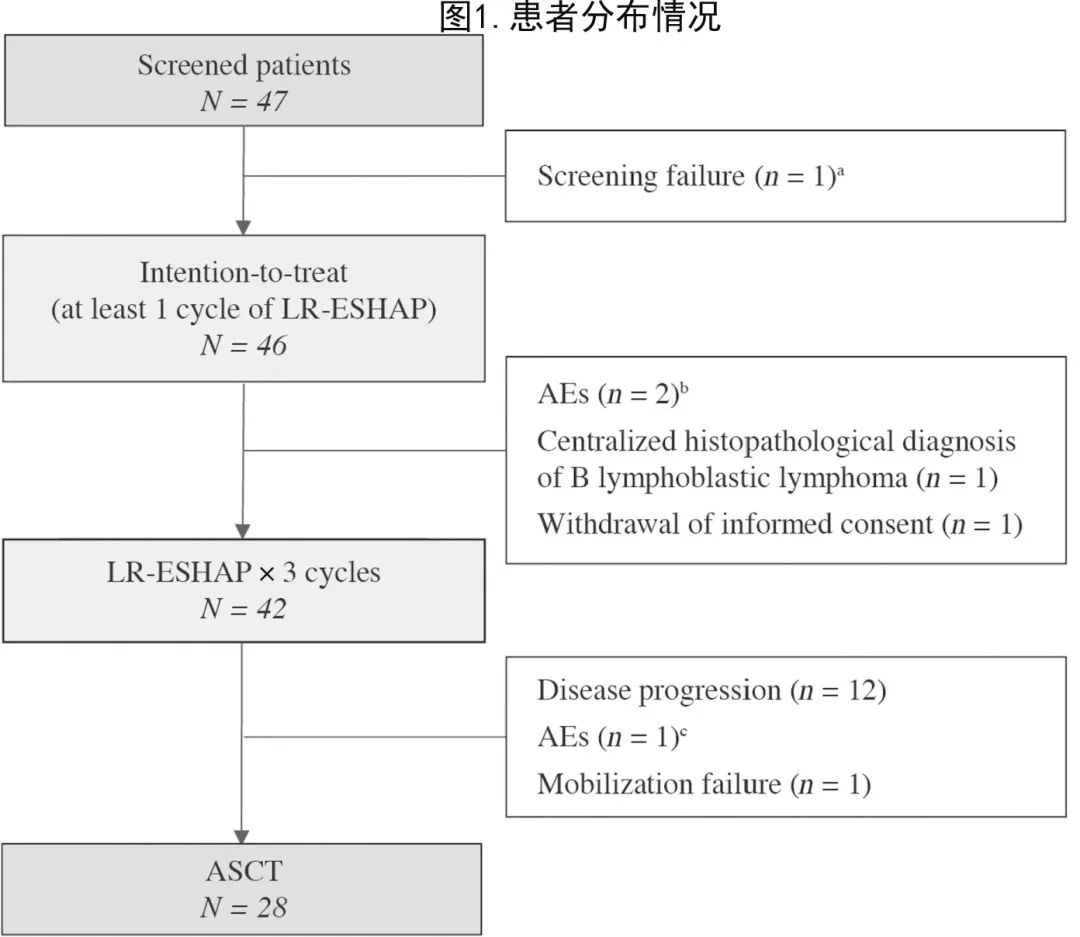
共46例入组研究(图1),其中12例在I期研究期间接受最大耐受剂量给药,34例在II期入组。
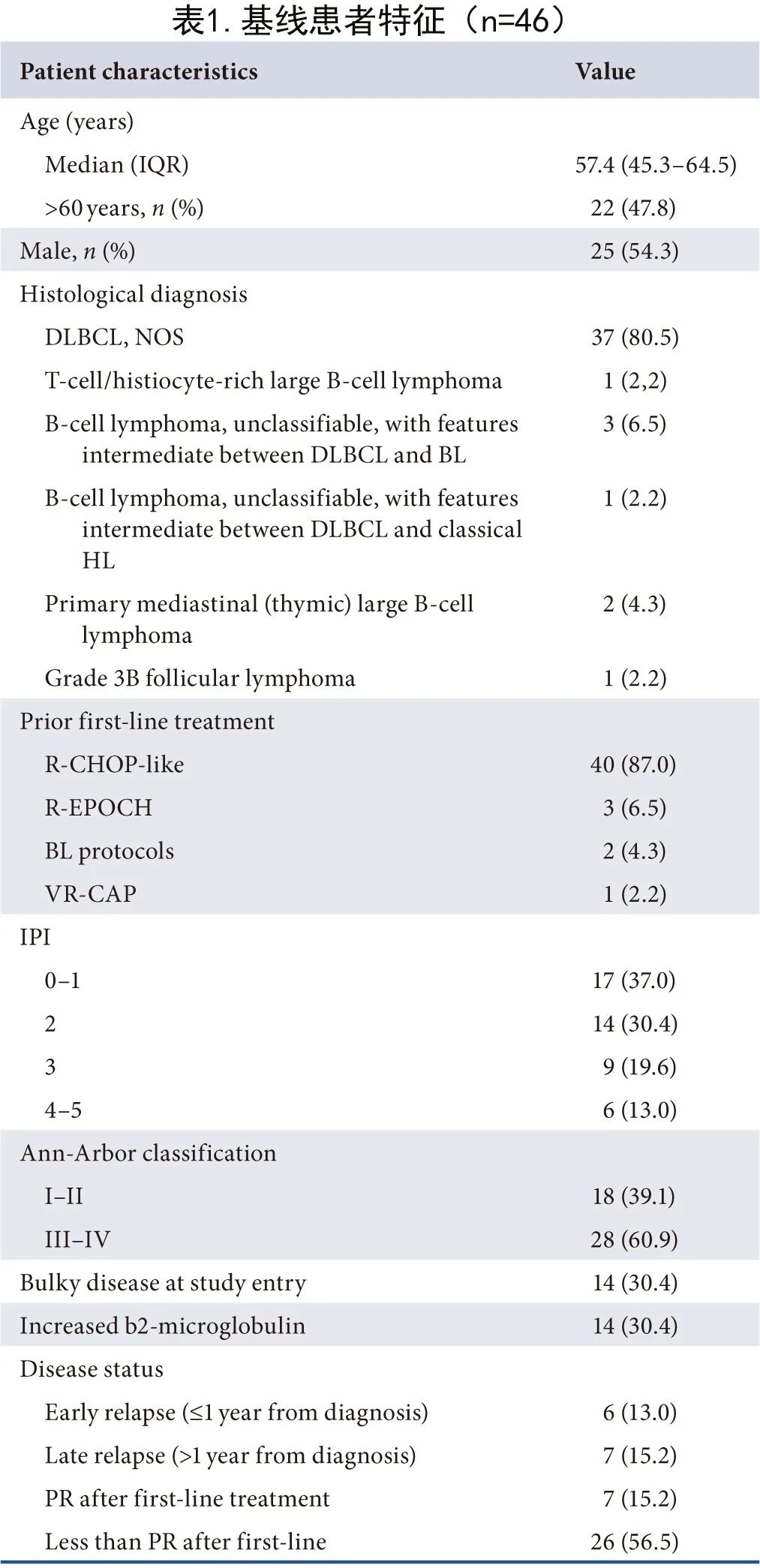
基线患者特征见表1,大部分患者(85%)为原发难治性疾病、一线后PR或早期复发(距诊断时间<1年)。尽管本研究的入组是基于当地组织学,但在具有诊断和/或复发肿瘤样本的患者(n=34)中进行了集中组织学审查,结果显示3例(9%)DLBCL的组织学不同(1-2级FL[n=1],3A级FL[n=1]和B细胞淋巴母细胞淋巴瘤[n=1])。
可行性
患者分布见图1。42例(91%)患者接受了计划的3个周期LR-ESHAP治疗。1例(2%)患者因撤回知情同意仅接受了2个周期,3例(7%)患者在第1周期因AE(分别为乳突炎、肺炎和诊断B细胞淋巴母细胞淋巴瘤)而中止治疗。46例患者接受128个周期治疗。
在第2个(n=23)或第3个(n=11)周期后,40例患者(87%)接受了G-CSF或G-CSF+普乐沙福的干细胞动员,7例患者需要第二次动员;除1例患者外,所有患者均成功动员(CD34+ 细胞≥2 × 106/kg)。28例(61%)患者按照方案接受了ASCT;12例(26%)患者因疾病进展(PD)未接受ASCT(3例在周期2后,9例在周期3后),5例(11%)患者因治疗中止(中心诊断为淋巴母细胞淋巴瘤[n=1]、撤回知情同意[n=1]、AE[n=2]和周期3后诊断结肠腺癌 [n=1]),1例(2%)患者因动员失败。
疗效
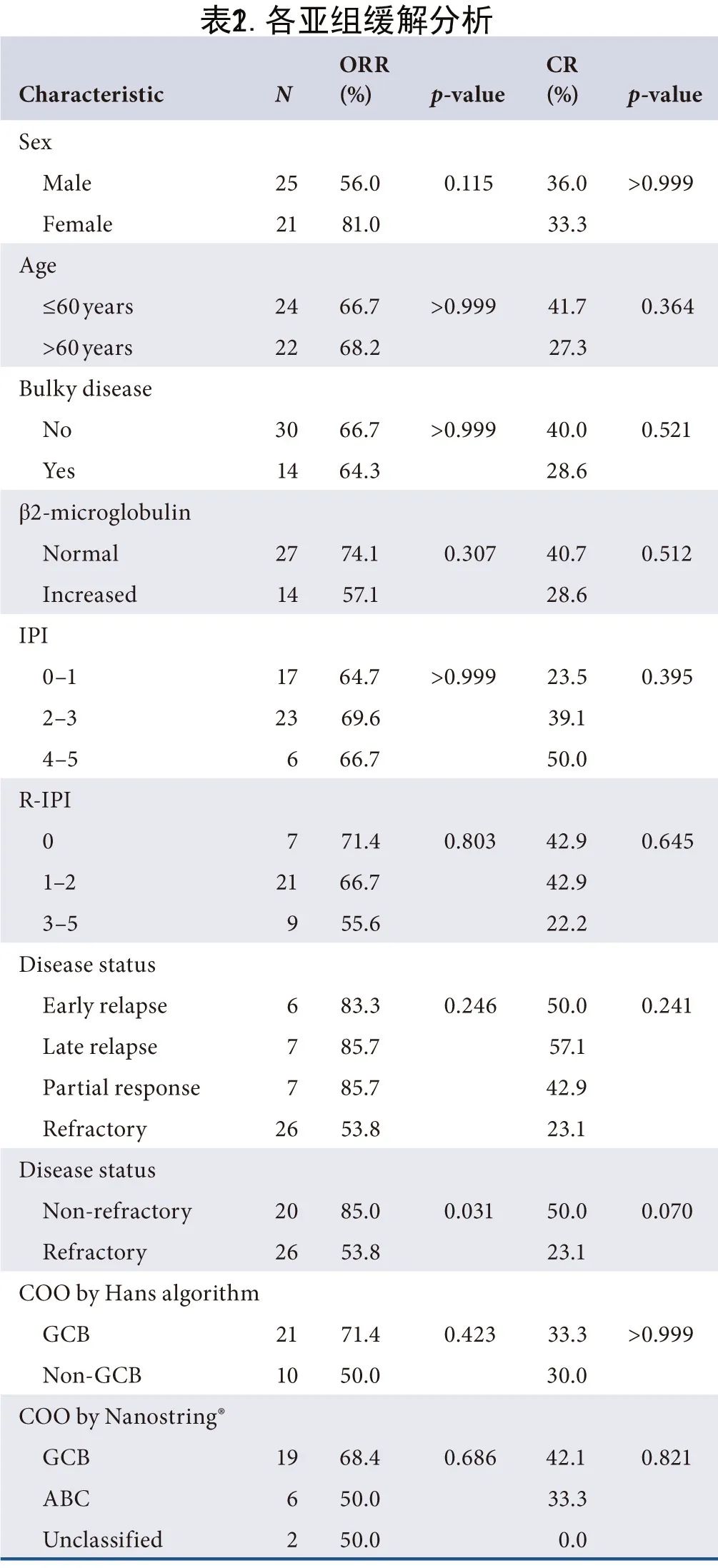
ITT人群(n = 46)接受3个周期LR-ESHAP治疗后的ORR和CR率分别为67%和35%。缓解的亚组分析见表2。只有进入研究时的疾病状态对缓解率有显著影响;非难治性疾病患者的ORR显著更好(85% vs. 54%,p=0.031),而CR率具有优于难治性疾病患者的趋势(50% vs. 23%,p=0.07)。基于COO(通过Hans算法确定[n=31]和Nanostring [n=27])未观察到缓解率差异(表2)。
中位随访41个月,20例患者疾病已进展,其中19例已死于淋巴瘤。中位PFS(图2A)、OS(图2B)和EFS(图2 C)分别为16个月、22个月和7个月,估计的3年PFS、OS和EFS分别为42%、48%和38%。
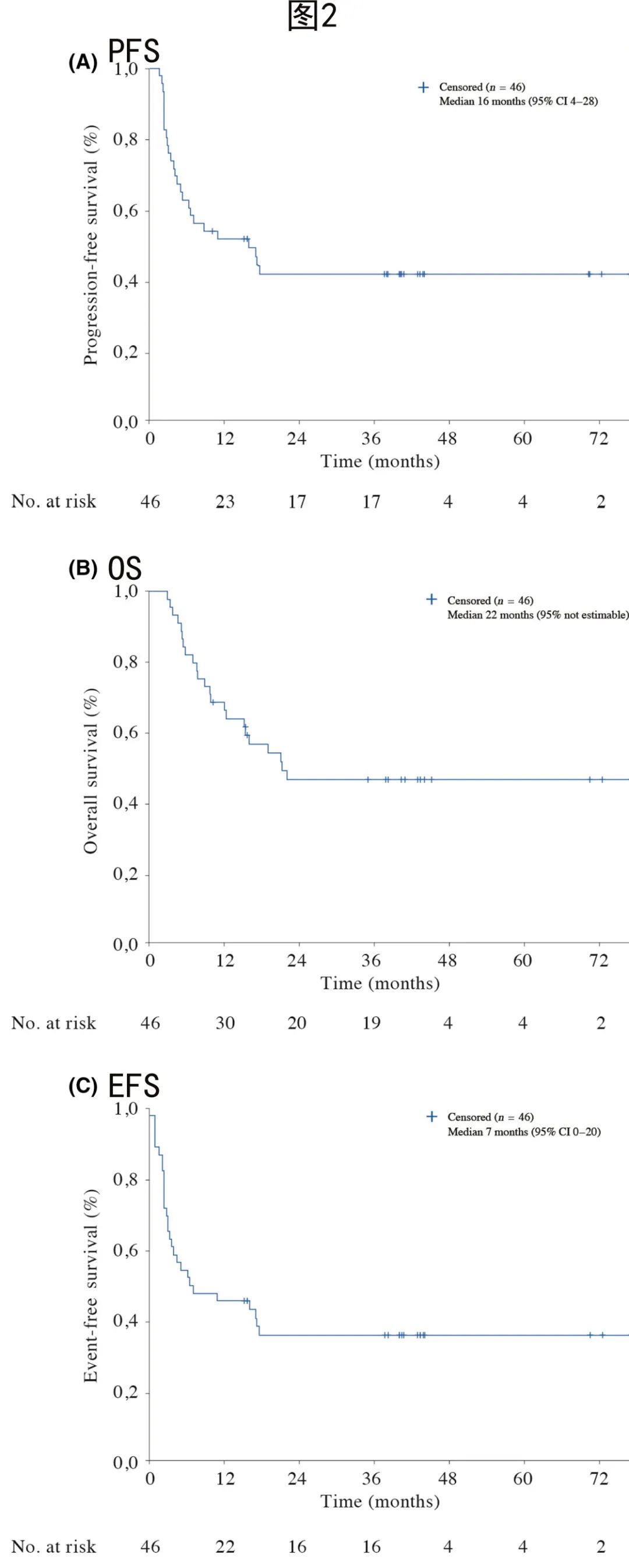
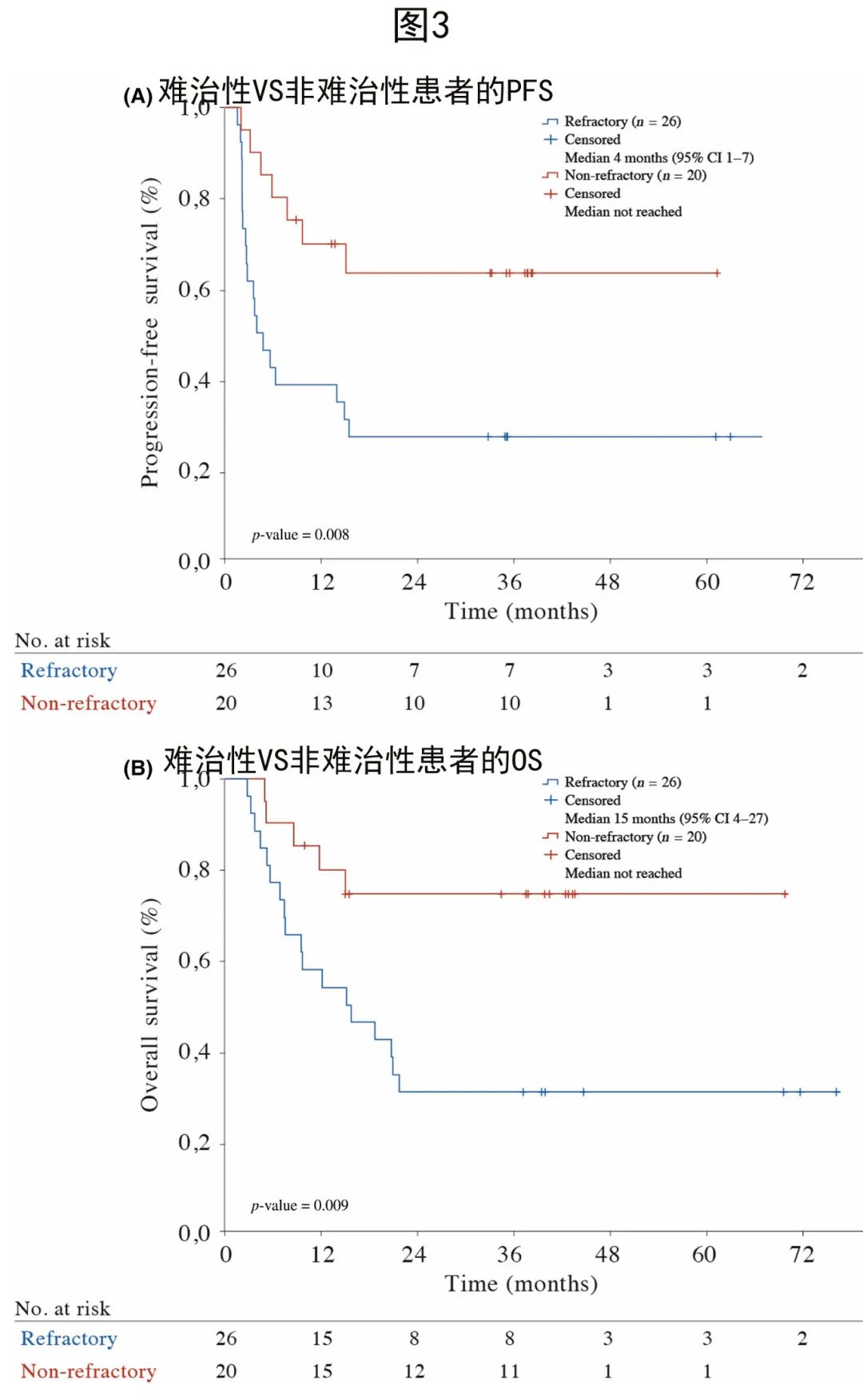
原发难治性患者的PFS和OS显著较差(图3),中位PFS和OS分别为4和15个月,而一线后早期复发、晚期复发或PR患者未达到中位PFS和OS。原发性难治性患者的估计3年PFS和OS分别为27%和31%,早期复发患者分别为56%和83%,晚期复发患者为71%和71%,一线后PR患者为57%和71%。根据其他预后因素或COO,未观察到PFS或OS差异。
排除集中审查中诊断的1例淋巴母细胞淋巴瘤和2例惰性FL后重复进行疗效分析,结果与整个系列非常相似。LR-ESHAP治疗3个周期后的ORR和CR率分别为67%和35%,中位PFS和OS分别为17个月和未达到。
安全性
表3总结了LR-ESHAP周期内的血液学和非血液学AE。最常见的3级或4级AE是血小板减少(70%的患者)、中性粒细胞减少(67%)、贫血(35%)、发热性中性粒细胞减少(24%)和淋巴细胞减少(24%)。3例(7%)患者发生血栓事件:1例治疗相关肺栓塞和2例中心静脉导管相关深静脉血栓形成。LR-ESHAP周期内未发生治疗相关死亡。

ASCT后的毒性,28例患者中的27例在中位12天(IQR,10.5-19.0)和12天(IQR,7.5-16.5)后植入,分别达到中性粒细胞超过0.5 × 109/L和血小板超过20 × 109/L;1例患者移植失败,在ASCT后9个月接受了异基因干细胞移植,最终死于肝窦阻塞综合征。1例患者在ASCT后第+ 20天死于屎肠球菌和铜绿假单胞菌肺部感染。ASCT后报告的其余AE均符合预期且可逆。
发生2例继发性肿瘤:1例在第3个LR-ESHAP周期后发生结肠腺癌,1例在ASCT后11个月发生甲状腺乳头状癌。
总结
该研究是第一项评估来那度胺与R-ESHAP联合治疗的研究,纳入46例R/R DLBCL患者给予LR-ESHAP方案治疗,LR-ESHAP后的ORR为67%(35%的患者达到CR)。原发难治患者(n=26)的ORR显著差于非难治性患者(54% vs. 85%,p=0.031);根据COO则未观察到缓解率差异。患者中28例(61%)行ASCT。中位随访41个月,估计的3年PFS和OS分别为42%和48%。最常见的≥3级不良事件为血小板减少(70%)、中性粒细胞减少(67%)和贫血(35%)。LR-ESHAP周期内未发生治疗相关死亡。
总之,LR-ESHAP是一种可行的挽救治疗方案,对于适合ASCT的R/R DLBCL患者具有高缓解率和良好生存结局。尽管研究人群有限,但考虑到患者的预后较差,结果还是有希望的,毕竟大多数患者为原发难治或早期复发(85%为原发难治性疾病、一线后PR或早期复发,仅15%为晚期复发)。
参考文献
Martín García-Sancho A, et al. Lenalidomide in combination with R-ESHAP in patients with relapsed or refractory diffuse large B-cell lymphoma: A phase 2 study from GELTAMO.Br J Haematol . 2023 Jul 23. doi: 10.1111/bjh.18989.


