安徽医科大学张群林教授《ACS AMI》:基于pH调控的多色金纳米团簇构建的ROS响应型荧光传感器阵列用于癌症精准诊断
时间:2023-08-08 19:30:15 热度:37.1℃ 作者:网络
癌症的早期诊断对其治疗以及预后评估均具有重要意义。目前基于抗体的检测方法包括组织病理学、生物成像和光学/电化学生物传感已被广泛应用,但它们依然面临着一些问题,如肿瘤细胞标志物的缺乏、抗体本身的高成本和固有免疫原性。活性氧(ROS)是生物体内具有高反应活性的自由基。大量研究表明肿瘤微环境由于肿瘤细胞代谢异常,通常具有高氧化应激状态,其特点是升高的ROS水平通过触发各种信号通路促进癌细胞增殖。因此,异常的ROS水平已经成为肿瘤细胞的重要标志物之一。鉴于此,细胞内ROS的模式识别可成为癌症精准诊断的有效策略。然而,基于该策略的检测方法尚未见报道。
2023年8月2日,安徽医科大学药学院张群林教授团队开发了一种基于多色组氨酸金纳米团簇(AuNCs@His)的ROS响应型荧光传感器阵列用于癌症精准诊断。相关工作以 “ROS-Responsive Fluorescent Sensor Array for Precise Diagnosis of Cancer via pH-Controlled Multicolor Gold Nanoclusters” 为题发表在《ACS Applied Materials & Interfaces》上。

在本研究中,作者通过调控pH值成功合成三种分别发射蓝色、绿色和黄色荧光的AuNCs@His,并以此构建ROS响应的荧光传感器阵列。由于细胞内源性ROS种类和水平的差异,导致三种AuNCs@His被细胞摄取后呈现不同程度的荧光淬灭响应,这种信号响应模式形成了独特的光学 “指纹图谱”,可进一步通过主成分分析(PCA)有效地识别不同的细胞株(图1)。综上所述,该研究工作为癌症精准诊断提供了一个有前途的工具,展示巨大的临床应用潜力。
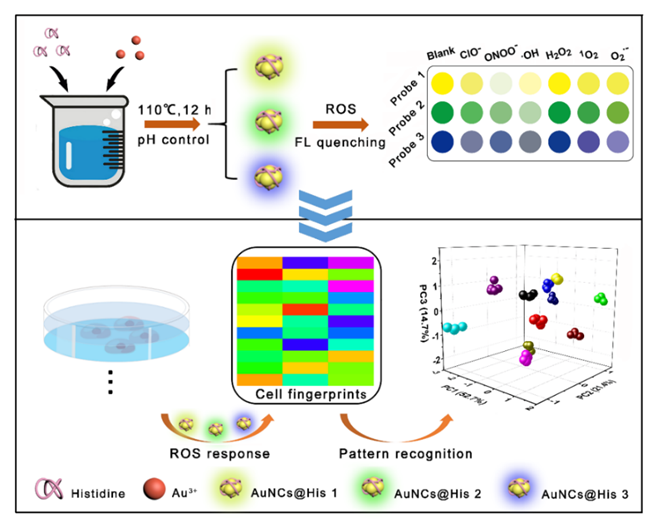
图1 基于多色AuNCs@His构建的ROS响应型荧光传感器阵列用于癌症精准诊断的原理图
【文章要点】
作者首先在pH 1.7、6.8和11.0条件下合成三种多色AuNCs@His作为荧光探针,透射电镜图和X射线光电子能谱图显示成功制备了三种单分散的AuNCs@His,荧光光谱表明AuNCs@His 1, 2和3具有显著的光学差异(图2)。
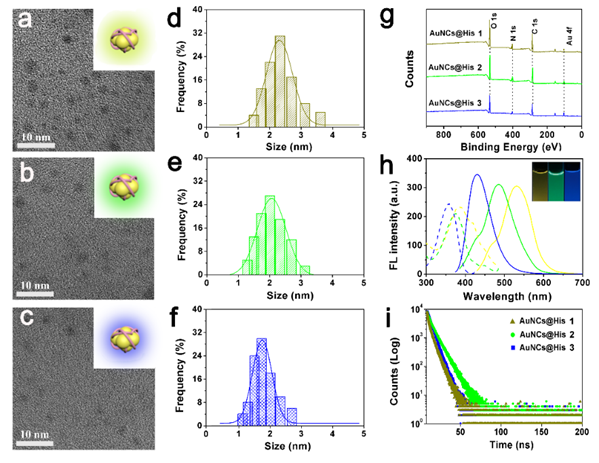
图2 AuNCs@His 1, 2和3的TEM、XPS和荧光性质表征
接下来,作者研究了三种AuNCs@His对ROS种类和水平的荧光响应,形成的荧光响应模式通过热图和PCA进一步分类。图3展示了该荧光传感器阵列对六种ROS(ClO-, ONOO-, •OH, H2O2, 1O2 和 O2•-)和不同水平ClO-的有效鉴别能力。随后,采用XPS和FTIR探究了ROS响应的荧光传感器阵列的作用机制,结果表明,金核和组氨酸配体的氧化导致了AuNCs@His的荧光猝灭(图4)。

图3 荧光传感器阵列对不同种类ROS的模式识别
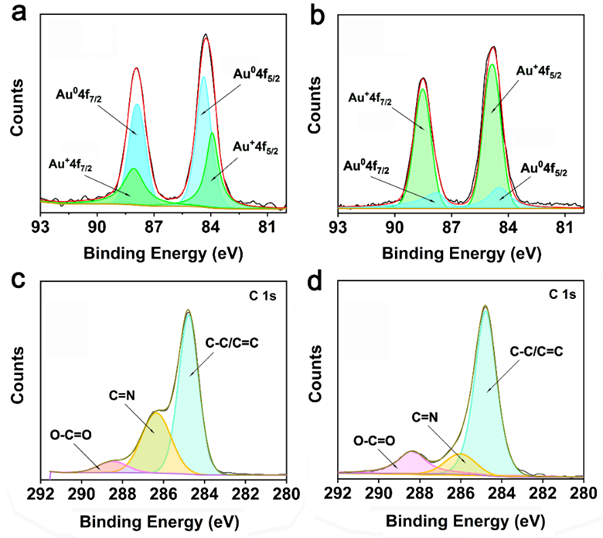
图4 AuNCs@His响应ROS的传感机制
作者考察了三种AuNCs@His的细胞摄取效率,流式细胞分析结果显示,由于表面配体相同,制备的AuNCs@His 1, 2和3呈现相似的细胞摄取效率。此外,三种AuNCs@His的表面均带正电荷,且内化的AuNCs@His能够响应细胞内ROS,引起不同程度的荧光猝灭(图5)。最后,ROS响应型荧光传感器阵列被成功应用于区分肿瘤细胞类型,准确率达到100 %。此外,该传感器阵列在区分十二个临床乳腺癌样本的肿瘤细胞增殖状态方面也表现出优异的性能,这与Ki-67免疫组化检测结果保持一致(图6)。
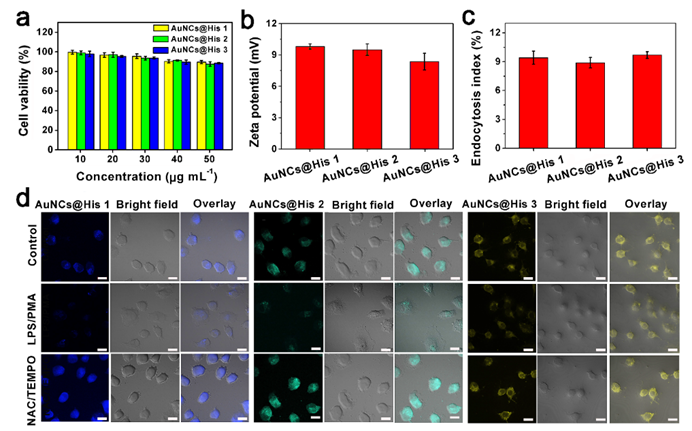
图5 AuNCs@His 1, 2和3的细胞摄取和ROS成像
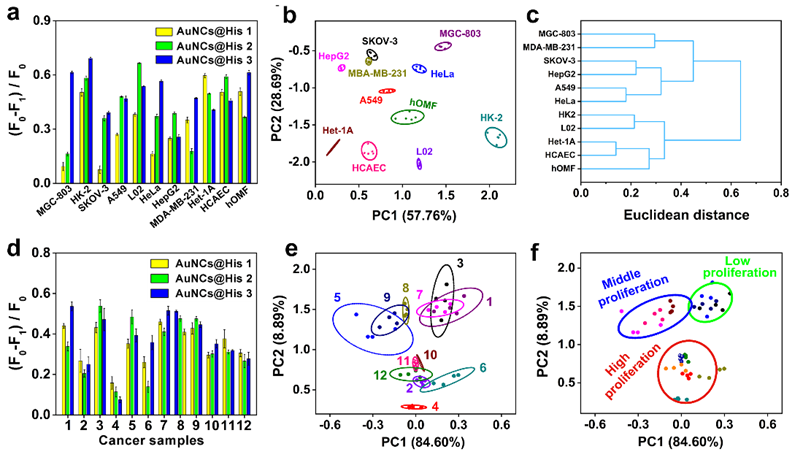
图6 ROS响应型荧光传感器阵列对肿瘤细胞类型和增殖状态的模式识别
该文章的第一作者为安徽医科大学药学院的卢海峰博士,硕士生卢麒和孙洪武为共同第一作者,张群林教授为文章的通讯作者,冉翔博士为文章的共同通讯作者。上述研究工作得到安徽医科大学科研水平提升项目、国家自然科学基金项目、和安徽省教育厅重点研究项目等资助。
原文链接:
https://doi.org/10.1021/acsami.3c09320


