Cell Metabolism:为人类治疗带来希望!刘恩岐/陈育庆/张继锋/郑乐民合作开发了非酒精性脂肪性肝炎的潜在新药物
时间:2023-04-13 17:10:57 热度:37.1℃ 作者:网络
非酒精性脂肪性肝炎(NASH)的患病率正在上升,但尚未有任何药物得以批准用来治疗。NASH药物开发的一个主要障碍是临床前研究难以转化为安全/有效的临床结果,最近的失败凸显了确定新的靶向途径的必要性。甘氨酸代谢失调已成为NASH的病因和治疗靶点。
2023年4月10日,西安交通大学刘恩岐、密西根大学陈育庆、张继锋及北京大学郑乐民共同通讯(西安交通大学为论文第一作者和通讯作者单位)在Cell Metabolism(IF=31)在线发表了题为“DT-109 ameliorates nonalcoholic steatohepatitis in nonhuman primates”的研究论文,该研究报道了三肽DT-109 (Gly-Gly-Leu)剂量依赖性地减弱小鼠脂肪性肝炎和纤维化。为了提高临床前研究转化成功率,该研究开发了一个非人灵长类动物模型,在组织学和转录上能模仿人类NASH。
应用转录组学、蛋白质组学、代谢组学和宏基因组学相结合的多组学方法,该研究发现DT-109不仅通过刺激脂肪酸降解和谷胱甘肽形成(如在小鼠中发现的那样),还通过调节微生物胆胆酸代谢,逆转肝脏脂肪变性并防止非人类灵长类动物的纤维化进展。该研究结果描述了一个高度转化性临床前的NASH模型,并强调了对DT-109进行临床评估的必要性。

世界范围内,非酒精性脂肪性肝病(NAFLD)及其更严重的形式非酒精性脂肪性肝炎(NASH)的患病率正在以惊人的速度增长。最近估计NAFLD的总体患病率为32.4%,而NASH在普通人群中的患病率估计为1.5%-6.5%。NAFLD和NASH已成为全球慢性肝病的主要原因,并与心血管、癌症和肝脏相关死亡率的增加有关。除了临床影响外,仅在美国,NAFLD的巨大经济负担每年就超过1000亿美元。尽管NAFLD的患病率很高,对导致NASH的机制的理解也取得了重大进展,并且在药物开发方面付出了巨大的努力,但目前没有药物疗法可以治疗这种疾病。
虽然目前有许多化合物正在对NASH进行评估,但在临床试验中,许多化合物要么没有表现出改善,要么引起了安全问题。NASH药物开发的一个主要障碍是未能将临床前研究的发现转化为临床环境。在NASH潜在疗法的临床前研究中,小鼠是最常用的动物。然而,尽管已经描述了大量的NASH小鼠模型,但许多模型不能准确地模拟人类疾病,也不能应用于临床。这可能是因为小鼠模型在疾病诱因、与肝脏脂质代谢、炎症和纤维化相关的病理生理学以及该病的组织病理学和肝外特征与人体存在巨大差异。尽管昂贵,但与人类疾病更密切相关的大型动物模型对于改善向临床的转化至关重要。因此,通过使用更容易转化为人类NASH的稳健临床前模型,可以显著提高临床试验成功的概率。
虽然目前的候选药物针对的是NASH发病机制中已建立的通路,但没有任何药物疗法被批准的事实突出了确定新的可靶向通路的必要性。最近,氨基酸代谢紊乱被认为与NASH有关。特别是,该研究团队和其他研究人员最近的研究发现,甘氨酸代谢受损是NASH和相关心脏代谢疾病的致病因素和治疗靶点。使用NAFLD和NASH小鼠模型,该研究团队确定了DT-109,一种基于甘氨酸的三肽(Gly-Gly-Leu),通过诱导脂肪酸(FA)降解和通过新生谷胱甘肽(GSH)生物合成的抗氧化防御来降低脂肪性肝炎和肝纤维化。
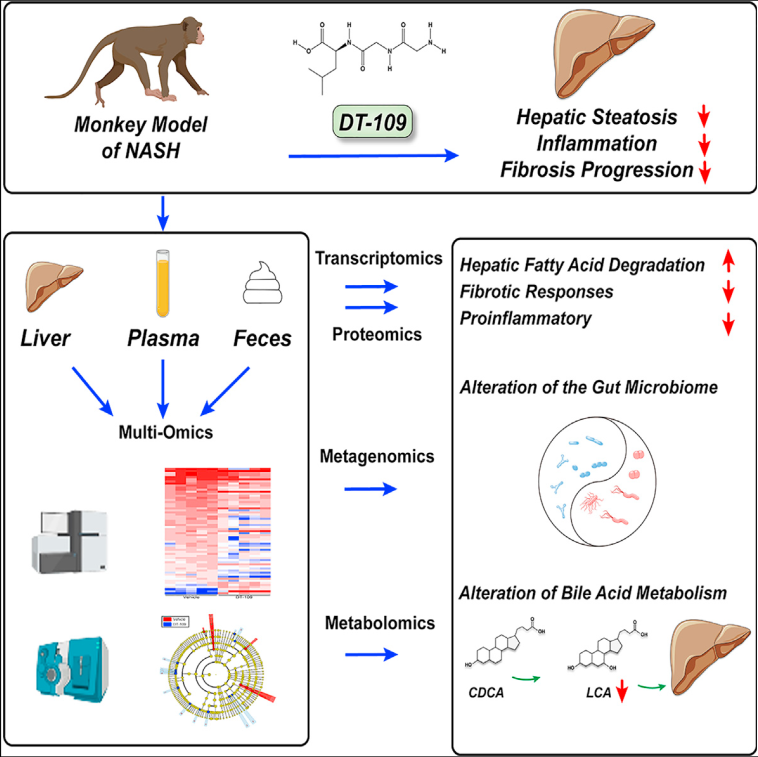
文章模式图(图源自Cell Metabolism )
为了提高DT-109在临床试验中成功的概率,该研究评估了DT-109的剂量反应,并测试了其在非人类灵长类动物(食蟹猴)中的有效性和安全性,这些灵长类动物在组织学和转录上模拟了人类疾病。该研究进一步应用了转录组学、蛋白质组学、代谢组学和宏基因组学相结合的多组学方法进行探索,结果揭示了DT-109在非人灵长类动物中逆转肝脏脂肪变性并抑制肝脏炎症和纤维化的进展,不仅是通过刺激肝脏FA降解和GSH形成,而且还通过调节微生物胆汁酸(BA)代谢。
原文链接:
https://www.cell.com/cell-metabolism/fulltext/S1550-4131(23)00091-8


