WCLC 2023:戈沙妥珠单抗+帕博利珠单抗在一线转移性NSCLC展示巨大潜力(EVOKE-02研究)
时间:2023-09-11 16:57:38 热度:37.1℃ 作者:网络
2023年WCLC大会于9月9日至12日在新加坡举行,汇聚国际肺癌领域专家、学者和医疗专业人士,共同探讨肺癌领域的最新进展、研究成果和临床实践。通过丰富的专题报告、研讨会、海报展示和互动讨论,为与会者提供了一个全面了解肺癌领域最新动态和未来趋势的机会。
EVOKE-02研究是一项全球、开放性、多队列Ⅱ期研究,评估戈沙妥珠单抗+帕博利珠单抗±铂类在无可靶向基因改变的转移性NSCLC初治患者的疗效和安全性。本次WCLC会上将会报告队列A和队列B接受SG+帕博利珠单抗治疗的初步结果。
EVOKE-02研究选择既往未经治疗的转移性NSCLC、无可靶向基因改变、ECOG PS为0或1分的患者,可纳入队列A[PD-L1肿瘤比例评分(TPS)≥50%]或队列B(PD-L1 TPS<50%)。给予两组患者SG(10 mg/kg,d1、d8)+帕博利珠单抗(200 mg,d1)、21天为1周期方案治疗。主要研究终点包括ORR、安全性导入阶段的剂量限制性毒性(DLT),次要研究终点包括DCR、缓解持续时间(DoR)、无进展生存期(PFS)、总生存期(OS)和安全性。
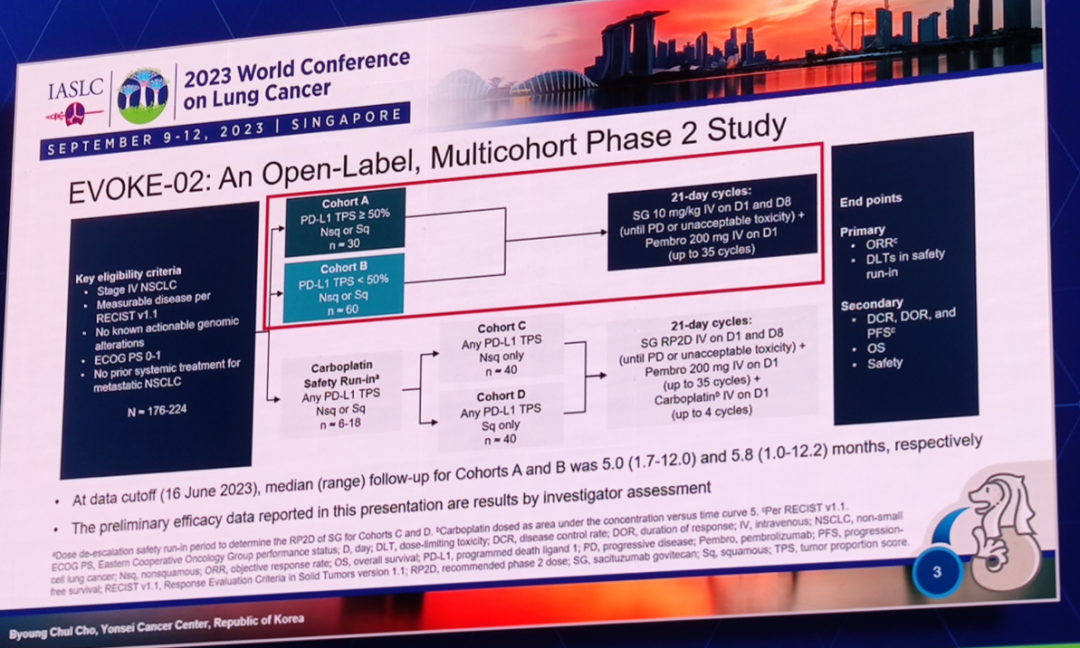
图5. EVOKE-02研究设计
总人群的ORR为56%,其中队列A为69%,队列B为44%;总人群的DCR为82%,其中队列A和队列B分别为86%和78%;总人群以及队列A和队列B的中位DOR均未达到,6个月的DOR率分别为87%、88%、88%。
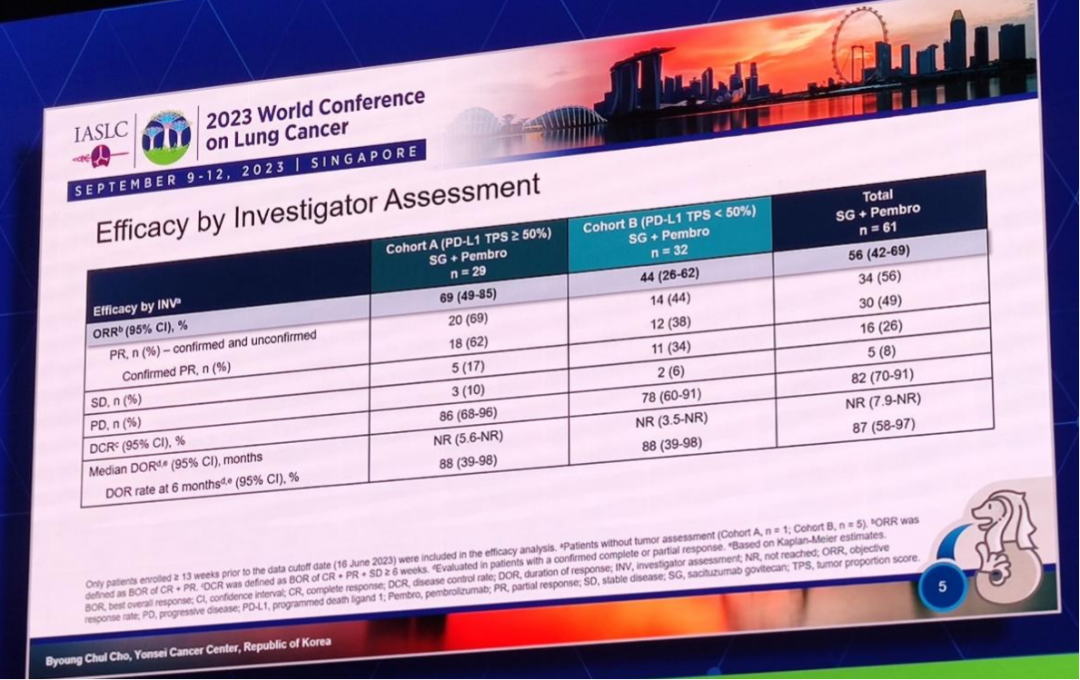
图6. EVOKE-02研究中研究者评估的疗效结果
在63例安全性可评估患者中,与治疗相关的任何级别TEAE发生率为90%,其中与治疗相关的≥3级TEAEs发生率为38%,严重TEAEs为14%。与治疗中止相关TEAEs的发生率为18%;与SG剂量降低相关的TEAEs发生率为18%。研究中观察到1例与治疗相关的死亡事件。最常见的任何级别TEAEs为腹泻(54%)、贫血(48%)和乏力(38%);免疫相关TEAEs与既往帕博利珠单抗已报道的安全性特征相似。
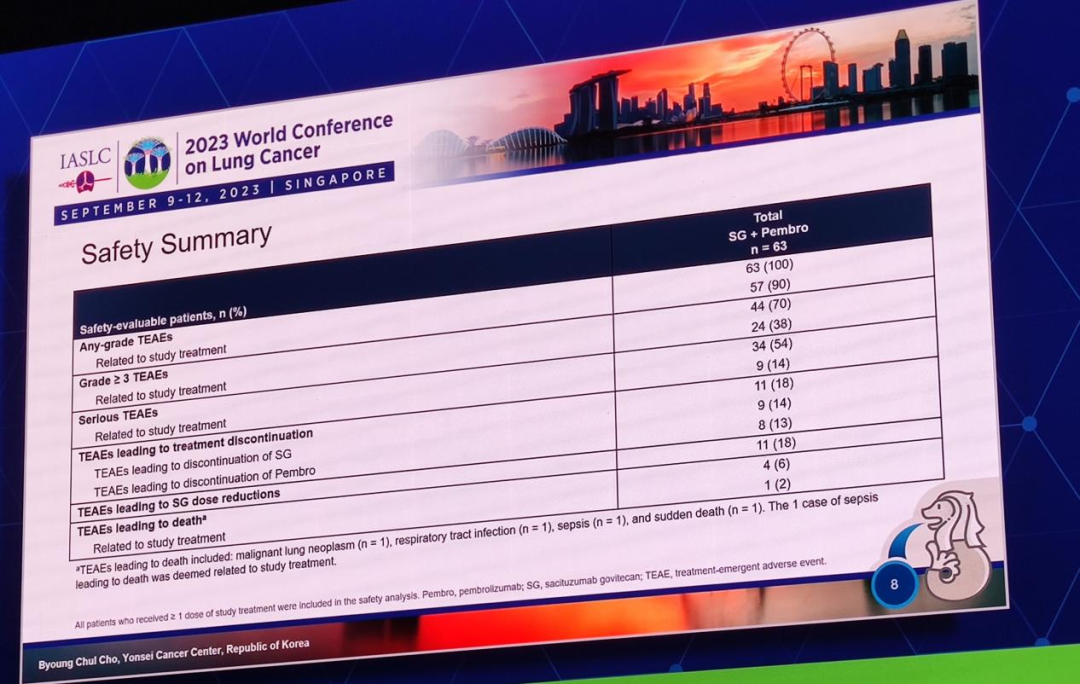
图7. EVOKE-02研究的安全性总结
总之,SG联合帕博利珠单抗在未经治疗的转移性NSCLC患者中表现出一定疗效和安全性,与单个药物的已知特征一致。
参考文献:
Heist RS, Guarino MJ, Masters G, et al. Therapy of Advanced Non-Small-Cell Lung Cancer With an SN-38-Anti-Trop-2 Drug Conjugate, Sacituzumab Govitecan. J Clin Oncol. 2017 Aug 20;35(24):2790-2797.


