系统性接触性皮炎的临床研究进展
时间:2023-09-13 11:02:05 热度:37.1℃ 作者:网络
系统性接触性皮炎(systemic contact dermatitis,SCD)是接触过致敏物的个体,再次通过口服、静脉注射、透皮吸收、吸入等方式接触同一变应原或具有交叉反应性的变应原(通常为半抗原)后发生的变应性炎症性皮肤病。
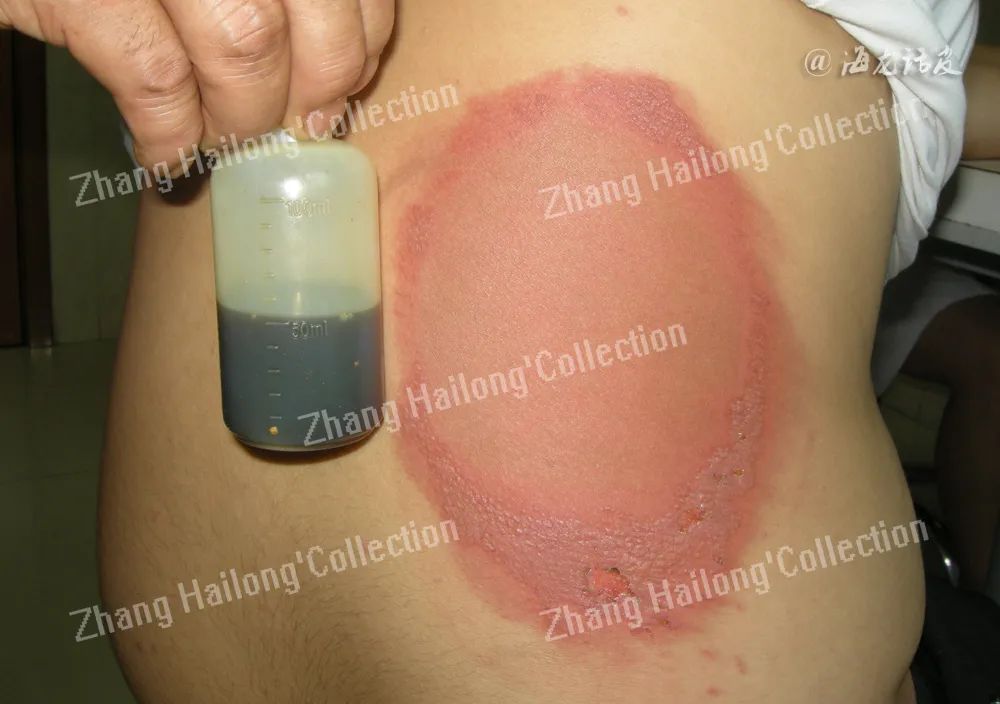
本病的诱因、发病机制和临床表现均存在相当大的异质性,特别是在致敏物质的多样性方面,临床医生目前对本病普遍认识不足,存在一定程度的误诊和漏诊。
临床表现
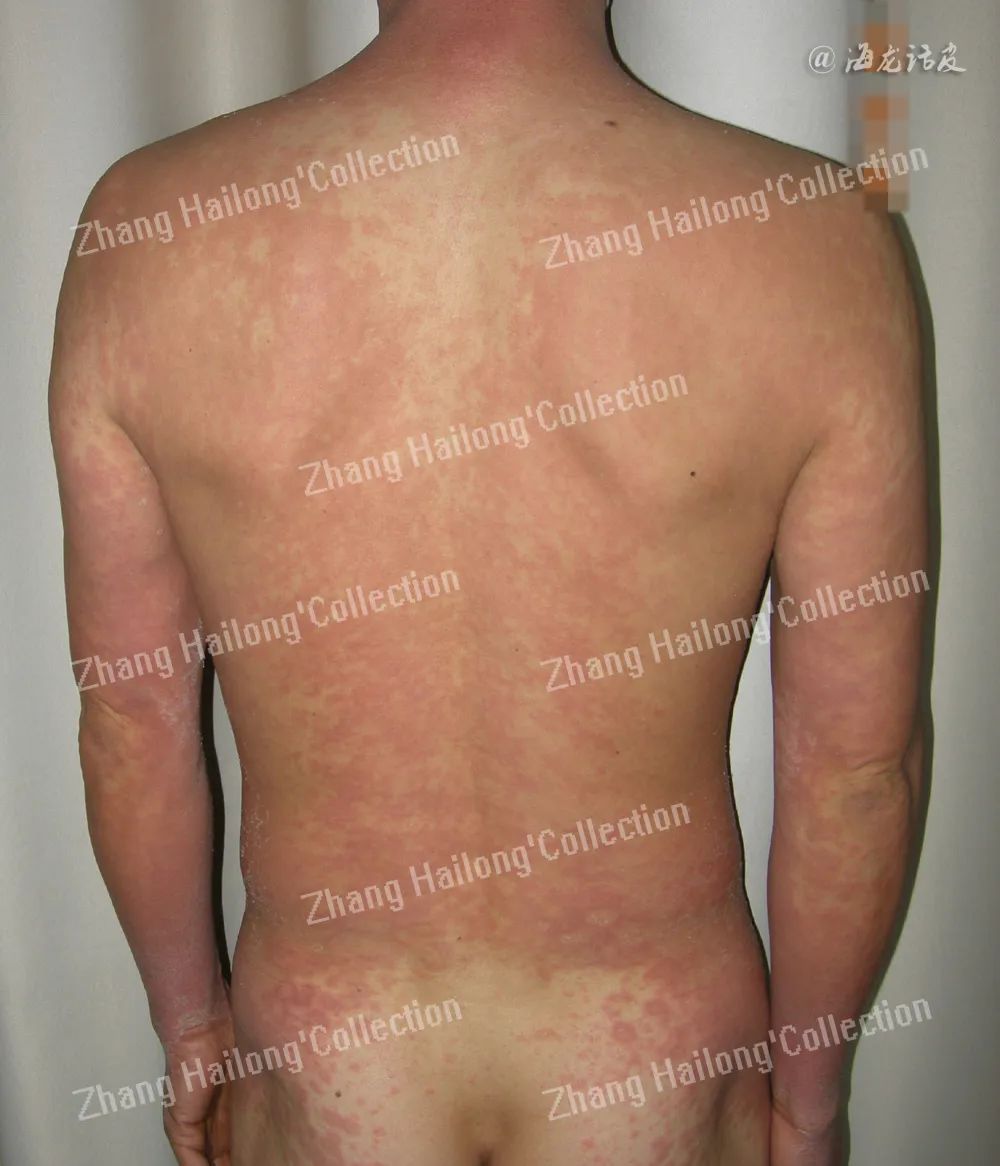
SCD除了表现为经典的湿疹样皮疹,还可表现为包括汗疱疹、既往斑贴试验部位加重、泛发性斑丘-水疱疹、狒狒综合征(baboon syndrome)、唇炎、口周湿疹、口腔炎、血管炎、紫癜样皮损、多形红斑、荨麻疹等多种皮疹。部分患者还可出现低热、乏力、头痛、关节疼痛、呕吐、腹泻等一过性的全身症状,因此又称为SCD综合征。
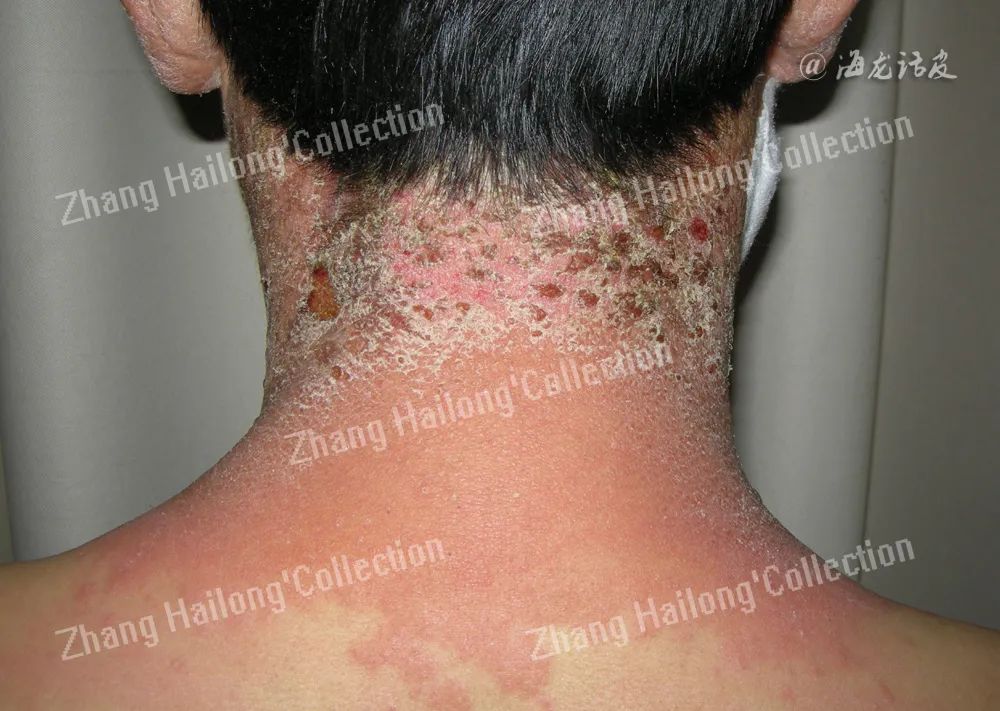
狒狒综合征是一种具有特殊表现的SCD,典型表现为臀部、大腿内侧、腹股沟区及阴囊的紫红色至鲜红色斑片,很少累及手掌、足底和面部。近期研究认为,狒狒综合征可累及更加广泛的范围,包括眼睑甚至全身,皮损也可呈脓疱样,表现为急性泛发性发疹性脓疱病。患者可无既往过敏史,斑贴试验也可阴性。
狒狒综合征可分为4型:Ⅰ型为汞、镍、秘鲁香脂、毒性青藤等过敏相关的红斑;Ⅱ型为外用药物介导的红斑;Ⅲ型为系统药物介导的红斑;Ⅳ型为非过敏接触导致的如感染诱导性狒狒综合征样皮损。其中Ⅲ型归属于药疹的一种特殊类型,即对称性药物相关性褶皱和屈侧红斑(symmetrical drug⁃related intertriginous and flexural exanthema),其最新的诊断标准为:①暴露于系统用药;②臀部和/或腹股沟区界限明显的红斑和/或V型红斑;③除臀部、腹股沟区以外至少1个其他褶皱或屈侧部位受累;④皮损具有对称性;⑤无全身症状和体征。
致敏物质
药物是SCD常见的致敏原之一。局部用药包括氨苄西林、新霉素、糖皮质激素、非甾体抗炎药(丁苯羟酸、双氯芬酸)、乙酰水杨酸、麻醉剂(辛可卡因)和乙二胺等,口服或静脉注射药物包括红霉素、新霉素、糖皮质激素、非甾体抗炎药、尼司他汀和乙二胺等。需要指出的是,药物和非药物诱发的SCD临床表现相似,明确由药物引起者建议诊断为药疹,部分患者的皮疹虽然可能是由隐藏在食物或其他物品中的药物成分引起,但临床上不能完全明确与药物的直接关系,这种情况下可诊断为SCD。
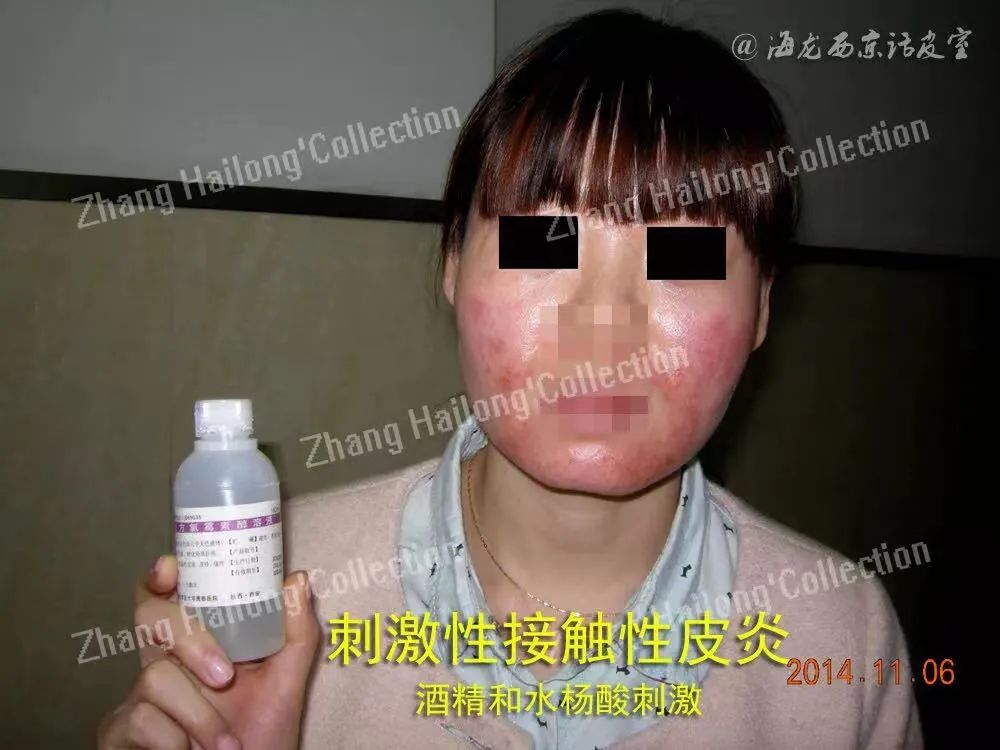
除药物外,可诱发SCD的物质还包括金属、医用体内植入物、空气中的植物花粉、种子以及化学物质等。镍是最常见的金属过敏原之一,可存在于生活常见的硬币、器皿、镀镍物品中,茶叶、坚果、海产品、罐头、豆类等也是含镍量高的食物。通常摄入的镍达到0.5~5.6mg/d时才可引起SCD的皮肤反应,极少数患者可能会由正常饮食中微量的镍(0.22~0.35mg/d)诱发。
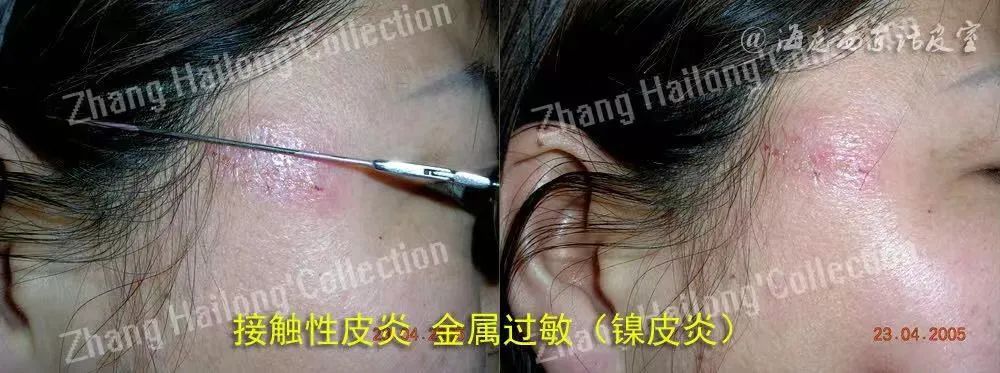
汞是另一种较常见的金属过敏原,部分化妆品和海鲜中含量较丰富。金、锌、铬和钴引起SCD相对少见。医用体内植入物如牙齿矫正及填充材料、假牙、人工关节、钢板钢针、心脏支架、人工瓣膜、人工血管、各种插管所含的金属,都可能使人体发生SCD。牙齿矫正及填充材料、假牙主要由镍、金、钴、汞、钯及甲基丙烯酸羟乙酯等组成, 常常引起唇炎、口周皮炎及扁平苔藓等局部皮疹,但也可以引起 SCD。宫内节育器主要含有硫酸铜和镍钛合金,后者引起的SCD发生率也较高。
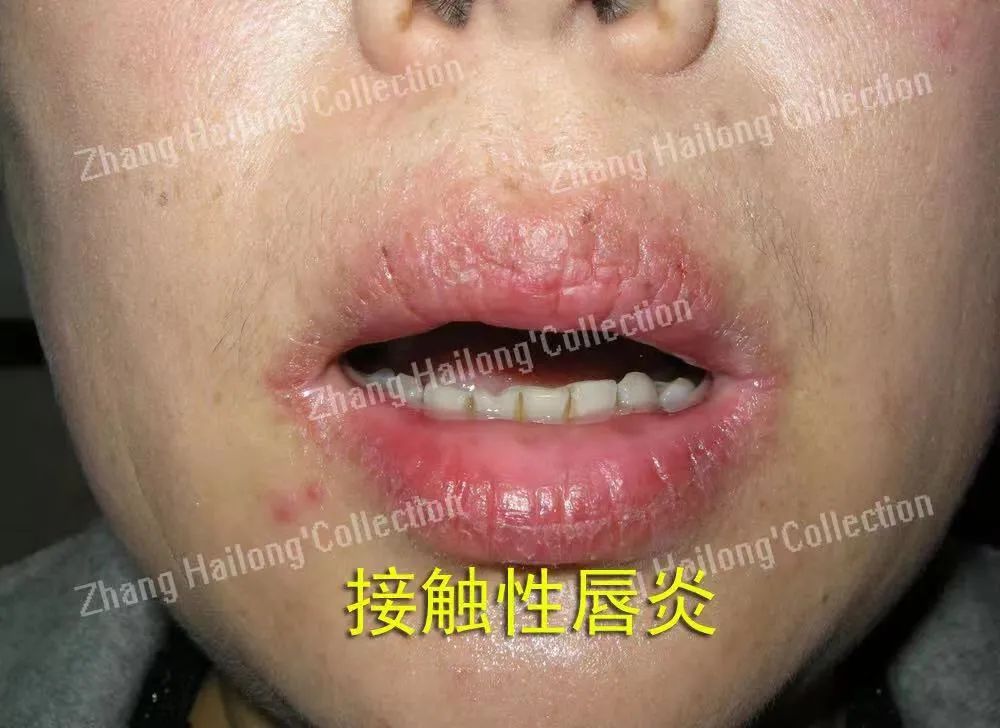
气传性接触性皮炎是由空气中的变应原(气传变应原)引起。皮疹最初一般发生于直接接触气传变应原的暴露部位(如面颈部),后期反复发作,变应原经呼吸道系统吸入后也可出现泛发性湿疹样皮疹,此时可归属于吸入变应原引起的SCD。气传变应原中,植物性的占绝大多数,常见的为菊科植物(包括豚草、黄花和向日葵)的花粉和种子,其次为空气中的化学物质(如甲醛、工业废气中的环氧树脂)及特殊物质(如饲料中的添加物)等。
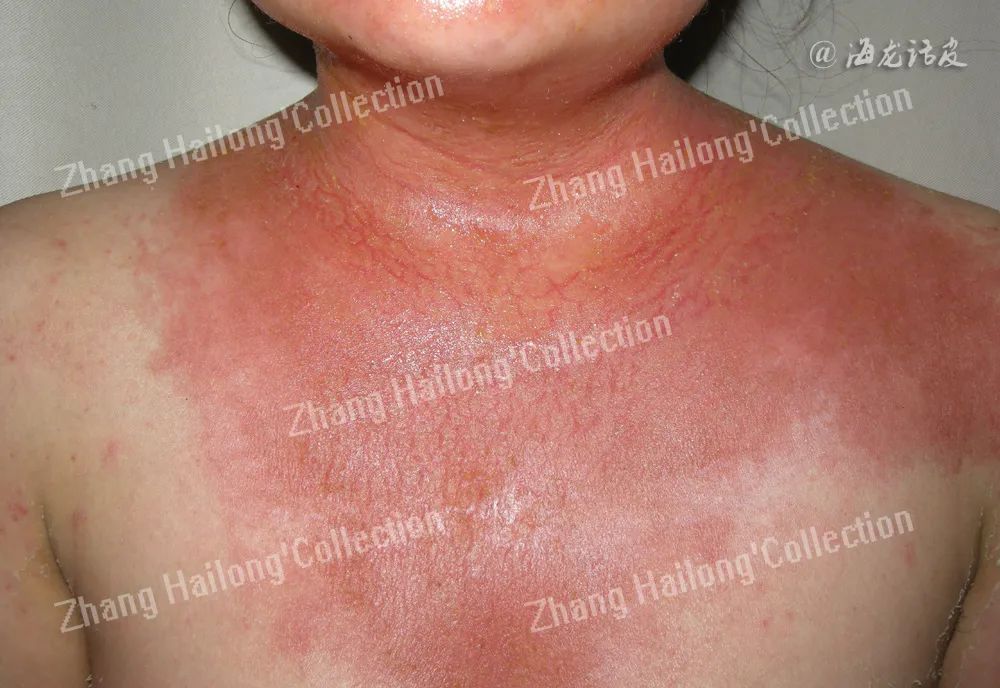
发病机制
目前普遍认为主要是Ⅳ型超敏反应参与SCD的发病机制。抗原提呈细胞(树突细胞)捕获半抗原后,在角质形成细胞分泌的炎症细胞因子如白细胞介素(IL)⁃1β、肿瘤坏死因子α、IL⁃6、IL⁃12和粒细胞-巨噬细胞集落刺激因子的作用下活化并迁移到淋巴结和脾脏皮质旁区,通过抗原提呈刺激原始T细胞增殖分化。再次接触变应原时,表达皮肤淋巴细胞相关抗原的T细胞迅速趋化至周围组织(如皮肤、肠道和肺)并活化诱导炎症反应。除了经典的抗原提呈细胞途径外,近年研究还发现,半抗原复合物可能通过IgE依赖和独立途径激活特异性T细胞。
除Ⅳ型超敏反应外,Ⅰ型、Ⅱ型、Ⅲ型超敏反应也参与SCD的发生,部分SCD甚至可以是皮肤超敏反应重叠的结果,重叠后反应的时间间隔通常比单纯的Ⅳ型超敏反应短,可能是其临床表现异质性的重要机制之一。
p⁃I机制是在药疹的发病机制中提出的一种概念:抗原(药物)可在未被主要组织相容性复合体分子呈递及缺乏先前致敏的情况下与T细胞受体直接结合,启动免疫反应。由于药疹和非药物诱发的SCD在发病机制上的相似性,这一机制也可以用于解释SCD临床上的一些现象,比如为什么有些患者在第一次接触某些药物时就会发生SCD。
诊断
SCD临床表现较为复杂。对于长期反复发作的多部位、多形性皮损均应考虑该病,尤其出现汗疱疹、既往斑贴试验部位加重、泛发性对称性红斑丘疹、狒狒综合征、难以解释的多形红斑或紫癜样损害、对治疗抵抗的顽固性皮炎等表现时。
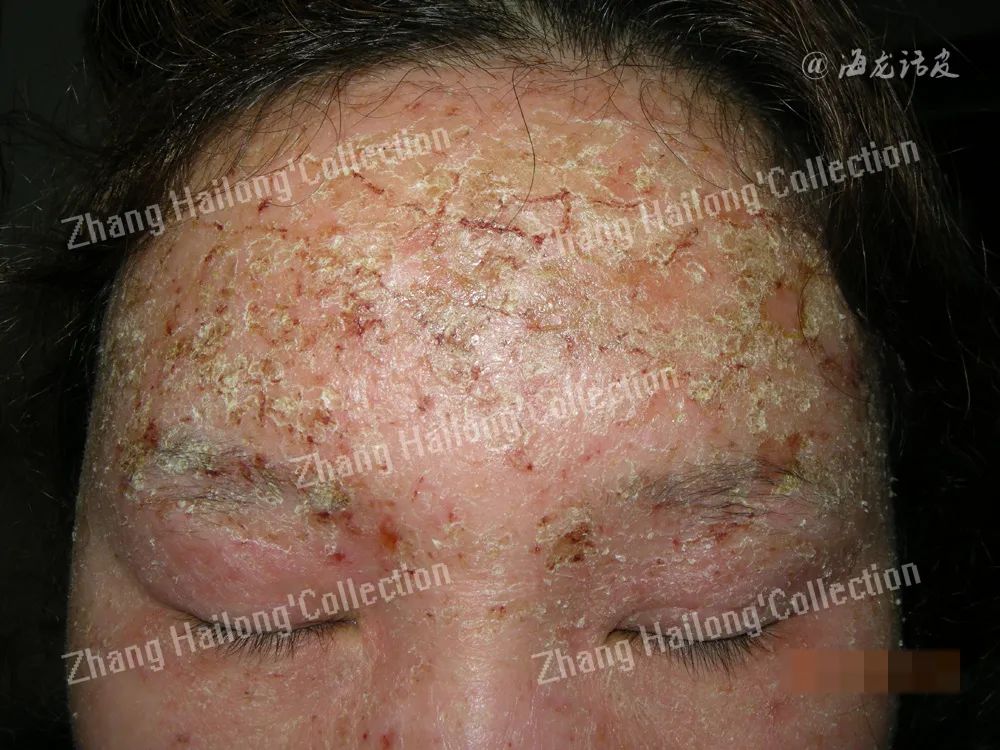
一些实验室检查对于SCD的诊断非常重要,其中斑贴试验(常规+药物+化妆品)最为常用。其他检查,包括嗜酸性粒细胞数目和比例检查、皮肤点刺试验、血液总IgE和特异性IgE检查、食物和镍口服激发试验、体外特异性细胞毒性T淋巴细胞检查等,可根据患者的病史有选择性地进行。金属诱导的淋巴细胞增殖可促进无菌性松动的人工关节等假体中破骨细胞生成,故淋巴细胞转化试验有助于对医用体内植入物中金属过敏的诊断,近年来越来越多地应用于临床。
治疗
绝大多数SCD是一个良性过程,停止接触致敏物质后, 皮疹往往在数周后逐渐消退。轻中度患者可给予口服抗组胺药和局部用糖皮质激素,较严重的需要短期系统糖皮质激素治疗。由于SCD病因常不清、病程相对迁延,症状控制后外用和/或系统用药不宜骤停,以防病情反跳。
寻找并避免相关的变应原是本病治愈的根本所在。单纯依赖检查来发现可疑变应原并指导临床可能会出现误差,从详细病史中探究患者皮炎发生、发展及加重的可能因素更为重要。由于医用体内植入物通常花费较大,且对患者身体有一定创伤,建议在放置之前详细询问患者金属过敏史,必要时完善斑贴试验和淋巴细胞转化试验等检查进行综合评估。对明确过敏者可使用非致敏合金替代植入物,并在其表面涂抹聚四氟乙烯以降低SCD的发生率。
对于部分明确诱因的患者,通过饮食治疗减少某些抗原摄入可能会取得一定的临床疗效,但这种方法也有其局限性。如由于镍在食物中的含量可能差别很大,要精确测量每日摄入量极其困难;此外,过于严格地限制含镍饮食可能会导致营养不良,尤其是膳食纤维的缺乏。二硫化氢或四乙基硫脲螯合疗法可作为治疗镍过敏所致SCD的选择,但应注意其肝毒性、周围神经病变和视神经炎等不良反应。
也有学者通过临床试验证实,配合低镍饮食联合脱敏疗法对镍过敏所致SCD有明确效果,联合脱敏疗法可避免单纯应用低镍饮食的不足,其中IL⁃2可能成为判断脱敏治疗是否成功的合理指标。近期国外临床观察研究表明,dupilumab单抗对部分难治性SCD 疗效满意,尤其对于Th2介导、变应原无法完全避免或对免疫抑制剂不能耐受的患者。这些研究为SCD的治疗带来了新理念,但由于目前尚缺乏大样本量研究,其价值有待进一步评估。
小结
认识SCD临床表现的多样性和病因机制的复杂性,了解致敏原的相关交叉知识并建立规范清晰的诊断思路是减少描述性诊断及误诊、漏诊的重要前提。在详尽的病史资料基础上科学进行变应原筛选分析,是制定规避变应原和长期防治方案的根本所在。
参考文献:
邓思思,宋志强.系统性接触性皮炎的临床研究进展[J].中华皮肤科杂志,2021,3(54):270-272.


