Precis Clin Med:NDRG1 通过靶向 TAF15 促进内皮功能障碍和缺氧诱导的肺动脉高压
时间:2023-10-31 14:30:47 热度:37.1℃ 作者:网络
研究背景:
肺动脉高压(PH)代表着一种威胁性的病理生理状态,可以由慢性低氧引起,并以广泛的血管重塑为特征。然而,低氧引起的血管重塑机制尚未完全阐明。为了研究缺氧期间内皮细胞功能障碍的分子机制,我们比较了正常氧和低氧条件下的肺内皮细胞,并发现当暴露在低氧条件下时,N-肉瘤细胞下游调控基因-1(NDRG1)在肺内皮细胞中明显上调。NDRG1属于NDRG家族,包括四个成员:NDRG1、NDRG2、NDRG3和NDRG4。NDRG1在细胞生长、发育、分化和应激反应中发挥多功能作用。然而,NDRG1是否与缺氧期间内皮功能障碍相关,以及是否在血管重塑中发挥作用,都尚未得到详细阐明。NDRG1在人体组织中广泛表达,但在正常ECs中几乎难以检测,这表明缺氧可能会特异性地上调这些细胞中的NDRG1,然后促进缺氧引起的PH。在本研究中,我们证明了在缺氧刺激的内皮细胞中,NDRG1的表达在时间依赖性和人体和大鼠内皮病变中明显增加。我们揭示了NDRG1在体内和体外内皮功能障碍和血管重塑中的潜在功能,然后探讨了其潜在机制。我们的结果揭示了NDRG1在HPH发病机制中的关键作用。

研究方法和结果:
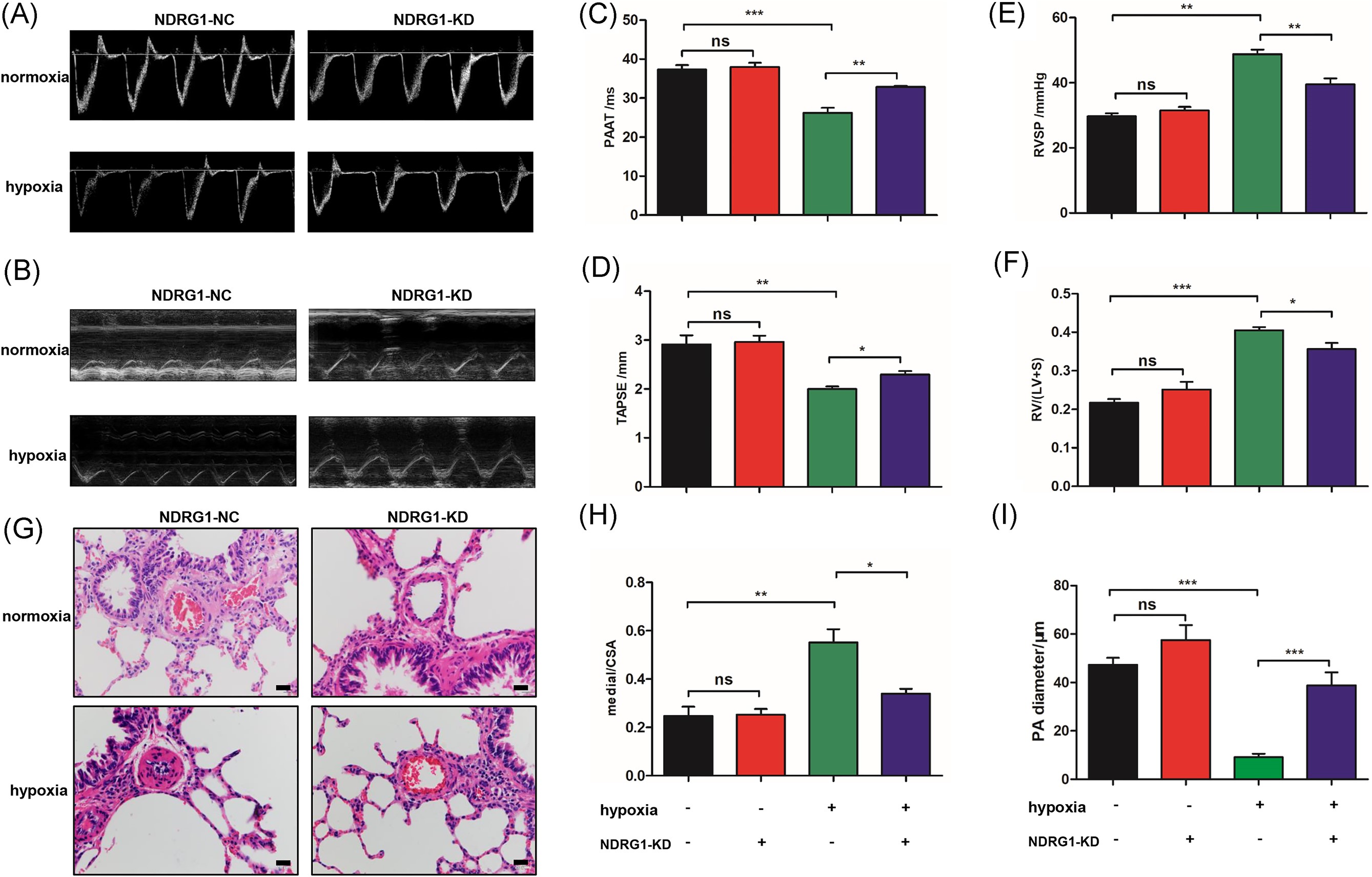
通过使用定量聚合酶链反应、免疫印迹和免疫组织化学,我们证明了N-肉瘤细胞下游调控基因-1(NDRG1)在低氧刺激的内皮细胞中呈明显时间依赖性增加,同时在人和大鼠的内皮病变中也有增加。为了确定NDRG1在内皮功能障碍中的作用,我们进行了使用NDRG1短发夹RNA和NDRG1过表达质粒的功能缺失研究。体外实验中,沉默NDRG1减轻了低氧条件下人肺动脉内皮细胞(HPAECs)的增殖、迁移和管形成,而NDRG1过表达则促进了HPAECs的这些行为。在机制上,NDRG1可以直接与TATA-盒结合蛋白相关因子15(TAF15)相互作用,并促进其核定位。TAF15的敲除消除了NDRG1对HPAECs的增殖、迁移和管形成能力的影响。生物信息学研究发现,TAF15参与调控已被证明与PH相关的PI3K-Akt、p53和缺氧诱导因子1(HIF-1)信号通路。此外,与野生型同胎仔鼠相比,NDRG1敲除大鼠的低氧引起的血管重塑和右心室肥厚明显减轻。
研究结论:
综合考虑,我们的结果表明,低氧引起的NDRG1上调通过靶向TAF15导致内皮功能障碍,最终促进了低氧引起的PH的发展。
原始出处:
Li C, Lv J, Wumaier G, Zhao Y, Dong L, Zeng Y, Zhu N, Zhang X, Wang J, Xia J, Li S. NDRG1 promotes endothelial dysfunction and hypoxia-induced pulmonary hypertension by targeting TAF15. Precis Clin Med. 2023 Oct 9;6(4):pbad024. doi: 10.1093/pcmedi/pbad024. PMID: 37885911; PMCID: PMC10599394.


