Cancer Research:短波红外成像助力神经母细胞瘤根治性切除
时间:2023-11-04 08:43:20 热度:37.1℃ 作者:网络
作为儿童中最常见的颅外肿瘤,神经母细胞瘤占据儿童恶性肿瘤总发病的8-10% ,造成了约15%的儿童癌症相关死亡,超过1/3的神经母细胞瘤患者在确诊时便已发生了肿瘤转移。至今为止,高危神经母细胞瘤患者的预后仍不容乐观。虽然无显微残留的根治性切除术一直以来都是高危患者手术治疗的金标准,但由于神经母细胞瘤具有浸润腹腔、胸腔,侵袭神经、血管以及周围器官等生长特性,做到根治性切除对于外科医生而言仍然是很大的挑战。
荧光导航技术为解决这一问题提供了新的思路。荧光染料的应用可以使难以捉摸的恶性肿瘤组织在术中实时显影,大大有助于阳性切缘的辨认,在完成根治性切除的同时最大程度保护周围的正常结构。虽然这一技术相关的研发和临床试验已在成人患者中取得了较大的进展,但尚未应用至儿童肿瘤领域。
近日,由英国大奥蒙德街儿童医院 Stefano Giuliani 团队发表于 Cancer Research 题为 Shortwave Infrared Imaging Enables High-Contrast Fluorescence-Guided Surgery in Neuroblastoma 的文章,通过使用自行设计的红外荧光成像系统,比较了分别交联了两种染料的GD2抗体、以及近红外与短波红外成像分辨肿瘤组织的能力,为短波红外成像应用于儿童神经母细胞瘤根治性切除提供了重要依据。

研究团队首先在体外实验中证实了分别交联了IR800、IR12两种荧光染料的GD2抗体与GD2阳性细胞的特异性结合能力。通过模拟皮下组织的特殊材料、观察荧光显像应用于皮下组织的情况显示,研究者发现使用波长较长的红外成像灵敏度更高,提示了短波红外成像(短波红外相较于广泛应用于活体成像的近红外波长更长)应用于皮下肿瘤组织成像的潜力。
随后,研究团队在小鼠体内进一步证实了短波红外成像应用于皮下肿瘤组织成像的能力,并比较了两种荧光染料的显像能力差别。在小鼠体内进行的临床前试验的整体安排如下图所示,将LAN-1细胞移植至小鼠皮下、构建移植瘤模型后,根据肿瘤的大小静脉注射交联了荧光染料的GD2抗体,并在不同时间点进行成像观察及相关指标检测。
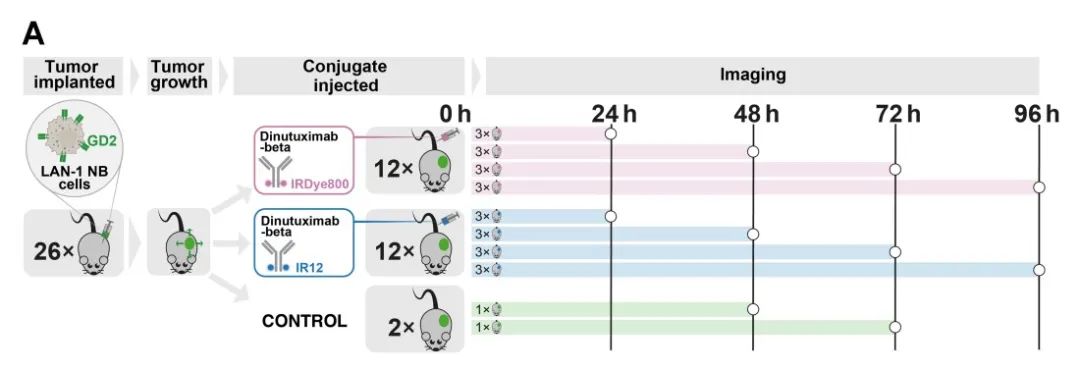
在移植瘤小鼠中进行的体内实验整体安排
主要试验结果如下图所示。交联了荧光染料的GD2抗体使得小鼠体内的肿瘤在不同时间段中均可以使用常规的近红外成像系统得到显影,IR800染料的显影能力相较于IR12要略强一些。在使用近红外成像系统导航下手术切除IR800染料示踪的肿瘤组织时,研究者发现,荧光信号不仅使大体上肉眼难以分辨的肿瘤阳性切缘更加明显,甚至可以使肉眼完成肿瘤切除后、剩余的肿瘤残留组织得以辨认。

使用2种染料交联抗体及近红外成像得到主要的实验结果,包括实时荧光显像照片、不同时间点两种染料的显像参数、对应肿瘤组织的病理染色照片(MFI:mean fluorescence intensity,平均荧光强度;TBR:tumor-to-background ratio,肿瘤与背景对比度)
在注射了荧光染料后持续性观察的96小时中,没有小鼠出现明显的毒性反应。虽然荧光的亮度随着时间推移、染料交联抗体的代谢在逐渐减弱,但在持续性观察的过程中一直可以在背景组织中清晰地显示出肿瘤的存在。
最后,研究团队探究了短波红外的成像能力是否的确优于近红外成像。在注射了交联不同染料抗体的移植瘤小鼠中,分别使用两种红外线对肿瘤及周围组织进行成像的结果显示:短波红外成像得到的荧光强度等具体参数,与近红外成像得到的高度一致。此外,短波红外成像的肿瘤与背景对比度(tumor-to-background ratio, TBR)以及边界的清晰度均优于近红外成像。
总之,这项前临床实验表明,通过将荧光染料与肿瘤特异性抗体交联,可以通过近红外/短波红外成像系统使得肿瘤组织边界在相对充足的时间内清晰可辨,且暂未见相关副作用。此外,这项研究也为理论上优于传统广泛使用的近红外系统、但未得到充分试验的短波红外成像系统的推广提供了重要依据。
通过将交联了荧光染料的肿瘤特异性抗体与短波红外成像系统相结合,使得肉眼难以辨认的肿瘤组织得以分辨,从而助力于高危神经母细胞瘤的根治性切除术,相关的临床实验及转化拭目以待。
DOI: 10.1158/0008-5472.CAN-22-2918


