儿童特应性皮炎的皮肤微生态环境
时间:2023-11-28 18:29:39 热度:37.1℃ 作者:网络
特应性皮炎(atopic dermatitis,AD)是儿童最常见的慢性、复发性、炎症性、瘙痒性皮肤病,其发病率在逐年上升,据报道该病影响了全球10%~20%的儿童和1%~3%的成人。近30年来全世界发病率均逐渐上升,在我国1~7岁儿童的患病率由2002年的2.78%上升到2014年的12.94%。因皮损反复发作和剧烈瘙痒,严重影响患儿及整个家庭的生命质量。
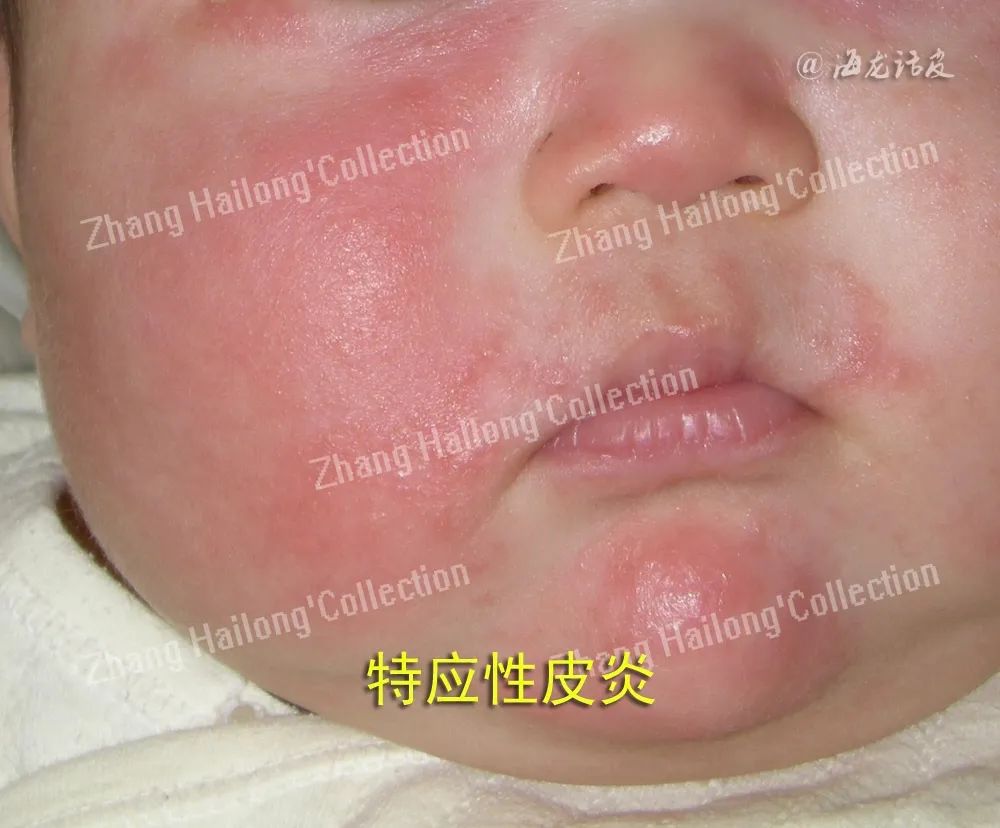
皮肤微生态环境失调已被普遍认为是AD发病的重要因素,如何实现并维持皮肤微生态环境与宿主之间的平衡已成为AD治疗领域的研究热点。
一 皮肤微生态环境简介
皮肤是人体最大的器官,维持着人体的完整性和功能稳态,是抵御病原体、紫外线和理化物质的第一道防线。其中表皮在屏障功能中发挥着最重要的防护作用,可限制被动失水、阻挡外界环境因素干扰以及防止微生物入侵等。在传统概念里,皮肤屏障主要指的是皮脂膜和角质层的物理屏障。而广义上的皮肤屏障的功能体现在多重方面—微生物屏障、物理屏障、化学屏障、神经屏障和免疫屏障。

微生物屏障是皮肤屏障的最外层,是皮肤屏障密不可分的一部分。皮肤表面存在着大量的微生物,由细菌、真菌、病毒及节肢动物等各种微生物与皮肤表面的组织、细胞及各种分泌物、微环境等共同组成的动态可变的生态系统,称为皮肤微生态环境或皮肤微生物组,其与表皮各种细胞、皮肤免疫系统等相互联系,构成了皮肤屏障的最外层防护,即微生物屏障。
皮肤表面的微生物包括常驻微生物和暂驻微生物,宏基因组学研究表明,皮肤表面的常驻微生物以细菌为主,其中主要包括四大类:放线菌门(丙酸杆菌和棒状杆菌)、厚壁菌门(葡萄球菌)、变形菌门和拟杆菌门,其中葡萄球菌、丙酸杆菌、棒状杆菌是最为丰富的三大菌属,而暂驻菌是引起皮肤感染的主要病原菌。
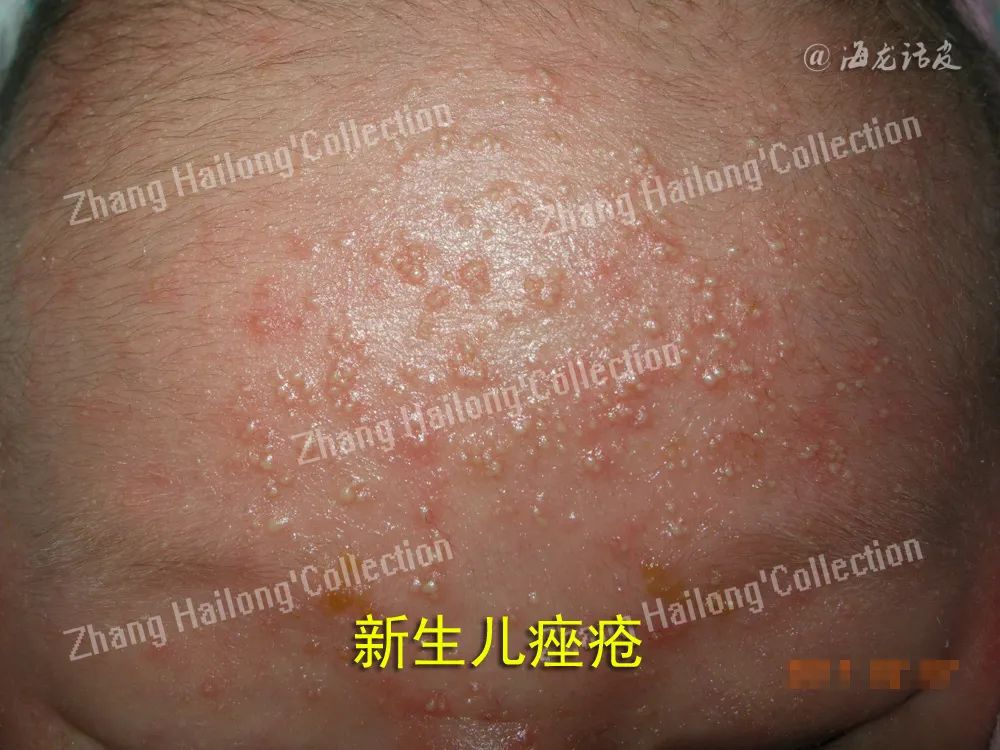
皮肤表面微生物的组成处于动态平衡的状态,即“微生态平衡”。微生态失衡会导致微生物屏障破坏,从而诱发多种皮肤病,与皮肤微生物群组成紊乱密切相关的疾病包括AD、痤疮、银屑病等。
1、儿童皮肤微生态环境:
以前,多认为子宫内部是无菌的,微生物于分娩过程中定植在人体皮肤。然而,越来越多的研究表明,子宫腔、胎盘和羊水并非无菌,定植发生在母亲体内。据推测,胎盘微生物组可能会影响胎儿的新陈代谢和免疫反应。胎盘微生物组主要由厚壁菌门、特内菌纲、变形杆菌门、拟杆菌门和梭菌门等非致病性共生微生物群组成。胎盘的微生物群丰度低,但代谢丰富。皮肤微生物群是一个动态系统,稳定性在不同年龄组之间有所不同,多样性与成熟度呈反比。新生儿皮肤的初始定植在很大程度上取决于分娩方式和新生儿在分娩过程中所接触的母亲菌属。通过生殖道出生的新生儿皮肤分离的微生物主要是乳酸杆菌、普雷沃菌和斯内菌的母系属。通过剖宫产出生的新生儿,皮肤微生物群主要是葡萄球菌、棒状杆菌和角质杆菌。剖宫产分娩婴儿皮肤微生物群多样性低于阴道分娩婴儿。分娩时的孕龄也会影响皮肤微生物群的组成。足月儿皮肤细菌多样性高于早产儿(<37周),但早产儿特定皮肤相关细菌丰度增加,包括葡萄球菌、链球菌、棒状杆菌等。随后,微生物群的富集随着哺乳期继续,皮肤环境经历动态的结构和功能变化,包括pH值、水分含量、经表皮失水和皮脂生成的变化。细菌生物量随着年龄增长而增加, 但在生后第1年内构成基本保持不变。另一项研究表明,生活在农村或城市环境中的儿童,其皮肤微生物群具有显著差异,特别是在儿童早期(1~4岁),这表明生活环境影响婴幼儿皮肤微生物群的构成。在青春期和性成熟期,激素水平刺激皮脂分泌旺盛,导致皮肤微生物群中亲脂性细菌 广泛增殖,链球菌属逐渐被丙酸杆菌属和棒状杆菌属取代。
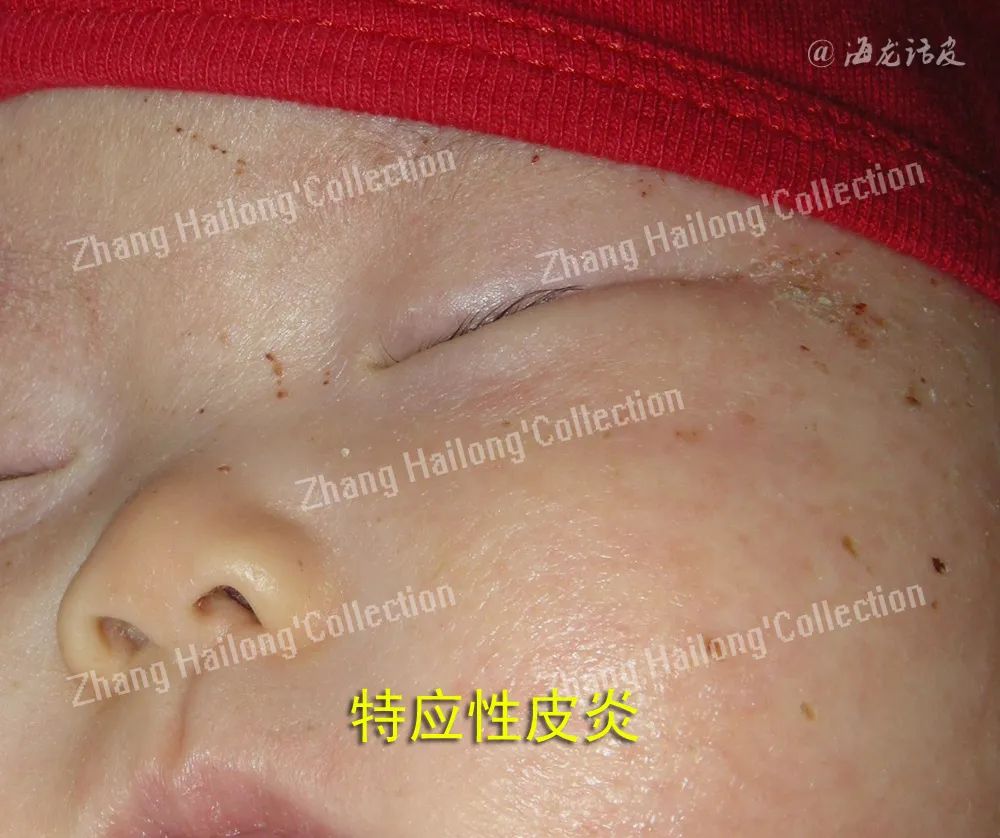
皮肤微生物群包括细菌和真菌。人类皮肤真菌微生物群主要由酵母组成,特别是马拉色菌属的物种,如球形马拉色菌、限制性马拉色菌和共生马拉色菌。这些微生物的分布与身体部位有关。如球形马拉色菌常分布在胸部和手臂,而限制性马拉色菌常分布在外耳道和耳后皱襞。曲霉菌、红酵母菌、隐球菌常存在于其他皮肤区域(如足部)。
2、皮肤微生态环境与免疫系统:
表皮葡萄球菌是一种革兰阳性细菌,占需氧常驻菌群的90%以上,被认为是一种良性微生物。表皮葡萄球菌是人类皮肤的典型共生体,通过分泌特定化学物质如酚溶性调节素促进伤口修复,增强皮肤免疫力,抑制病原体感染;与宿主相互作用有助于微生物群的稳定性和皮肤的完整性。表皮葡萄球菌细胞壁衍生的脂磷壁酸通过抑制角质细胞释放的炎性细胞因子和由受损表皮细胞产生的RNA共同来预防基于皮肤损伤的皮肤免疫反应。
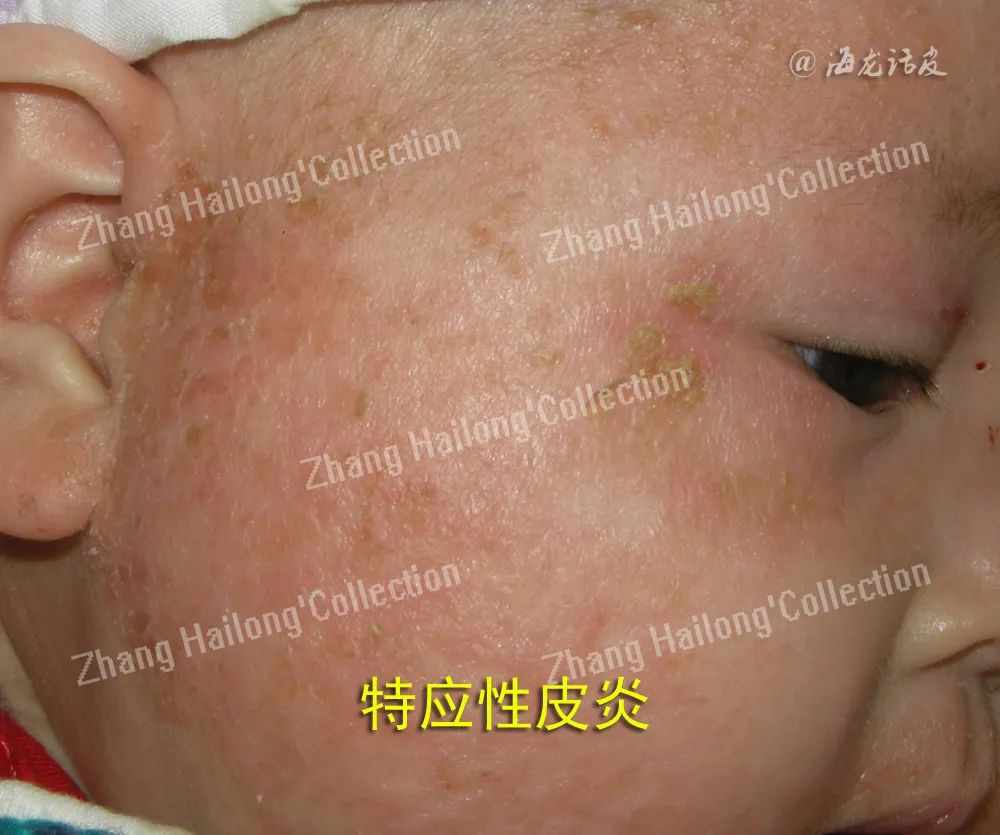
此外,表皮葡萄球菌也可以通过增强抗菌肽(如β-防御素)的基因表达来增强皮肤对感染的防御机制。痤疮丙酸杆菌是一种厌氧菌,也是人类皮肤中最常见和最重要的共生细菌之一,尤其在富含皮脂腺的皮肤区域,痤疮丙酸杆菌以高浓度存在。痤疮丙酸杆菌产生丙酸,有助于维持健康皮肤的酸性pH值,从而抑制更多病原微生物的定居。表皮葡萄球菌和痤疮丙酸杆菌等皮肤共生菌是人类皮肤免疫的重要驱动者和放大器。
二 AD与微生态环境
AD是一种由上皮屏障功能障碍、免疫调节失调、皮肤炎症共同引起的全球性、异质性、复发性、慢性、瘙痒性皮肤病。研究发现,皮肤微生物群失调中,主要病原体金黄色葡萄球菌的定植对AD的发生、发展影响尤为重要。条件致病菌金黄色葡萄球菌在稳态条件下以相对较低的定植率和几乎检测不到的丰度水平无症状定植于超过30%的个体,表明在健康人皮肤上定植的潜在致病菌会受到本地微生物群落制约。但是,定植是随后感染的一个重要风险因素,某些情况下的迅速膨胀成为机会性病原体,破坏平衡状态,导致多种皮肤病发生。
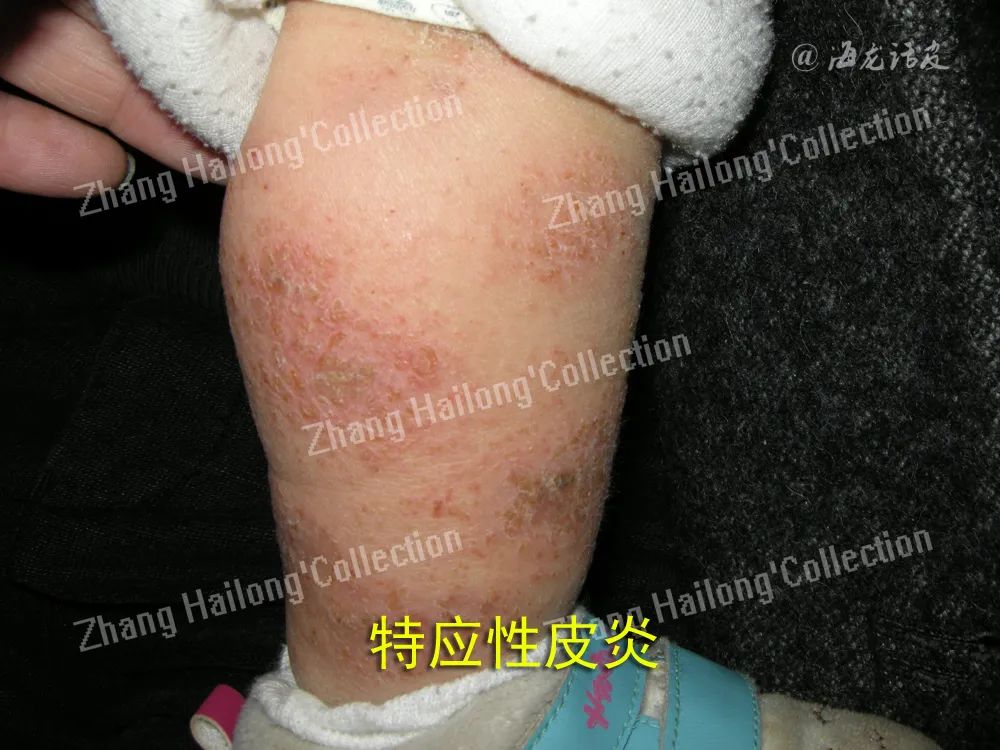
AD微生态环境的主要特征是细菌多样性的下降和葡萄球菌科相对丰度的急剧增加。在AD发作期间,未经治疗的患者中金黄色葡萄球菌和棒状杆菌的丰度显著增加,细菌多样性下降,包括丙酸杆菌、链球菌、不动杆菌和棒状杆菌减少;AD治疗后临床症状缓解,细菌多样性增加,表皮葡萄球菌、链球菌、棒状杆菌和丙酸杆菌的丰度增加。
除金黄色葡萄球菌外,皮肤中还含有其他葡萄球菌属的物种,尤其是表皮葡萄球菌。表皮葡萄球菌是凝固酶阴性葡萄球菌物种中最显著的一种,该物种主要存在于 AD病情较轻的患者中,似乎可以抑制强烈的细胞因子和趋化因子反应,表明这些细菌具有一定保护作用,而金黄色葡萄球菌则与较严重的病例相关。还有研究表明,受累皮肤内链球菌属、棒状杆菌属和丙酸杆菌属细菌数量减少,皮肤细菌种类丰度的这种变化可能是金黄色葡萄球菌和表皮葡萄球菌分泌抗菌化合物作用的结果。
AD的严重程度通常与金黄色葡萄球菌形成的生物膜有关。生物膜是附着在皮肤表面并被细胞外基质包围的细菌组合。研究表明,生物膜诱导免疫逃逸,导致AD复发和难以治疗的感染。许多研究报道了金黄色葡萄球菌、上皮屏障破坏和免疫系统之间的相互作用。AD患者皮肤抗菌肽水平降低,金黄色葡萄球菌定植增加。金黄色葡 萄球菌激活朗格汉斯细胞释放白介素(IL)-4、IL-5和IL-13,诱导Th2细胞因子过度释放,激活大量幼稚T淋巴细胞引起混乱的炎症反应。
研究显示,AD发作期间,表皮葡萄球菌和金黄色葡萄球菌定植均增加,提示表皮葡萄球菌具有代偿作用。这种皮肤共生体通过Toll样受体2信号通路促进角质形成细胞抗菌肽的表达,同时产生细胞溶酚调素γ和细胞溶酚调素δ,增强抗菌肽效应,抑制金黄色葡萄球菌的生长。表皮葡萄球菌菌株分泌高水平的细胞外丝氨酸蛋白酶(Esp),不仅防止金黄色葡萄球菌的定植,还增强了金黄色葡萄球菌生物膜对免疫系统效应机制的敏感性,进而减少金黄色葡萄球菌引起的皮肤炎症。除此之外,痤疮丙酸杆菌不仅产生卟啉分子Ⅲ诱导金黄色葡萄球菌聚集和生物膜形成,也可以通过增强金黄色葡萄球菌的细胞溶解活性,诱导促炎细胞因子的产生,从而对皮肤造成损害。
与大量关于皮肤细菌的研究相比,AD患者皮肤真菌多样性的报道很少。与健康受试者一样,马拉色菌属(尤其是球形马拉色菌和限制性马拉色菌)在AD患者中占优势。在轻中度AD患者中,限制性马拉色菌定植为主;重度AD患者中,这两 种菌的比例基本相等。马拉色菌物种被证明可以穿透AD患者的上皮屏障,引起免疫细胞的激活和皮肤炎症。而非马拉色菌真菌,如白色念珠菌、分流隐球菌和液化隐球菌在AD患者中的检出率也是高于健康受试者的。
AD是一种复杂的多因素疾病,严重影响患儿及其家庭的生活质量。在过去的几十年里,对AD及其病理生理机制的研究有了重大进展,对皮肤屏障功能障碍和免疫系统之间的相互作用也有了详细了解。在近几年,越来越多的研究分析了健康和患病个体中微生物群落与宿主的关系,证明了皮肤微生物群失调是AD发生、发展的关键因素之一。对微生物群落可能变化的研究有助于管理AD的发展、诊断和治疗,恢复微生物群的稳态,开发新的治疗方法,是今后面临的主要挑战。
参考文献:
1.管志伟,刘欣欣,李钦峰.儿童特应性皮炎的皮肤微生态环境[J].中国实用儿科杂志,2023,38(9):704-708.
2.Ahluwalia J,Borok J,Haddock ES,et al.The microbiome in preadolescent acne:Assessment and prospective analysis of the influence of benzoyl peroxide[J].Pediatr Dermatol,2019,36,(2):200-206.
3.Liu Y,Wang S,Dai W,et al.Distinct skin microbiota imbalance and responses to clinical treatment in children with atopic dermatitis[J].Front Cell Infect Microbiol,2020,10:336.
4.其他参考文献略。


