BMC Oral Health:IRE1α介导的脂肪细胞内质网应激诱导的实验性牙周炎低脂联素血症
时间:2024-01-12 21:10:10 热度:37.1℃ 作者:网络
脂联素是一种30kda的蛋白,主要由内脏脂肪细胞产生,分泌到外周血中。循环脂联素浓度可达2 - 20µg/mL,占血清总蛋白的0.01-0.05%。循环脂联素可以到达许多组织,如心脏、肝脏、肾脏、胰腺和骨骼肌。它与靶细胞表面的脂联素受体结合,具有积极的抗炎、抗动脉粥样硬化和抗糖尿病作用。因此,血浆脂联素水平的稳态对全身健康至关重要。近期研究证实,低血清脂联素水平即低脂联素血症与生殖、消化、内分泌、心血管等全身性疾病的发生及预后不良有关。揭示低脂联素血症的发病机制,提高血清脂联素水平,对预防和治疗相关全身性疾病,特别是胰岛素抵抗和T2D具有重要的临床意义。流行病学调查发现,低脂联素血症与牙周炎有关。

牙周炎是一种发生在口腔内的持续性炎症性疾病。龈下微生物生态失调是一个重要的病理特征。牙龈下菌群紊乱会导致致病微生物和有毒产物的显著增加,引起牙龈、牙周韧带和牙槽骨等牙周支撑组织从多颗甚至全部牙齿上的炎症和破坏性吸收。最新报告显示,全球牙周炎患病率高达50%,其中重度牙周炎患者达11亿人。牙周炎患者血清脂联素水平明显低于牙周健康人群,这可能导致低脂联素相关疾病的发生。然而,牙周炎如何引起低脂联素血症尚未见报道。牙周炎患者的病原微生物和有毒产物可从牙周袋上皮组织溃疡进入体循环,导致菌血症、内毒素血症或在远离口腔的其他组织定植。这些毒力因子诱导或加重组织的免疫和炎症反应或代谢功能障碍。由牙龈卟啉单胞菌分泌的脂多糖(P.g -LPS)是细菌外壁的组成部分。既往研究表明,P.g -LPS是牙周炎对全身健康负面影响的关键毒力因子之一,P.g -LPS不仅可引起局部牙周破坏,还可引起内毒素血症,介导肝脏和内脏脂肪组织的病理改变。内脏脂肪组织是脂联素合成和分泌的重要部位。任何导致内脏脂肪细胞脂联素合成和分泌紊乱的原因,如遗传、环境等因素,都是低脂联素血症的重要原因。研究发现,牙周炎可导致内脏脂肪细胞分泌异常,特别是脂肪因子白介素-6 (il -6)、肿瘤坏死因子-α (TNF-α)、瘦素分泌增加,脂联素分泌减少。
因此,本研究通过结扎牙周建立大鼠牙周炎模型,体外建立pg - lps刺激的内脏脂肪细胞模型,探讨ire1 α介导的ERS与低脂联素血症的关系,初步揭示牙周炎所致低脂联素血症的潜在机制。
方法:采用双侧上颌第二磨牙局部结扎法建立大鼠牙周炎模型。用牙龈卟啉单胞菌脂多糖(P.g-LPS)体外刺激内脏脂肪细胞。检测葡萄糖调节蛋白78 (GRP78)、肌醇需要蛋白1α (IRE1α)、蛋白激酶rna样ER激酶(PERK)、活化转录因子6 (ATF6)和脂联素的表达水平。体外将IRE1α慢病毒转染到内脏脂肪细胞中,并在大鼠附睾脂肪组织中注射IRE1α抑制剂(KIRA6),检测并验证ERS对内脏脂肪细胞中脂联素表达的影响。

表1 实时定量pcr基因引物序列
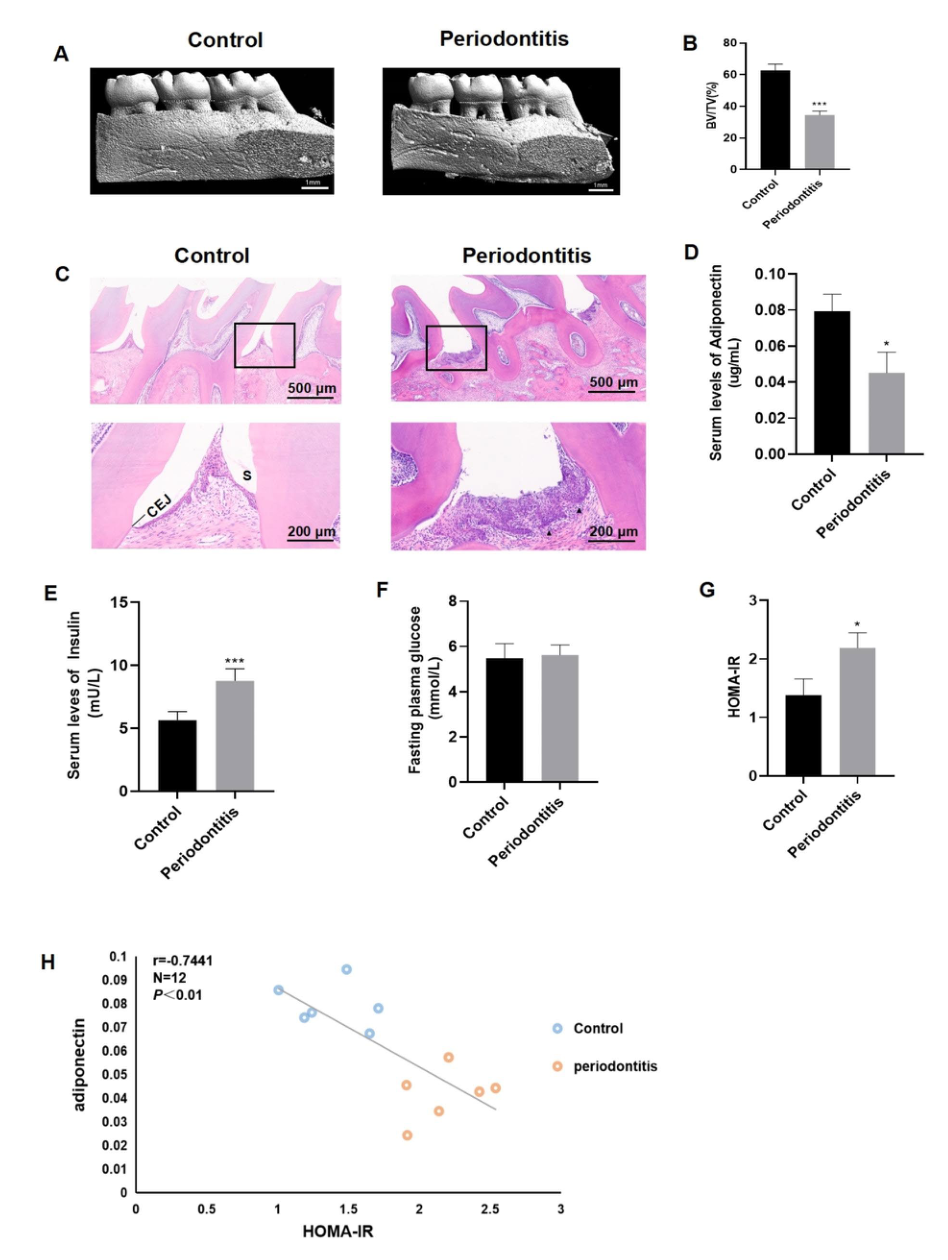
图1:大鼠牙周炎引起的低脂联素血症和胰岛素抵抗。(A) Micro-CT图像显示对照组和牙周炎组牙槽骨具有代表性的三维轮廓。(B)牙周炎患者上颌骨BV/TV值明显降低。(C) HE染色显示大鼠牙周组织的病理改变。对照组(比例尺,500 μm)用黑框表示特写(比例尺,200 μm)牙周结构正常。牙周炎组(刻度条,500 μm),黑框表示近距离(刻度条,200 μm)显示结缔组织上皮向牙根迁移,炎症细胞浸润(黑色箭头)。(D)牙周炎组血清脂联素水平明显低于对照组。(E)牙周炎组空腹血浆胰岛素水平明显升高。(F)两组空腹血糖水平无显著差异。(G)牙周炎组HOMA-IR高于对照组。(H)脂联素与HOMA-IR呈负相关。CEJ =骨水泥-牙釉质交界处,S =沟,数据以平均值±SD表示。*P < 0.05, ***P < 0.001与对照组比较

图2 牙周炎诱导大鼠内脏脂肪细胞内脂联素表达降低。(A)牙周炎组GRP78、IRE1α和PERK mRNA水平显著高于对照组,而ATF6无变化。(B) GRP78、IRE1α、p-IRE1α、PERK、p-PERK和ATF6表达的Western blotting图像。(C) GRP78和p-IRE1α/IRE1α的表达显著高于对照组,而p-PERK/PERK和ATF6的表达无明显变化。(D)牙周炎组脂联素mRNA水平低于对照组。(E)脂联素表达的Western blotting图像。(F)脂联素表达低于对照组。样品来自同一实验,并且印迹是并行处理的。全长印迹见补充文件1。图5 . GRP78 =葡萄糖调节蛋白78;IRE1α =肌醇需要蛋白1α;p-IRE1α = IRE1α磷酸化水平;PERK =双链rna依赖性蛋白激酶(PKR)样ER激酶;p-PERK = PERK磷酸化水平;活化转录因子6。数据以平均值±SD表示。*P < 0.05, **P < 0.01
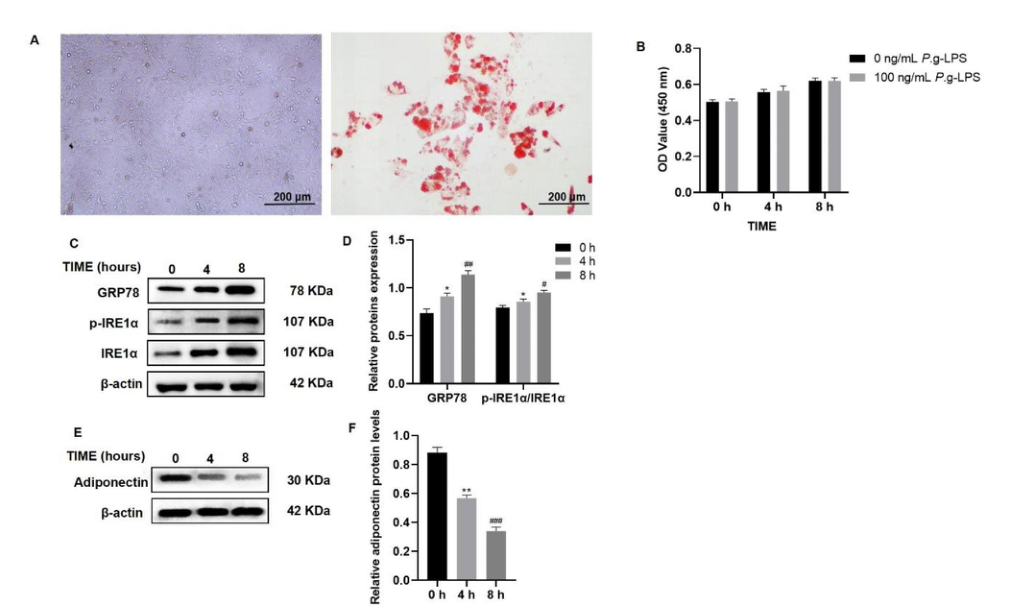
图3 P.g-LPS诱导体外内脏脂肪细胞内质内质网和下调脂联素表达。(A)光学显微镜图像显示内脏脂肪细胞培养和油红O染色,用于识别脂肪细胞(标尺,200 μm)。(B) p - g- lps浓度对内脏脂肪细胞增殖的CCK8分析。(C) 100 ng/mL P.gLPS作用0、4和8小时后内脏脂肪细胞中GRP78、IRE1α和p-IRE1α表达的Western blotting图像。(D) GRP78和p-IRE1α/IRE1α表达呈时间依赖性上调。(E) 100 ng/mL P .g- lps处理内脏脂肪细胞0、4和8小时后脂联素表达的Western blotting图像。(F)脂联素表达呈时间依赖性显著降低。样品来自同一实验,并且印迹是并行处理的。全长印迹见补充文件1。图5 .数据以平均值±SD表示。与0 h组比较,*P < 0.05, **P < 0.01;与4 h组比较,#P < 0.05, ##P < 0.01, ##P < 0.001
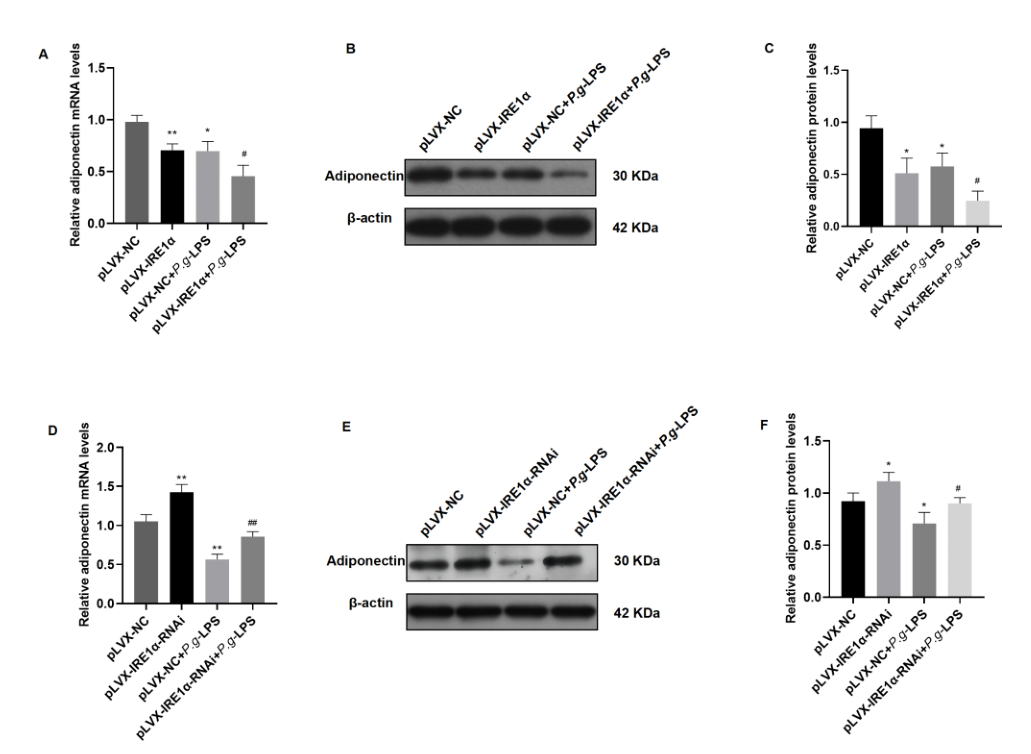
图4 IRE1α过表达和抑制对内脏脂肪细胞脂联素表达的影响。(A) pLVX-IRE1α组脂联素mRNA水平低于pLVX-NC组。与pLVX-NC + p - g- lps组相比,pLVX-IRE1α + p - g- lps组脂联素mRNA水平显著降低。(B)脂联素表达的Western blotting图像。(C)脂联素在pLVX-IRE1α组的表达低于pLVX-NC组。与pLVX-NC + p - g- lps组相比,pLVX-IRE1α + p - g- lps组脂联素表达降低。(D)与pLVX-NC组相比,pLVX-IRE1α-RNAi组脂联素mRNA水平升高。pLVX-IRE1α-RNAi + p - g- lps组脂联素mRNA水平高于pLVX-NC + p - g- lps组。(E)脂联素表达的Western blotting图像。(F)与pLVX-NC组相比,pLVX-IRE1α-RNAi组脂联素表达升高。脂联素在pLVX-IRE1α-RNAi + P.g- lps组的表达高于pLVX-NC + P.g- lps组。样品来自同一实验,并且印迹是并行处理的。全长印迹见补充文件。图5 .数据以平均值±SD表示。与pLVX-NC组比较,*P < 0.05, **P < 0.01;与pLVX-NC + Pg-LPS组比较,#P < 0.05, ##P < 0.01
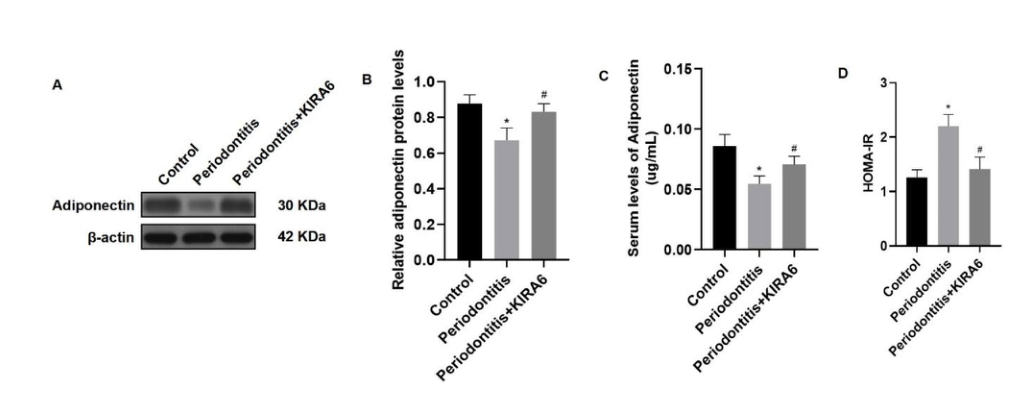
图5:附睾脂肪组织注射KIRA6可改善牙周炎大鼠低脂联素血症和胰岛素抵抗。(A)脂联素表达的Western blotting图像。(B)牙周炎+ KIRA6组脂联素表达高于牙周炎组。(C)牙周炎+ KIRA6组血清脂联素水平高于牙周炎组。(D)牙周炎+ KIRA6组HOMA-IR低于牙周炎组。样品来自同一实验,并且印迹是并行处理的。全长印迹见补充文件。图5 .数据以平均值±SD表示。*与对照组比较P < 0.05,与牙周炎组比较P < 0.05
结果:牙周炎大鼠出现低脂联素血症,内脏脂肪细胞内ERS关键蛋白GRP78及IRE1α (p-IRE1α)/IRE1α磷酸化水平升高,脂联素蛋白表达降低。KIRA6注射到牙周炎大鼠附睾脂肪组织后,内脏脂肪细胞内脂联素水平升高,血清脂联素水平有一定程度恢复。p- g- lps诱导的内脏脂肪细胞中GRP78和p-IRE1α/IRE1α蛋白表达水平升高,脂联素蛋白表达降低。在p.g - lps刺激的内脏脂肪细胞中,过表达IRE1α进一步抑制脂联素的表达,相反,抑制IRE1α恢复脂联素的表达。
结论:牙周炎可诱导内脏脂肪细胞内的ERS,导致低脂联素血症。IRE1α是内脏脂肪细胞中调节脂联素表达的关键蛋白。
原始出处:
Wu Q, Yan L, Wu X,Experimental periodontitis induced hypoadiponectinemia by IRE1α-mediated endoplasmic reticulum stress in adipocytes.BMC Oral Health 2023 Dec 21;23(1)


