【AJH】Ph+ ALL异基因移植后TKI维持治疗受限于毒性:真实世界研究
时间:2024-06-08 06:01:28 热度:37.1℃ 作者:网络
Ph+ ALL移植后TKI维持
异基因造血细胞移植(HCT)是费城染色体阳性(Ph+)急性淋巴细胞白血病(ALL)潜在的治愈手段,但复发仍较为常见的,也是死亡的主要原因。预防复发的策略是之一为HCT后给予酪氨酸激酶抑制剂(TKI)维持治疗,但相关报道多为一代TKI伊马替尼,而新一代TKI的数据有限。
希望之城国家医疗中心(City of Hope NationalMedical Center)对185例接受HCT和TKI维持治疗的Ph+ ALL患者进行了真实世界回顾性分析,重点关注TKI的初始选择、治疗时间、毒性和剂量调整。近日发表于《American Journal of Hematology》。

研究结果
患者、疾病和移植特征
研究纳入2003年到2021年期间接受了HCT和TKI维持治疗的Ph+ ALL患者共185例。HCT后最常见的初始TKI为达沙替尼(60.0%,n=111),其次为伊马替尼(27.0%,n=50)、ponatinib (9.2%,n=17)、尼洛替尼(3.2%,n=6)和bosutinib (0.5%,n=1)。148例(80.0%)患者接受预防性TKI维持,37例(20.0%)患者接受抢先性(preemptive)TKI维持。预防性维持开始的中位数为71天,抢先性维持开始的中位数为90天。初始TKI累积暴露的中位数为289天,而包括第二次和第三次TKI维持的总TKI累积暴露为416天。分别有27例(54.0%)、46例(41.4%)和13例(76.5%)患者完成≥12个月的初始伊马替尼、2G-TKI和ponatinib治疗;对于所有接受TKI的患者,102例(55.1%)完成≥1年TKI维持。
表1总结了整个队列以及接受伊马替尼、2G-TKI和ponatinib的患者的基线和移植特征。在2016年至2021年期间,更多的患者接受了2G-TKI和ponatinib,更多患者处于CR1而非CR2+,在伊马替尼和2G-TKI组中,MRD阴性的患者多于ponatinib组。此外,与接受其他TKI维持的患者相比,接受伊马替尼TKI维持的患者更多接受相合同胞供者HCT,而接受单倍型相合HCT的可能性更小。此外,在ponatinib组,更多的患者接受他克莫司、霉酚酸酯和后置环磷酰胺治疗。最后,比较接受抢先性维持治疗的患者与接受预防性维持治疗的患者时,基线特征的唯一差异为预防性维持治疗队列中HCT前MRD阳性率较高(62% vs 21%,p<0.01)。
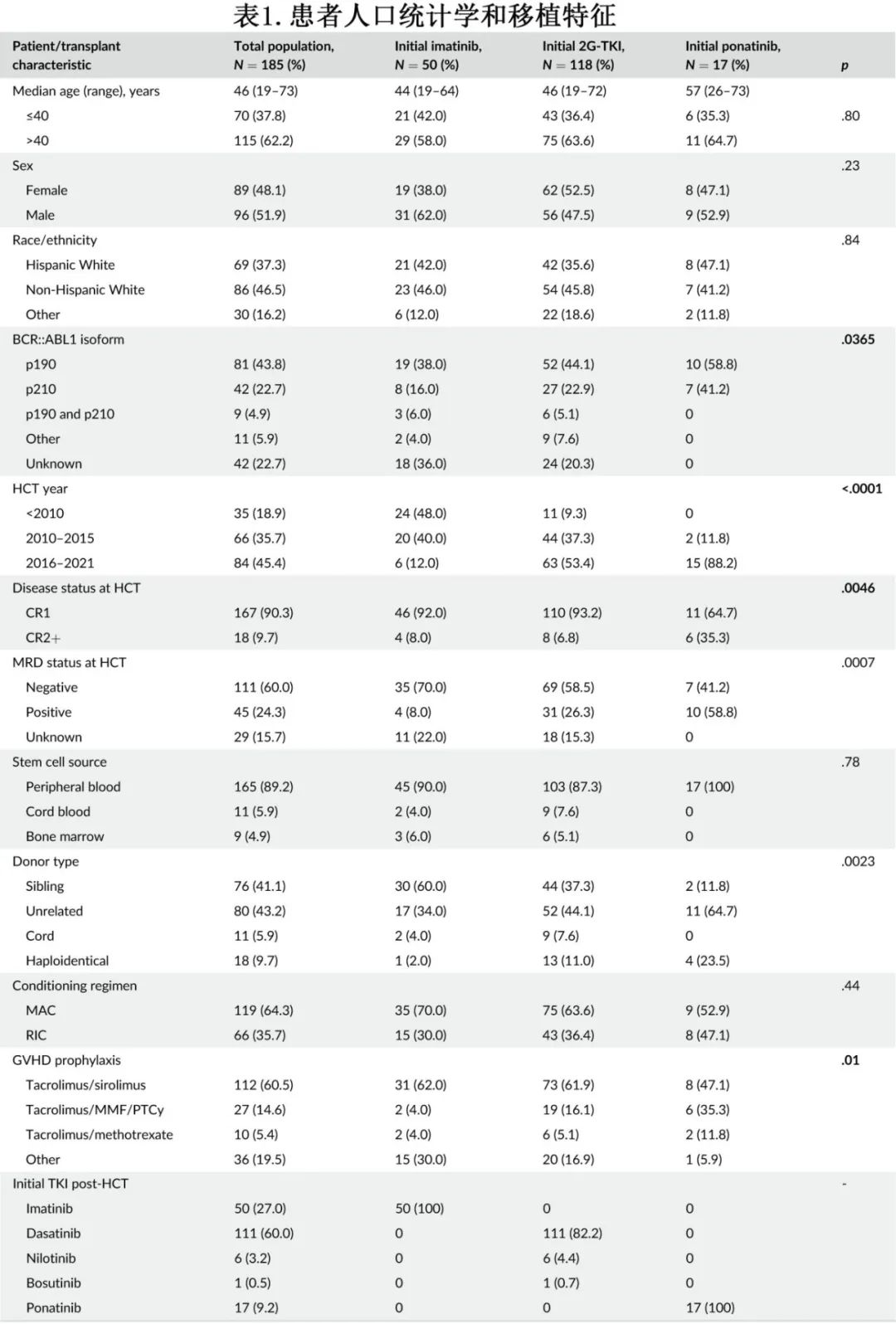
分析了同一时期103例未接受HCT后TKI维持的患者,与TKI维持组相比,无TKI维持组的1年OS和PFS较低、NRM较高。
TKI维持治疗的毒性
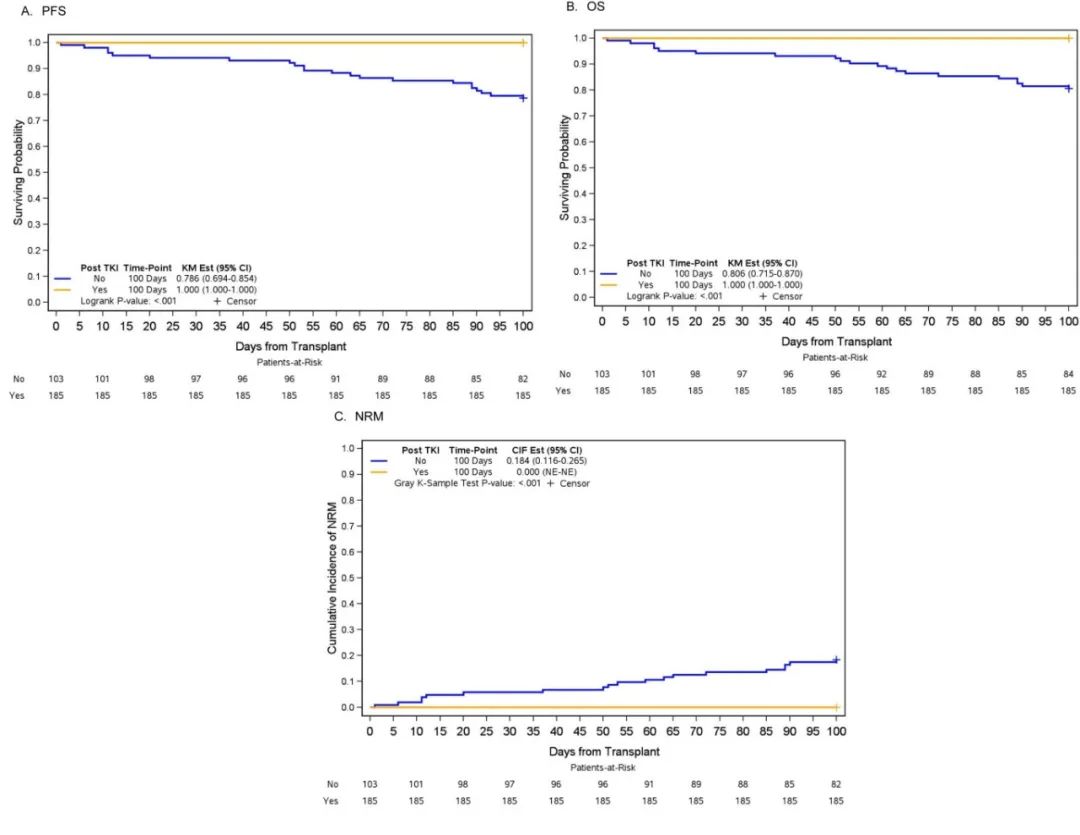
在整个维持期间,77例患者(41.6%)因毒性需要减少初始TKI剂量,包括19例患者(10.2%)需要减少≥2次剂量。138例(74.6%)患者的TKI维持治疗短暂中断,包括121例(65.4%)患者因毒性而中断。66例(35.7%)患者因毒性未完成TKI维持治疗;69例(37.3%)患者因毒性停用1个TKI, 11例(5.9%)患者停用2个TKI。
18例(36.0%)患者由于毒性需要减少初始伊马替尼维持剂量,7例(14.0%)患者需要减少≥2次剂量;59例(50.0%)患者由于毒性需要减少2G-TKI初始维持剂量,12例(10.2%)患者需要减少≥2次剂量;伊马替尼、2G-TKI和ponatinib初始维持组分别有27例(54.0%)、86例(72.9%)和8例(47.1%)(p=0.01)因毒性暂时中断,分别有19例(38.0%)、61例(51.7%)和3例(17.6%)患者因毒性而停止初始维持治疗(p=0.02)。与2G-TKI相比,ponatinib作为初始TKI的患者维持时间更长:576.0天 vs 254.5天(P=0.02)。
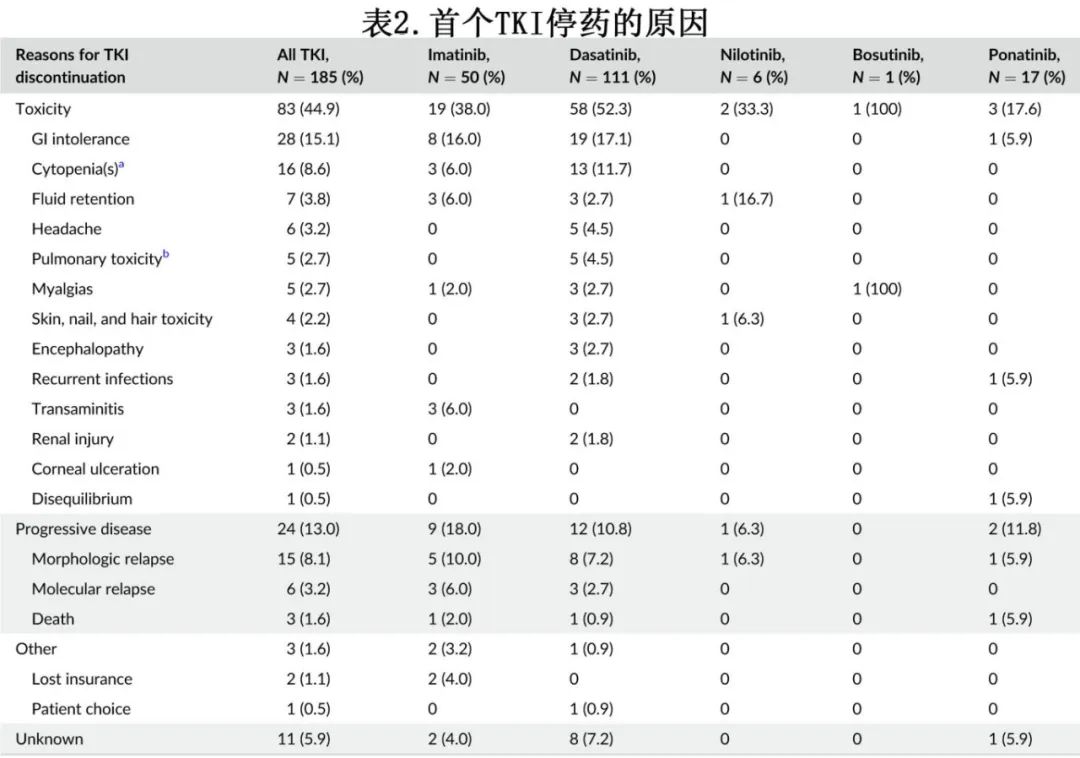
导致伊马替尼最初停药的最常见毒性包括胃肠道不耐受(16.0%,n=8)、血细胞减少(6.0%,n=3)和液体潴留(6.0%,n=3);最常见的导致2G-TKI停药的毒性包括胃肠道不耐受(16.1%,n=19)、血细胞减少(11.0%,n=13)、肺毒性(4.2%,n=5)和头痛(4.2%,n=5)。表2为停药原因。
患者结局
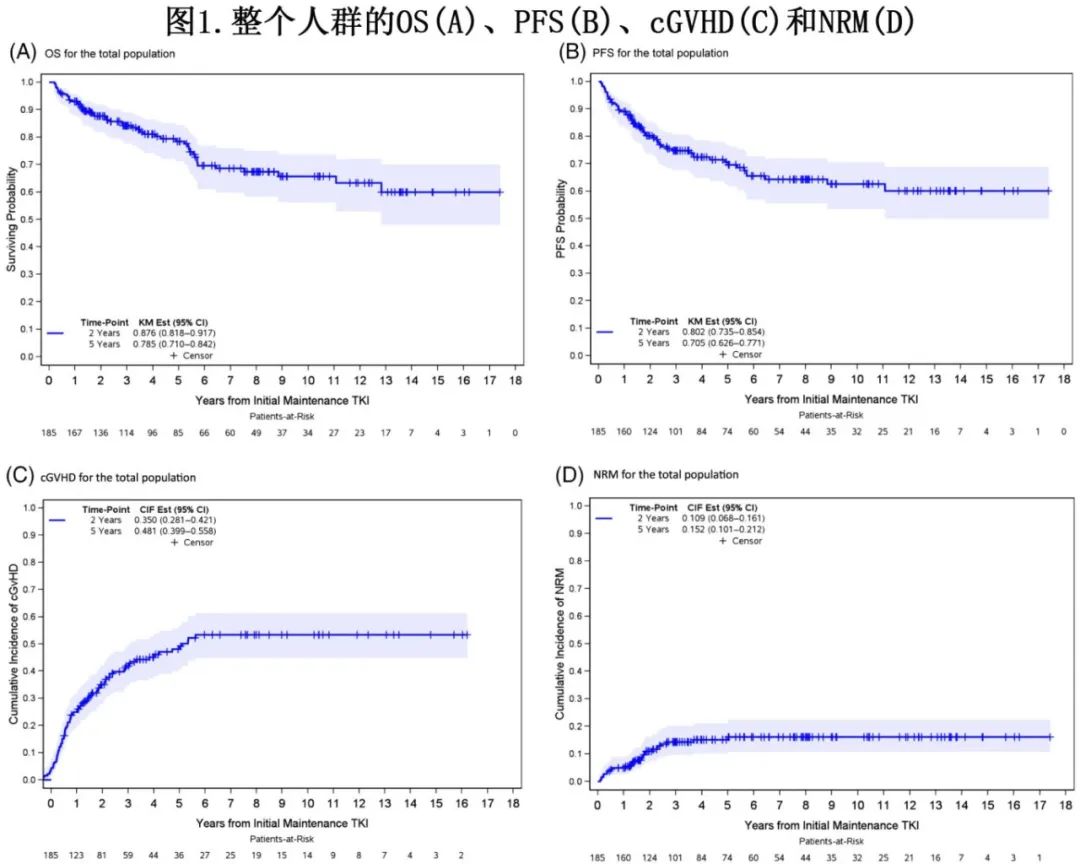
所有患者的中位随访时间为4.4年,存活患者的中位随访时间为5.3年。总体人群的中位OS和PFS未达到(图1A),2年和5年OS分别为88%和79%,2年和5年PFS分别为80%和71% (图1B);5年cGVHD和NRM率分别为48%和15%(图1C,D)。
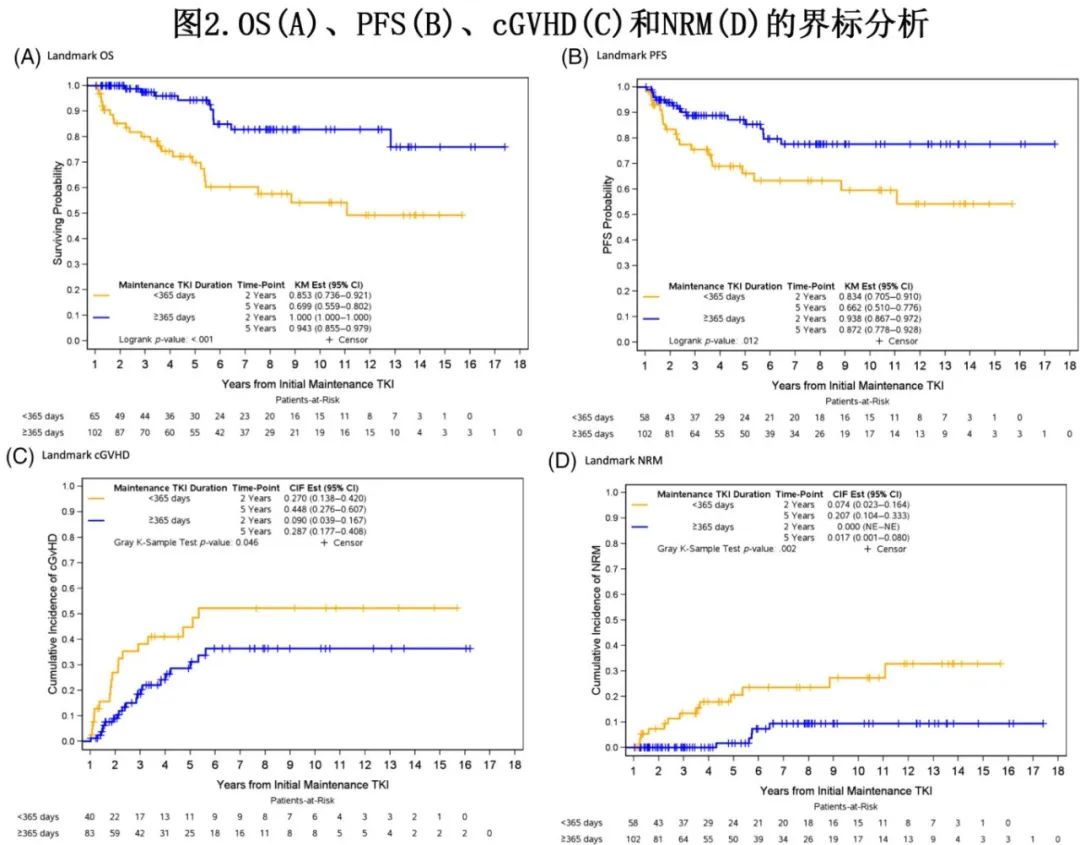
TKI维持治疗开始后1年的界标分析显示,完成≥365天TKI维持的患者相对于<365天的患者,5年OS (94% vs 70%,p<0.01)和PFS(87% vs 66%,P=0.01)均显著改善(图2A、B),且5年cGVHD(29% vs 5%,p=0.046)和NRM(2% vs 21%,p<0.01)较低(图2C,D)。值得注意的是,两组的5年CIR没有差异(11% vs 12%,P=0.87)。
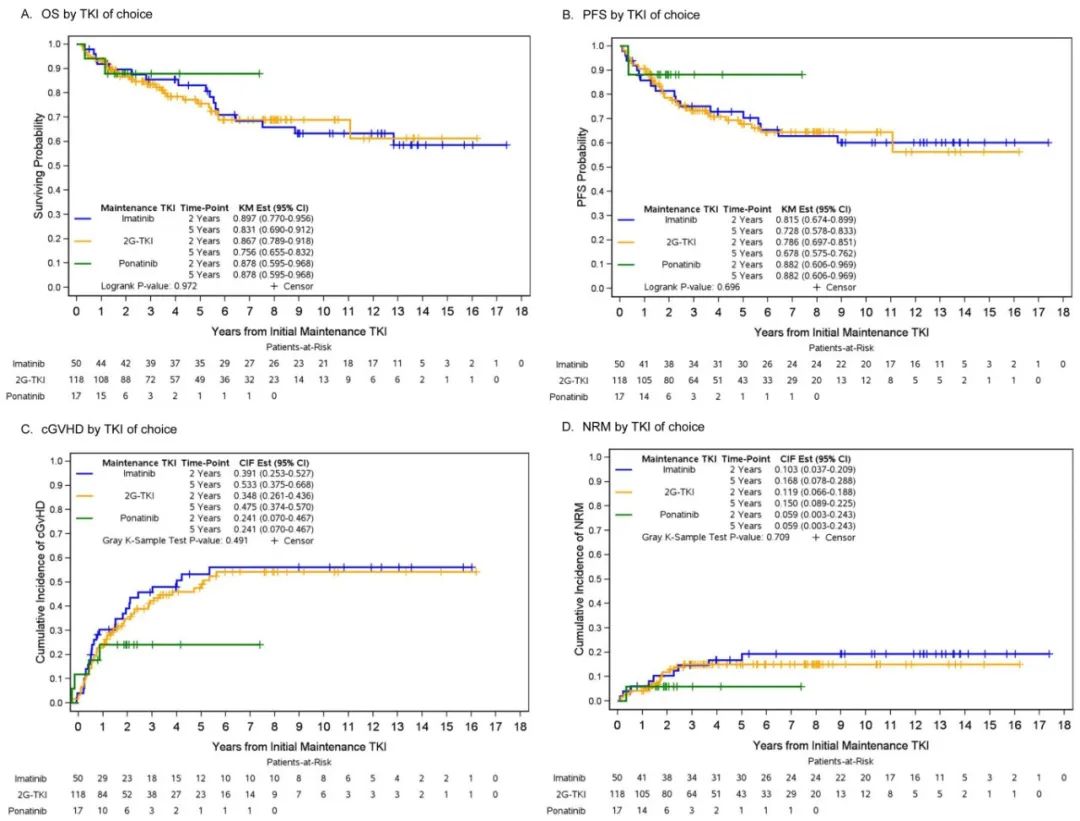
伊马替尼组、2G-TKI组和ponatinib组的2年OS分别为90%、87%和88% (p=0.97),2年PFS分别为82%、79%和88%,2年cGVHD累积发生率分别为37%、33%和14% (p=0.19),2年NRM分别为10%、12%和6% (p=0.71),2年累积复发率分别为10%、10%和6% (p=0.71)。
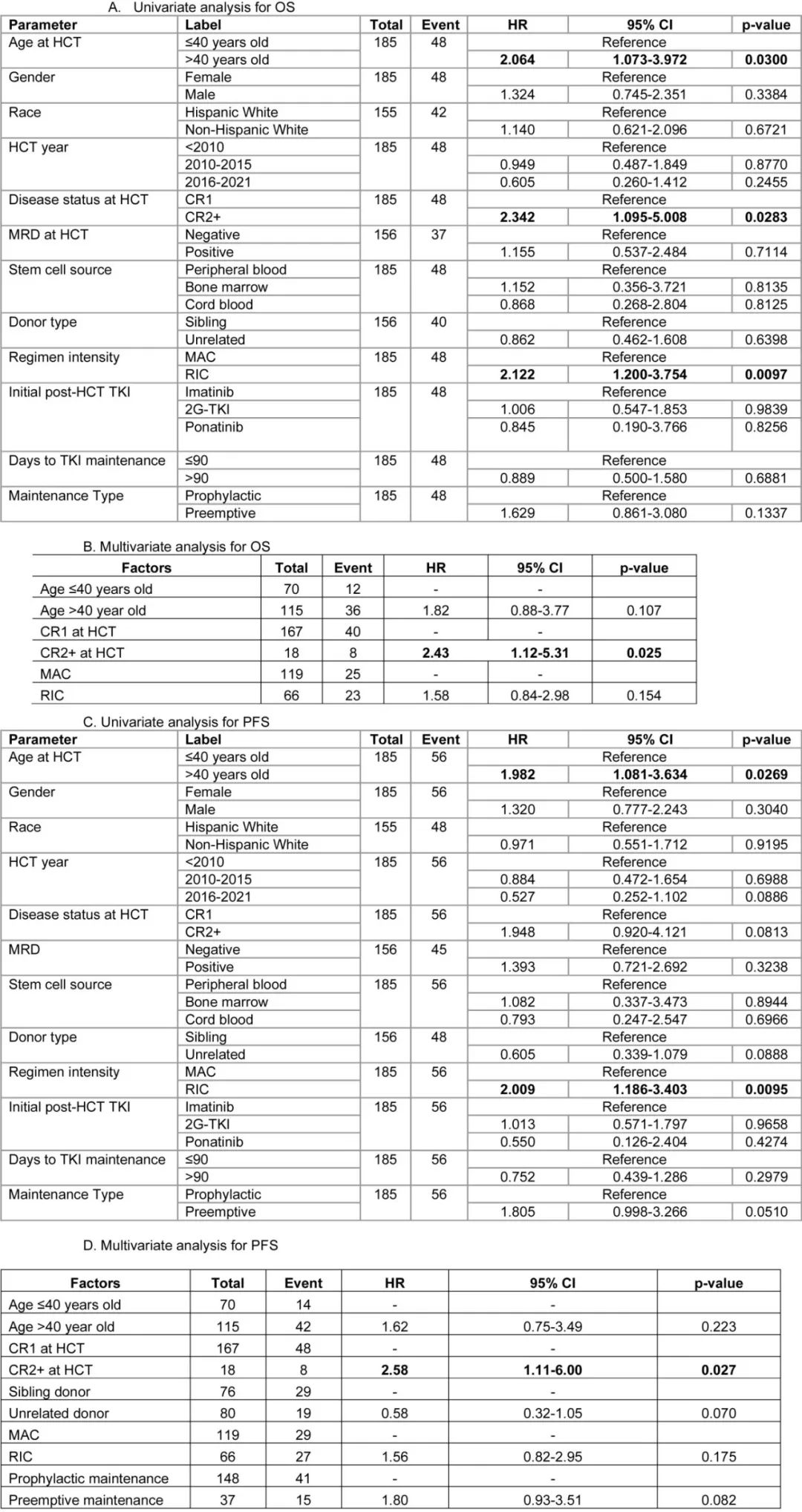
单变量和多变量分析显示了各种因素与总体人群OS和PFS的相关性。在单变量分析中,HCT年龄>40岁、CR2+相对于CR1)、减低强度预处理(RIC)(相对于清髓性预处理)与较差的OS相关,而年龄>40岁、HCT CR2+、相合非亲缘供者、RIC和维持治疗类型(预防性相对于抢先性)与较差的PFS相关。在多变量分析中,HCT时CR1是唯一与OS和PFS改善相关的变量。
总结
该回顾性研究纳入185例接受HCT和TKI维持治疗的Ph+ ALL患者,50例(27.0%)接受伊马替尼,118例(63.8%)接受2G-TKI, 17人(9.2%)接受ponatinib。共77例患者(41.6%)因毒性需要减少初始TKI剂量。66例(35.7%)患者因毒性未完成维持治疗;69例(37.3%)患者因毒性停用1个TKI, 11例(5.9%)患者停用2个TKI。由于毒性,分别有19例(38.0%)、61例(51.7%)和3例(17.6%)患者停止初始伊马替尼、2G-TKI和ponatinib维持治疗(p=0.002)。与2G-TKI相比,ponatinib作为初始TKI的患者TKI维持时间更长(576.0天 vs 254.5天,P=0.02)。最初停用TKI的最常见原因包括胃肠(GI)不耐受(15.1%)、血细胞减少(8.6%)和液体潴留(3.8%)。5年总生存率和无进展生存率分别为78%和71%。
该真实世界大型队列研究表明, HCT后TKI维持治疗存在挑战,因为毒性导致TKI中断、停药和剂量减少较为常见。通过更大规模的前瞻性研究探索毒性更小的TKI或其他减少HCT后复发的新方法,或有助于改善Ph+ ALL患者的HCT预后。
参考文献
Othman T, Koller P, Tsai N-C, et al.Toxicities associated with tyrosine kinase inhibitor maintenance following allogeneic hematopoietic cell transplantation in Philadelphia chromosome-positive acute lymphoblastic leukemia. Am J Hematol. 2024;1‐11. doi:10.1002/ajh.27378


