Mol Psychiatry:iPSC 衍生的后脑类器官用于评估草酸艾司西酞普兰治疗阿尔茨海默病神经精神症状的反应
时间:2024-06-24 10:00:59 热度:37.1℃ 作者:网络
阿兹海默病是全球首要的失智症发病原因,病发机制难以揭示,治疗效果有限。其病理表现包括Aβ沉积和神经原纤维缠结。血清中5-羟色胺的合成酶突变相关,5-羟色胺在中枢神经系统内部合成并调控情绪等功能。研究显示阿兹海默病早期5-羟色胺系统损害相关。选择性5-羟色胺再摄取抑制剂治疗神经心理症状,但对部分病人无效。诱导多能干细胞可重现人体差异性,通过体外分化成脑细胞,建立个体化药敏性药效筛查平台。

本研究计划通过体外分化,将健康人及带症状和无症状阿兹海默病人中的iBNS干细胞转化为5-羟胺神经的脑区小体,进而建立个体化药物筛查平台。筛选艾斯西酞普兰,评估系统功能,为个体化精准治疗提供依据。这将有助于深入研究阿兹海默病病理机制和个体差异,优化临床治疗策略。
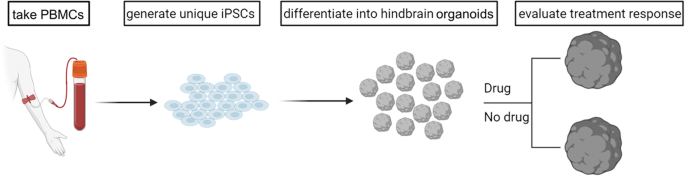
图1
研究人员首先从3名健康人和3名阿尔茨海默病患者体外获得外周血单个核细胞。随后利用质粒将细胞转化为iPS细胞。为建立5-HT能神经元体外模型,研究人员运用WNT/SHH通路在3D类器官中对iPS细胞进行分化诱导。分化效率通过流式细胞术检测细胞表面标志物的表达情况进行评价。同时,研究人员利用自行开发的图像分析算法对类器官在分化过程中的形态变化进行定量分析。此外,还通过qRT-PCR和免疫细胞化学技术检测各重要标志物的mRNA和蛋白表达水平。
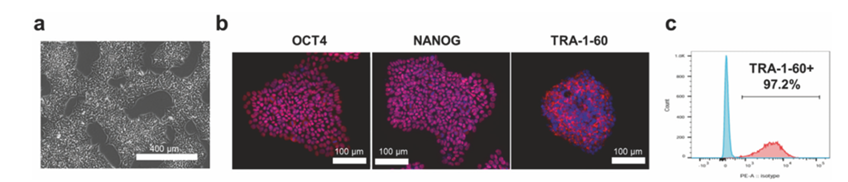
图2:PBMCs重编程为iPSC
为验证该模型的有效性,研究人员采用ELISA法评价细胞培养上清液中的5-羟色胺含量,并检测精神药物氧西他普拉对其影响。统计学分析采用SPSS软件进行一致性检验和组间比较,全面评价该人源iPSC模型在5-HT能神经元研究中的可靠性。研究结果为相应疾病机制研究提供了一个可靠的体外模型平台。
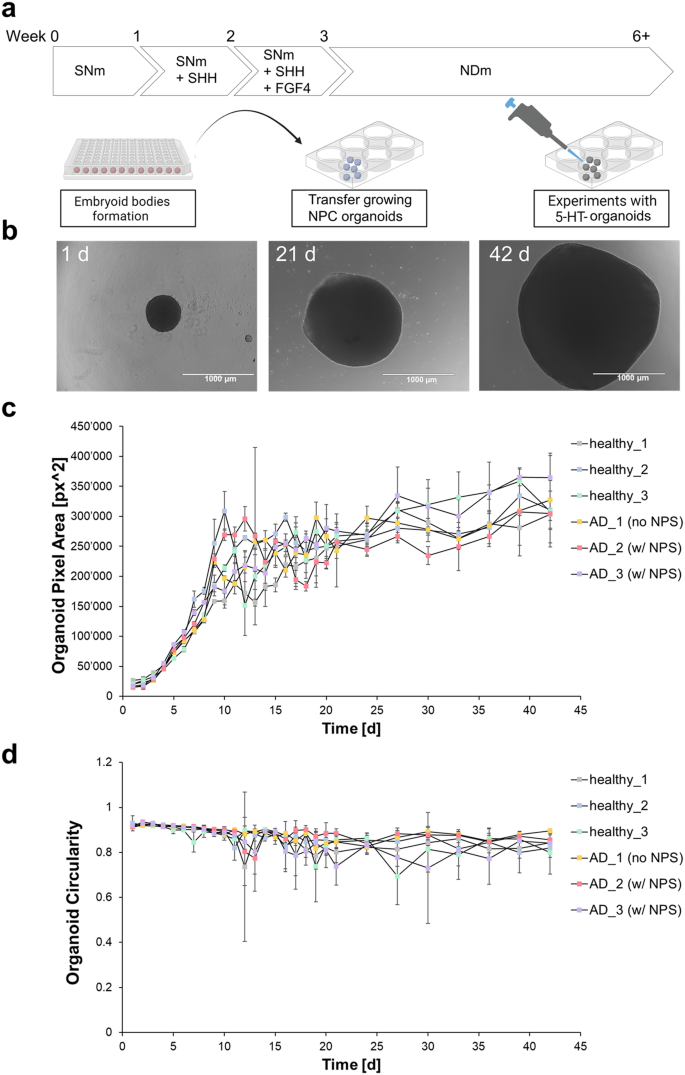
图3:从iPSC生成5-HT类器官
本研究从3名健康人和3名阿尔茨海默病患者取得的外周血单个核细胞中,成功致增多能性恒定细胞系。随后,采用分化诱导方法将这些细胞分化成结构完整的5-HT脑干球体模型。通过流式细胞术、qRT-PCR及免疫荧光等手段,验证细胞中表达了神经元标志物TUJ1和5-HT生物合成标志物TPH2,表明球体中含有5-HT神经元。且经过一个月的培养,球体能够稳定分泌5-HT。
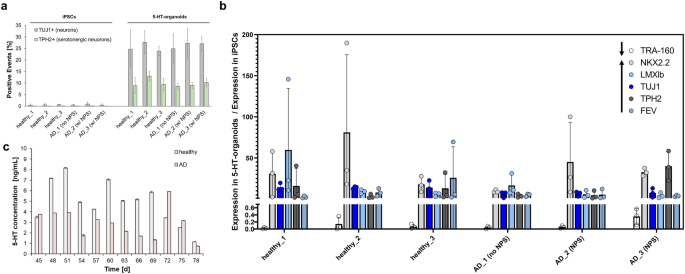
图4:5-HT类器官的表征
在建立此脑干球体模型的基础上,研究以抗忧郁药艾司西酞普兰为药物进行干预试验。结果显示,艾司西酞普兰能够在一定浓度下显著增加球体分泌5-HT的水平,且此效应具有剂量依赖性。但不同个体对药物的反应不完全相同,初步证实个体间存在差异。
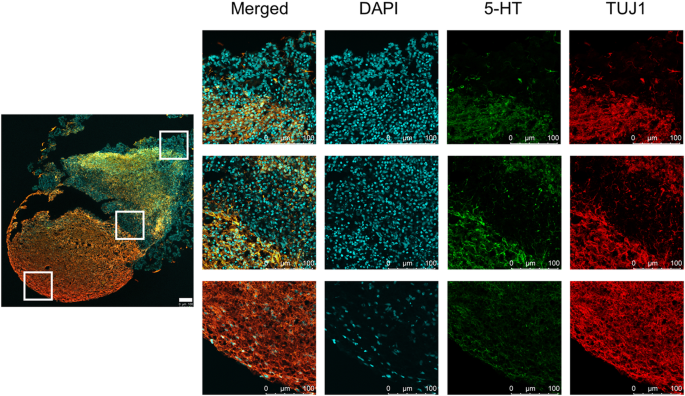
图5:5-HT类器官的免疫细胞化学
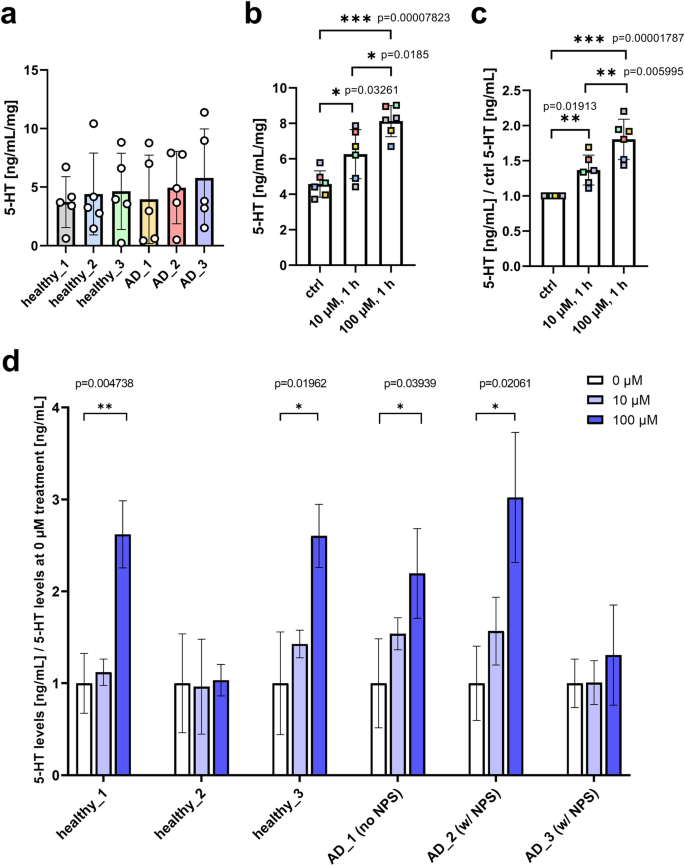
图6:草酸艾司西酞普兰1h处理对5-HT类器官血清素释放的影响
综上所述,本研究成功构建了人源iPSC细胞导出的5-HT脑干球体模型,该模型或对阿尔茨海默病神经精神症状机制研究和新药评价提供参考,在精神药理研究中具有重要价值。
文献出处:
Zivko C, Sagar R, Xydia A, Lopez-Montes A, Mintzer J, Rosenberg PB, et al. iPSC-derived hindbrain organoids to evaluate escitalopram oxalate treatment responses targeting neuropsychiatric symptoms in Alzheimer’s disease. Mol Psychiatry 2024:10.1038/s41380-024-02629-y. https://doi.org/10.1038/s41380-024-02629-y.


