复旦大学孙涛/蒋晨团队最新Biomaterials综述:仿生策略用于胶质母细胞瘤免疫治疗的最新研究进展
时间:2024-07-02 16:00:39 热度:37.1℃ 作者:网络
免疫治疗是当前被认为最有希望治愈肿瘤的一种方式,目前针对胶质母细胞瘤(GBM)也的确存在许多免疫治疗的思路。然而,免疫治疗药物体内命运差、缺乏血脑屏障(BBB)穿透性和GBM靶向性、引起的免疫效应单一等问题的存在并未使这些免疫治疗思路的效果达到理想的预期,即使在常规递药系统的帮助下也收效甚微。仿生策略是通过模仿自然界生物体中某些巧妙的结构或者功能来解决药物递送过程中遇到的重大挑战。基于生物体结构和功能的多样性,在仿生策略指导下的仿生递药系统不仅为多种免疫治疗药物的共递送提供了一种简易制备的平台,而且其高生物相容性以及天然跨越BBB和靶向GBM的能力也为实现和增强GBM的免疫治疗提供了可能。
【最新综述】
基于此,复旦大学药学院孙涛/蒋晨团队全面回顾了当前针对GBM免疫治疗的各种思路和药物,并分析了免疫治疗药物在实现GBM免疫治疗过程中面临的各种障碍,以及从功能和结构的角度总结了克服上述障碍的相应仿生策略。最后,作者探讨了用于GBM免疫治疗的仿生策略的临床转化情况和未来发展方向。相关综述以“Recent Advances in Biomimetic Strategies for the Immunotherapy of Glioblastoma”为题在线发表在Biomaterials. 博士研究生游昊宇为该论文的第一作者。

【文章要点】
GBM属于高级别脑胶质瘤(IV级),最致命并且最难治疗,病人的中位生存期只有4-15个月。然而,由于其强浸润性,肿瘤和正常脑组织边界不清,导致手术并不能完全切除病变组织。另外,GBM高度异质性而产生的耐药也极大了限制了化疗药物的疗效。因此,当前GBM治疗的困境揭露了更加精确有效的新型疗法的必要性。
近年来,通过激活机体自身的免疫系统来攻击肿瘤的免疫疗法已经在其他侵袭性肿瘤(如晚期黑色素瘤和晚期非小细胞肺癌)中获得了巨大成功。而机体在硬脑膜窦周围的区域存在着对大脑的免疫监视这一现象也彻底改变了人们对大脑与免疫之间的看法,从将大脑视为与外周免疫细胞隔离且无法接触的器官,转变为一个与免疫系统保持紧密物理和功能交流的器官。这些研究为GBM的免疫治疗奠定了基础。进一步研究发现与外周肿瘤一样,GBM也是一种典型的“冷”肿瘤且具有高度免疫抑制的肿瘤微环境(TME),这表现为大量免疫抑制性细胞及其分泌物的浸润和免疫杀伤性细胞的耗竭。
因此,针对GBM这些特点,目前已经衍生出许多免疫治疗思路,包括提高GBM的免疫原性(诱导GBM免疫原性死亡、溶瘤病毒(OV)疗法以及肿瘤疫苗)、削弱GBM的免疫逃逸能力(阻断GBM中免疫检查点间的相互作用以及减少GBM免疫检查点的表达)、增加T细胞浸润以及恢复T细胞功能(嵌合抗原受体T细胞疗法(CAR-T)、细胞因子疗法以及免疫调节剂)、重编程胶质瘤相关巨噬细胞和小胶质细胞(GAM)(缓解乏氧、调控代谢以及免疫激动剂)和阻断调节性细胞(Tregs)和髓系来源的抑制性细胞(MDSCs)的募集等。
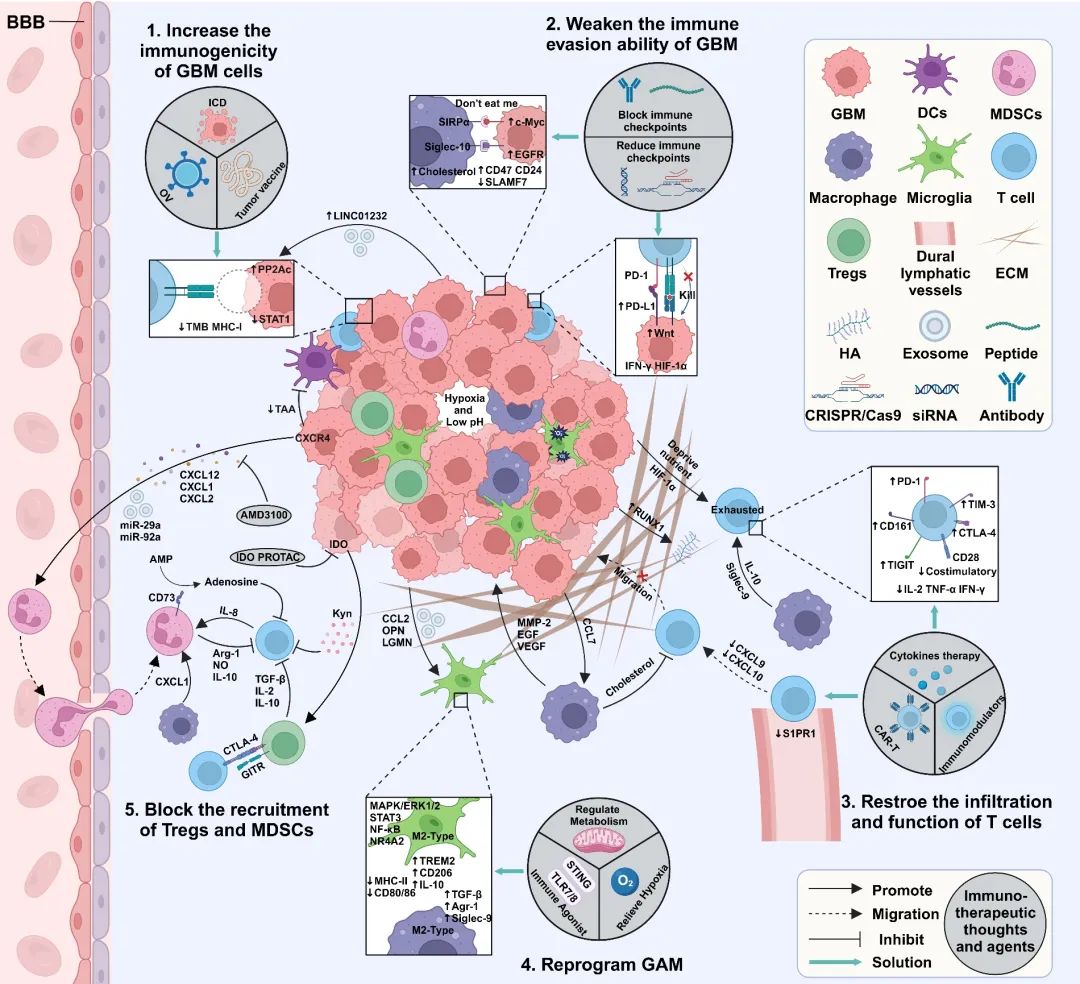
图1 针对GBM的免疫治疗思路以及药物
然而,尽管有各种各样的思路,GBM免疫治疗的效果并没有达到令人满意的预期。分析其本质的原因在于所有免疫治疗思路的实现其实都依赖于免疫治疗药物(例如免疫检查点抑制剂(ICI)、细胞因子、多肽疫苗以及小分子激动剂等)在GBM病灶发挥作用。但是大多数免疫治疗药物理化性质较差且体内命运不佳,直接系统给药很容易被机体的单核吞噬细胞系统清除,而提高给药剂量则会引起潜在的副作用。另外,这些药物还缺乏跨越BBB的能力和GBM靶向性,这进一步导致它们在病灶部位的蓄积量极低。值得一提的是,大部分免疫治疗药物只作用于某种细胞或者某条通路上,因此往往只能引起单一的免疫效应,这在复杂的TME中是远远不够的。常规的递药系统(例如胶束、脂质体、脂质纳米粒(LNP)等)虽然一定程度可以帮助免疫治疗药物改善上述困境,但效果有限且效率不高。同时这些递药系统本身也存在生物安全性、脱靶效应以及处方工艺复杂等问题。因此当前迫切需要新的方案将多种免疫治疗药物安全且精准递送至GBM病灶处,从而有效实现GBM的免疫治疗。
自然界中的生物在数百万年的进化过程中通过不断改变自身的结构和功能来适应外界的环境变化,而仿生策略是指通过模仿自然界的生物体中某些巧妙的结构和功能,并将其中的生物学原理与材料学或工程学结合,从而解决各个领域所面临的重大挑战。在药物递送方面,基于生物体结构和功能的多样性,在仿生观念的指导下构建的仿生递药系统除了具有高生物相容性以及天然跨越BBB能力和GBM靶向性的独特优势之外,还为多种药物的协同递送提供了一种简易制备且可大量获得的平台。因此,仿生策略在实现GBM免疫治疗方面拥有巨大潜力。基于此,作者从功能和结构的角度总结了克服GBM免疫治疗过程中所面临障碍的仿生策略(包括伪装成“自我”成分、模仿内源性细胞及其外泌体跨越BBB向GBM趋化迁移、模仿GBM细胞之间相互粘附接触与外周肿瘤脑转移、模仿细菌感染和病毒入侵、模仿大脑和GBM对营养物质进行摄取和利用以及模仿细胞对多种物质进行协调与分配等)。
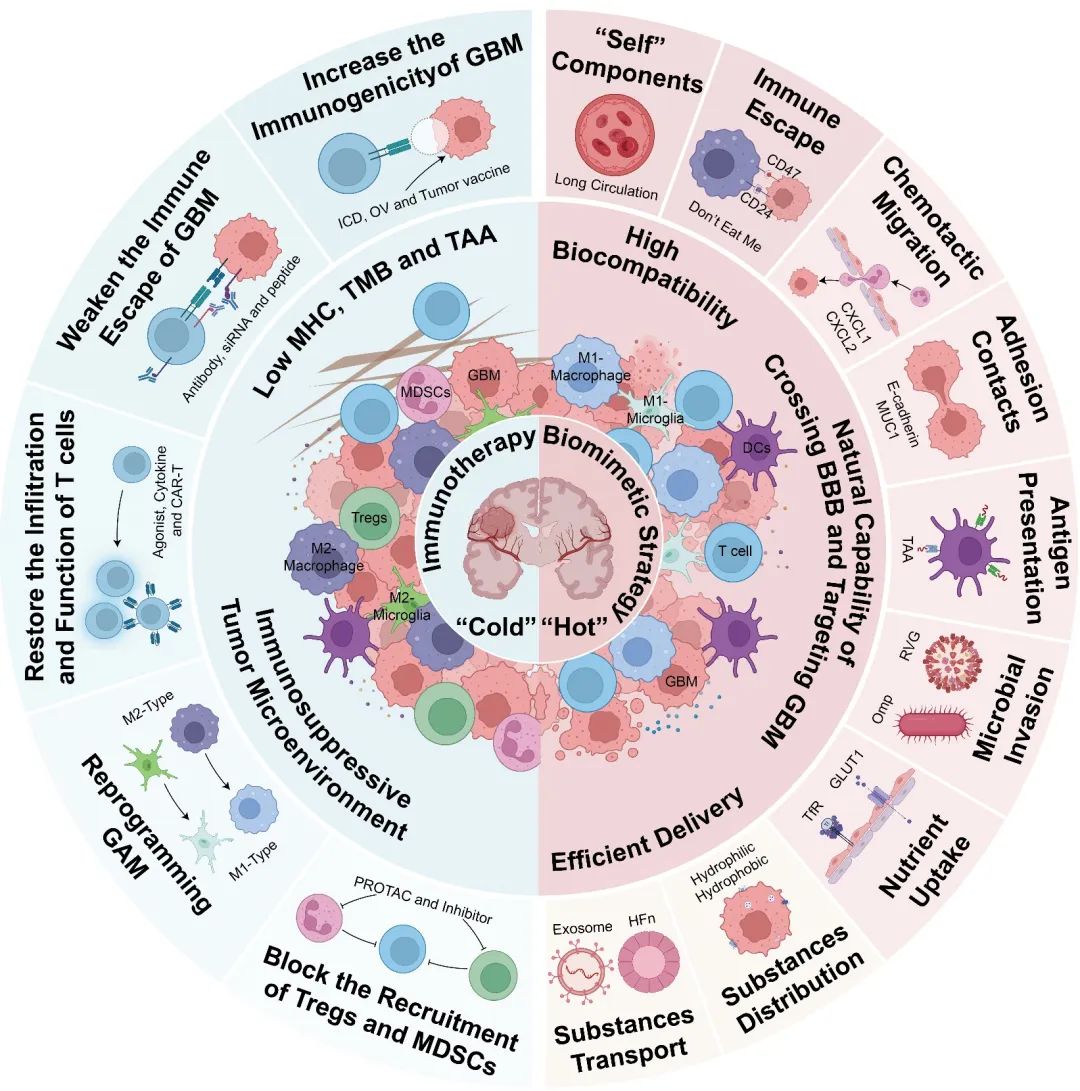
图2 用于GBM免疫治疗的仿生策略
【总结与展望】
尽管仿生策略十分匹配于GBM的免疫治疗,但必须承认的是,执行不同仿生策略的关键组分很大程度上都是相同的,包括各种细胞膜以及细胞外泌囊泡等; 虽然模仿细菌和病毒的仿生策略十分令人感兴趣且新颖独特,但是仍需再次强调的是,大脑作为人体最为关键的器官,它的重要性不言而喻。因此,生物安全性是在使用该仿生策略时必须着重考察的因素,必要时可以通过基因工程手段对它们进行改造,以进一步减弱它们的毒性;作者在综述中所讲述的仿生策略大部分是生物体灵感来源的,但这并不意味着仅局限于此。某些植物和水果的衍生物可为用于GBM免疫治疗的仿生策略的制定提供启发。
基于基因工程技术的发展,在目前用于GBM免疫治疗的仿生策略中,只有几项CAR-T疗法进入了临床试验阶段,而其他方面则均处于临床前研究阶段,这其中的原因是多方面的。第一,当前大部分研究都集中在仿生策略用于原位GBM的免疫治疗中,只有少量研究是将仿生策略用于术后GBM的免疫治疗中,这与临床相差较大。第二,与常规的递药系统一样,仿生递药系统目前也缺乏统一的质量标准。第三,执行仿生策略的关键组分大部分都是细胞衍生物(细胞膜和细胞外泌囊泡),直接将动物来源的异种生物成分用于人体治疗则必须考虑潜在的免疫原性风险。第四,即便是具备高生物相容性,仿生递药系统在体内的过程以及与体内成分之间的相互作用也尚未完全明确。最后,GBM的发生发展和免疫治疗效果存在个体差异大的情况,因此仿生策略还需要将个性化治疗纳入考虑的范围内。
当然,用于GBM免疫治疗的仿生策略向临床转化的道路虽然曲折艰难,但随着科学家对GBM独特性质(肿瘤微管的存在等)和与周围环境相互作用研究的进一步深入,它的发展前景依然是广阔的。尤其是最新的研究表明,GBM与周围神经系统系统形成了一种“致命共舞”,简单来说,GBM是一种电活性组织,它的发生发展在每时每刻都影响着周边细胞的同时也受到周边复杂神经回路环境的影响。因此在未来,作者认为GBM这些独特的病理特征以及与神经系统之间密切相互作用可以为仿生策略的开发提供大量灵感和方向并且进一步推动GBM免疫治疗的发展。
原文链接:
https://doi.org/10.1016/j.biomaterials.2024.122694


