CLIN CANCER RES | HER-Vaxx疫苗在HER2过表达晚期胃癌患者中的II期临床试验结果
时间:2024-07-30 16:04:04 热度:37.1℃ 作者:网络
HER2 是一种在人类恶性肿瘤中起着重要作用的表皮生长因子受体家族成员,在高达 30% 的胃癌中过度表达,尤其是在胃食管交界处 (GEJ) 或胃贲门肿瘤中,目前,针对 HER2 的单克隆抗体 (mAb) 曲妥珠单抗 (Herceptin®) 已成为 HER2 过表达晚期胃癌患者的标准一线治疗方案,然而,曲妥珠单抗的使用存在一些局限性,例如需要频繁注射、缺乏免疫记忆、潜在的毒性和高昂的费用,相比之下,主动免疫疗法(如疫苗)能够激活宿主免疫系统并形成免疫记忆,从而提供更持久的保护作用,HER-Vaxx 疫苗包含三种 B 细胞表位肽,其中包括曲妥珠单抗的结合表位,在之前的临床前研究和 I 期临床试验中,HER-Vaxx 疫苗表现出良好的免疫原性和安全性,并能够诱导 HER2 特异性抗体和细胞免疫反应,以及对肿瘤的生长抑制作用,该研究旨在评估 HER-Vaxx 疫苗联合化疗与单独化疗在 HER2 过表达晚期胃癌患者中的临床疗效和安全性。

方法
该研究是一项多中心、随机、开放标签的 II 期临床试验,共纳入 36 名 HER2 过表达晚期胃癌患者,年龄 ≥ 20 岁,既往未接受过化疗或放疗,患者被随机分配到单独化疗组 (n=17) 或 HER-Vaxx 疫苗联合化疗组 (n=19),HER-Vaxx 疫苗组中患者接受 50 µg 剂量的 HER-Vaxx 疫苗,分别在 Day 0、14、35 和 77 天进行接种,之后每 63 天接种一次,直至疾病进展,化疗组中患者接受以铂类为基础的化疗方案,每 21 天进行一次,共 6 个周期。主要终点为总生存期 (OS),次要终点为安全性评估,包括不良事件 (AE) 和治疗相关不良事件 (TEAE) 的发生率、无进展生存期 (PFS)、疾病客观缓解率和总缓解率肿瘤大小的变化。
研究结果
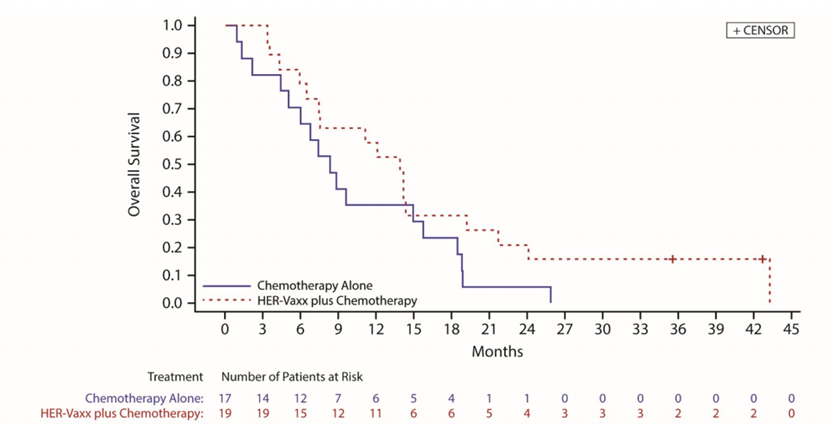
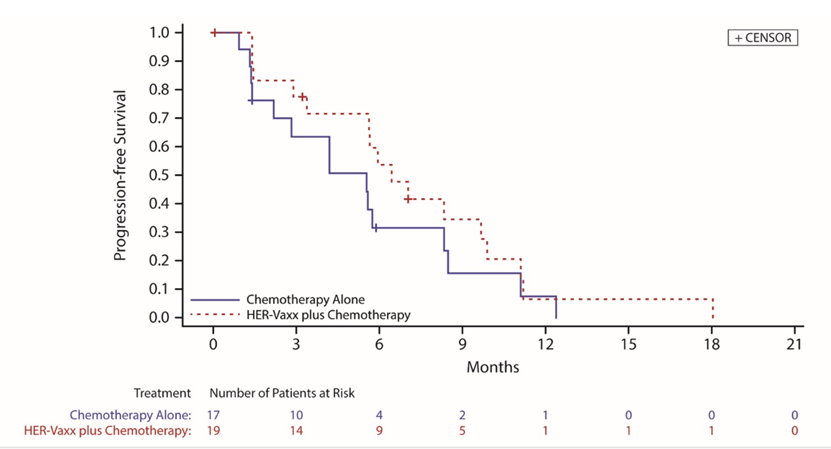
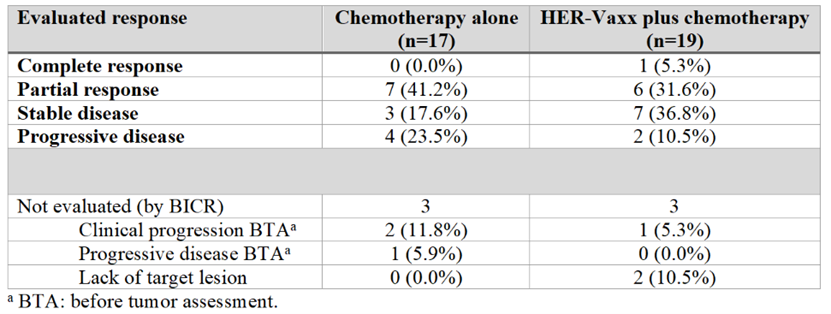
与单独化疗组相比,HER-Vaxx 疫苗联合化疗组患者的总生存期 (OS) 延长了 40% (HR: 0.60; 中位 OS: 13.9 个月 vs. 8.31 个月),HER-Vaxx 疫苗联合化疗组患者的无进展生存期 (PFS) 比单独化疗组高 20% (HR: 0.80; 中位 PFS: 6.93 个月 vs. 6.01 个月),HER-Vaxx 疫苗联合化疗组患者的客观缓解率 (ORR) 为 37%,而单独化疗组患者的 ORR 为 41%,HER-Vaxx 疫苗联合化疗组患者的肿瘤大小较基线平均缩小了 30%,而单独化疗组患者的肿瘤大小较基线平均缩小了 10%。
安全性分析
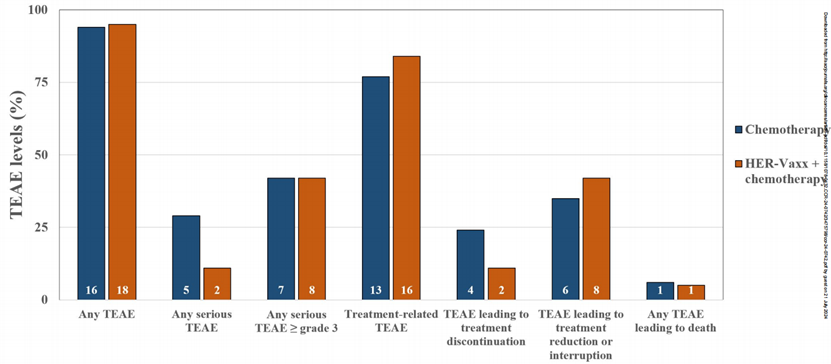
HER-Vaxx 疫苗联合化疗组与单独化疗组之间在不良事件发生率方面没有显著差异,最常见的不良事件包括头痛、食欲下降、腹泻和恶心,这些事件均为轻度至中度,并且可以通过标准支持治疗进行管理,未观察到与 HER-Vaxx 疫苗相关的额外安全性问题。
结论
HER-Vaxx 疫苗联合化疗在治疗 HER2 过表达晚期胃癌患者中表现出良好的安全性和有效性,疫苗诱导的 HER2 特异性抗体反应与肿瘤缩小程度和免疫学功能改善相关,该研究结果表明,HER-Vaxx 疫苗是一种有潜力的 HER2 靶向免疫疗法,有望为 HER2 过表达晚期胃癌患者提供新的治疗选择。
原始出处
Tobias J, et al. 2024. Phase II trial of HER-Vaxx, a B cell peptide-based vaccine, in HER2-overexpressing advanced gastric cancer patients under platinum-based chemotherapy (HERIZON). Clinical Cancer Research.


