人参总皂苷:阿尔茨海默症的神奇治疗钥匙及其深层作用机制
时间:2024-08-02 18:05:47 热度:37.1℃ 作者:网络
阿尔茨海默症(AD)是最常见的痴呆症形式,也是一种起病非常隐匿的进行性发展的神经系统退行性疾病,从轻度的记忆丧失开始,最终发展成为广泛的执行和认知功能严重受损。β淀粉样斑块(Aβ)的形成是AD的主要病理特征之一,因淀粉样前体蛋白(APP)的异常代谢,大量的产生并发生聚集形成淀粉样斑块,最终导致神经毒性的产生。目前临床上常用的治疗手段主要从加强中枢胆碱能活动和减少β淀粉蛋白的沉积入手,但均收效甚微,因此,开发安全有效的AD治疗药物迫在眉睫。
人参作为一种常用的补虚药,具有安神益智的作用,在改善精神状态和调节神经系统疾病方面有着悠久的药用历史。迄今为止,多个研究发现人参的主要活性成分人参总皂苷(TG)可改善神经退行性疾病的记忆和学习,但TG的治疗作用是否与AD患者脑中Aβ的沉积减少相关尚不清楚。
近期,一篇名为“Total ginsenosides decrease Aβ production through activating PPARγ ”的文章探究了TG治疗AD的具体机制。

图1 论文首页
TG治疗改善APP/PS1小鼠的空间学习和记忆能力
研究人员构建APP/PS1转基因小鼠模型进行Morris水迷宫实验,在1-5天的实验中,与对照组相比,模型组的潜伏期增加;与模型组相比,TG治疗组潜伏期降低(图2B),这提示TG对APP/PS1转基因小鼠的空间学习和记忆能力有一定的改善作用。
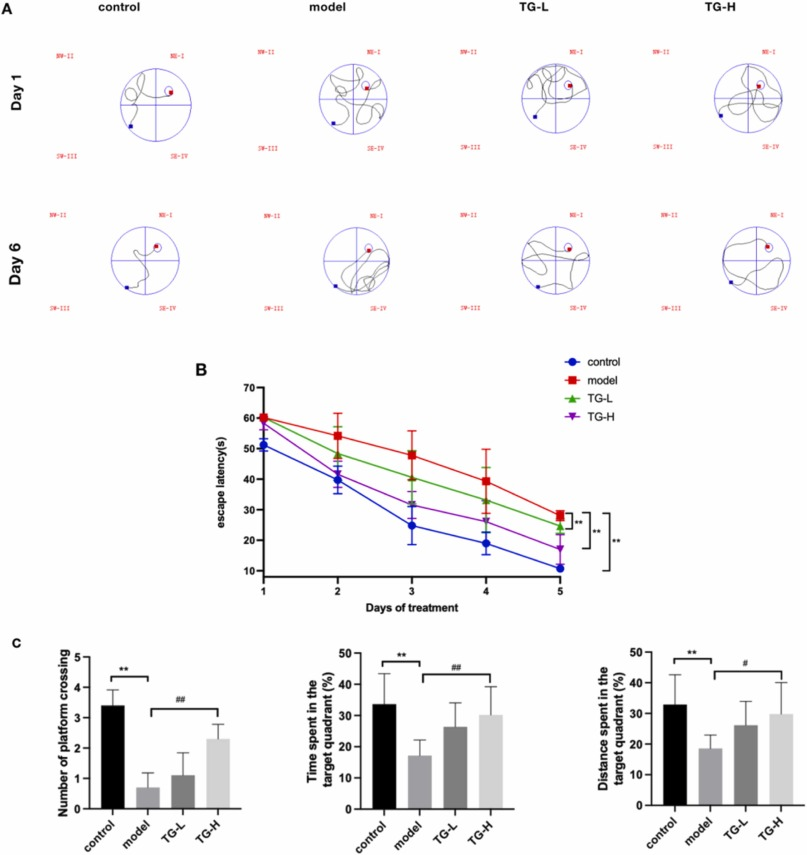
图2 TG治疗改善APP/PS1小鼠的空间学习和记忆能力
TG减轻APP/PS1小鼠海马和皮层区域神经损伤
HE染色结果显示,模型组神经元明显减少、排列松散、形态不规则;与模型组比较TG治疗组神经元数目明显增多,细胞排列紧密,胞浆、胞核染色均匀(图3A),这提示TG可减轻APP/PS1小鼠海马和皮层区域的神经损伤。
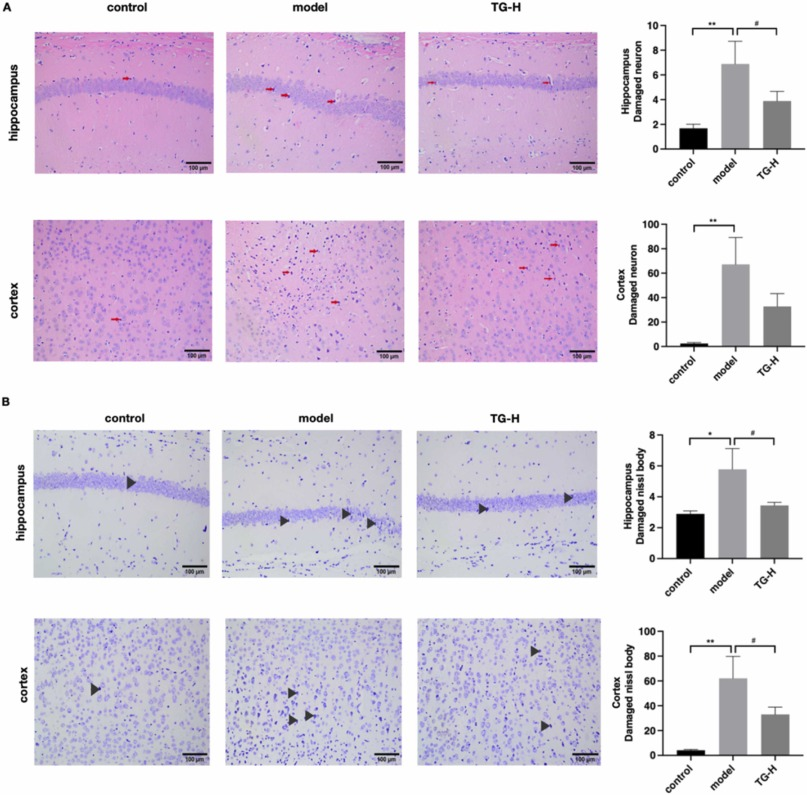
图3 TG减轻APP/PS1小鼠海马和皮层区域神经损伤
TG减少APP/PS1小鼠脑内Aβ的沉积
免疫荧光显示,模型组小鼠皮层和海马区域Aβ斑块数目明显增多,TG给药后Aβ的沉积明显减少,这说明TG可减少APP/PS1小鼠脑内Aβ的沉积(图4C)。
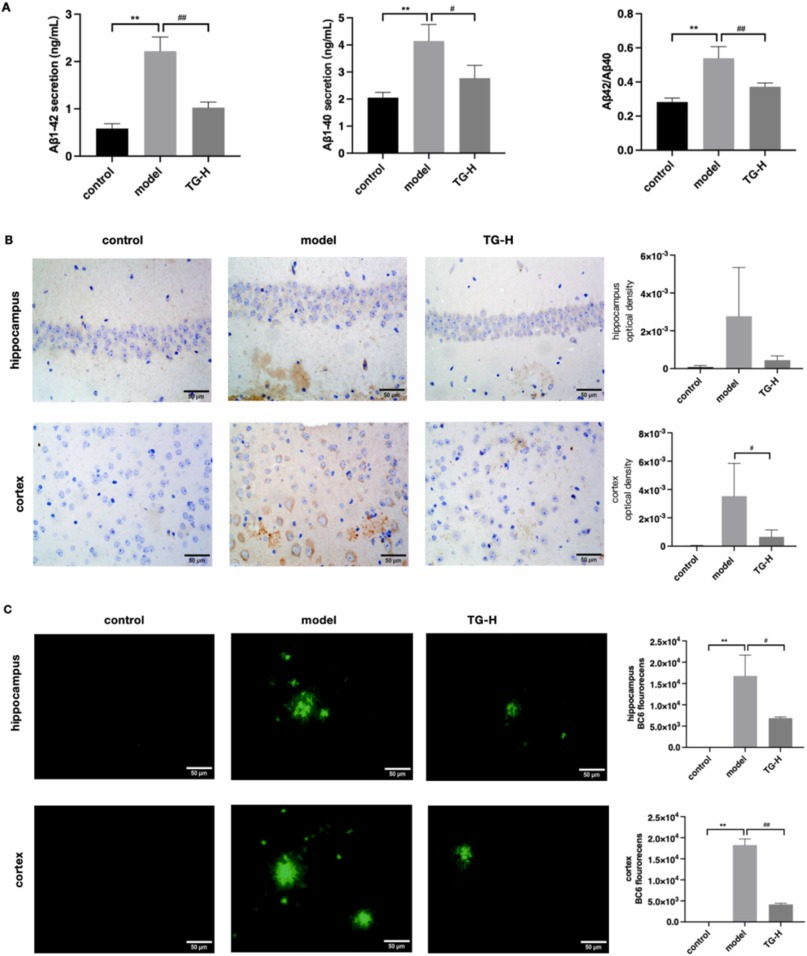
图4 TG减少APP/PS1小鼠脑内Aβ的沉积
TG降低了与淀粉样生成途径相关的基因BACE1、PS1和PS2的表达
为观察TG是否参与调控淀粉样生成相关途径,研究人员对相关基因和蛋白表达水平进行了检测。在模型组中,BACE1,PS1和PS2的mRNA和蛋白质水平要显著高于对照组;TG的治疗则明显降低了BACE1,PS1和PS2的mRNA和蛋白质表达(图5)。
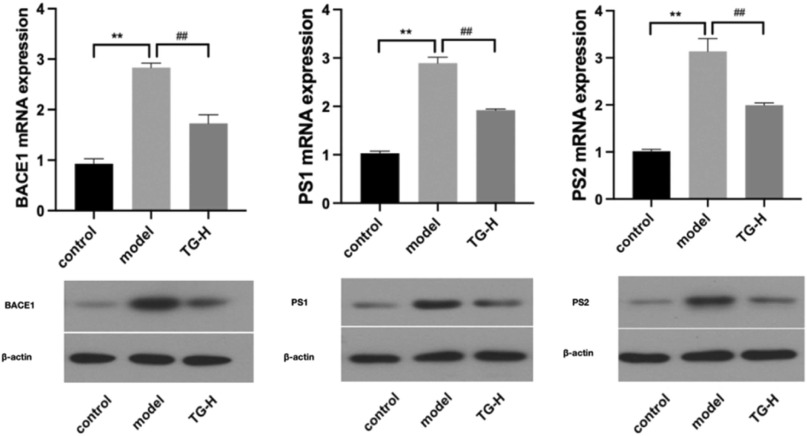
图5 TG抑制了APP/PS1小鼠大脑组织裂解物中BACE1、PS1和PS2的表达
TG对APP/PS1小鼠PPARγ和NF-κB表达的影响
紧接着通过免疫荧光对可影响BACE1表达及活性的过氧化物酶体增殖物激活受体γ(PPARγ)和核因子κB(NF-κB)进行检测,结果显示,与模型组相比,TG治疗组海马和皮层中的PPARγ显著增加(图6A),NF-κB p65核移位显著减少(图7A),这提示TG可能通过抑制NF-κB的核转入,激活PPARγ的表达,从而减少了Aβ的产生。
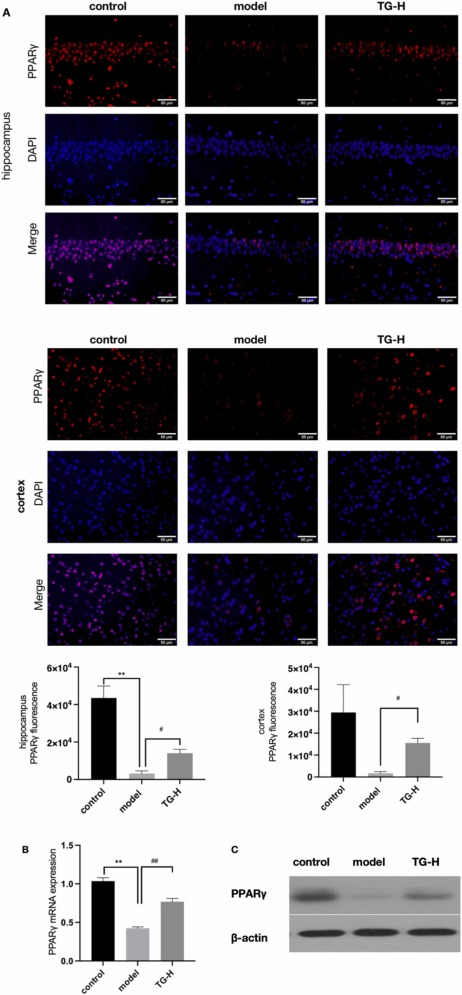
图6 TG增加了海马和皮层中PPARγ的表达
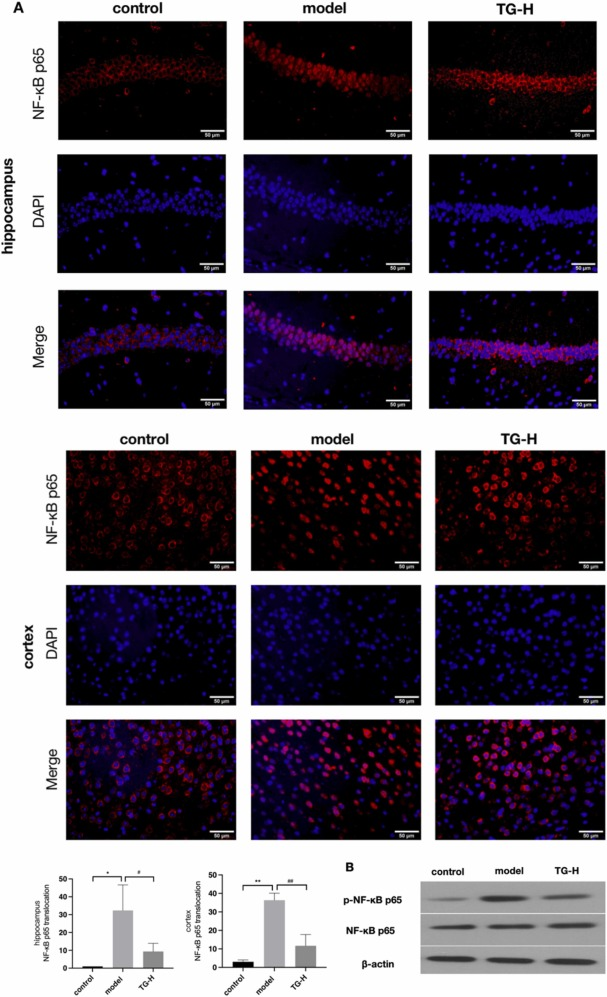
图7 TG减少了海马和皮层中NF-κB的核移位
TG激活PPARγ以减少N2a/APP695细胞中Aβ的分泌
研究人员构建N2a/APP695细胞模型,并选择PPARγ拮抗剂GW9662作为阳性对照组进行研究发现,TG可以显著降低N2a/APP695细胞中Aβ的分泌并中和GW9662的作用(图8)。
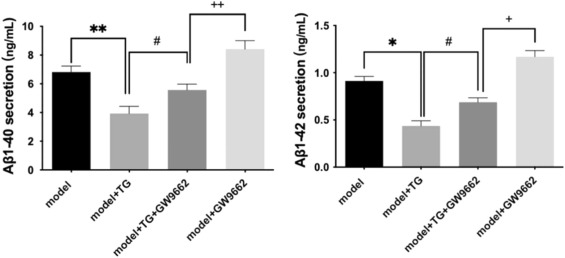
图8 TG通过激活N2a/App695细胞中的PPARγ减少Aβ的分泌
TG通过激活PPARγ抑制N2a/App695细胞中的淀粉样生成途径
使用GW9662预处理后,检测BACE1、sAPPβ、PS1和PS2的mRNA和蛋白质水平,结果显示,TG可显著降低GW9662诱导的N2a/APP695细胞中sAPPβ、BACE、PS1和PS2的过度表达(图9)。
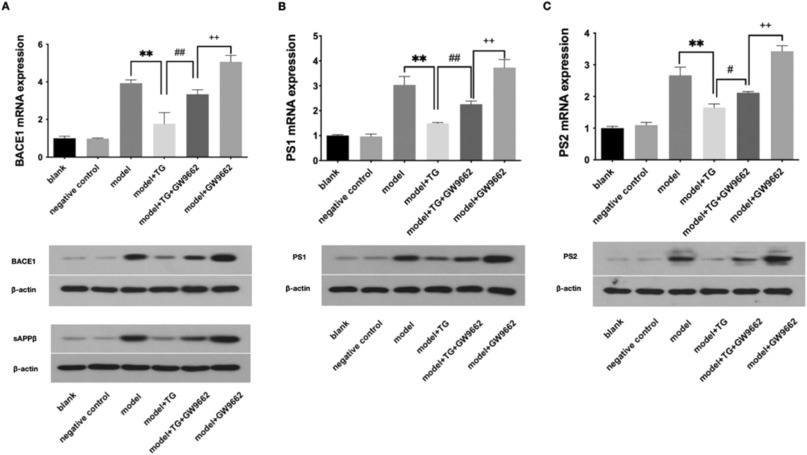
图9 TG降低GW9662诱导的N2a/APP695细胞中sAPPβ、BACE、PS1和PS2的过度表达
TG增加了N2a/APP695细胞中PPARγ的表达,抑制了NF-κB的活性
进一步使用免疫荧光对N2a/APP695细胞中PPARγ和NF-κB的表达进行检测发现,TG显著增强了N2a/APP695细胞中PPARγ的表达(图10),抑制了NF-κB的活性(图11)。
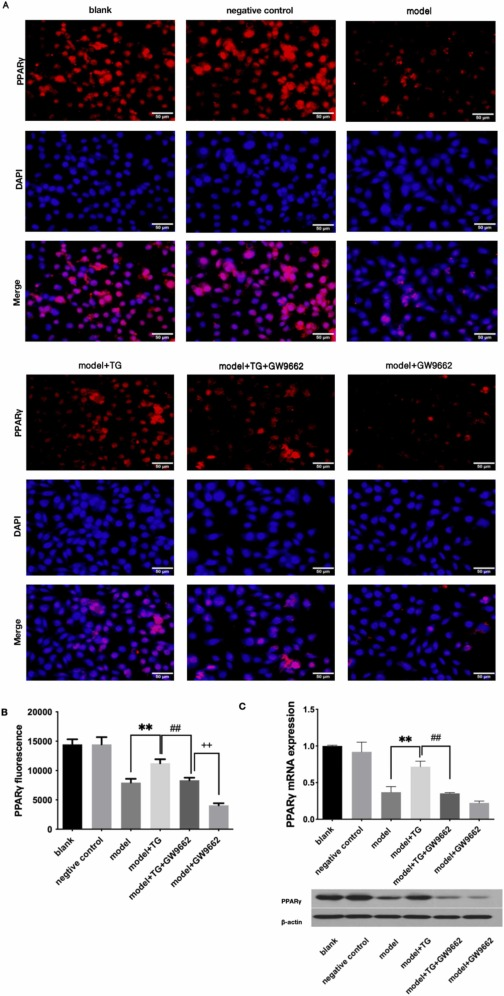
图10 TG增加了N2a/APP695细胞中PPARγ的表达
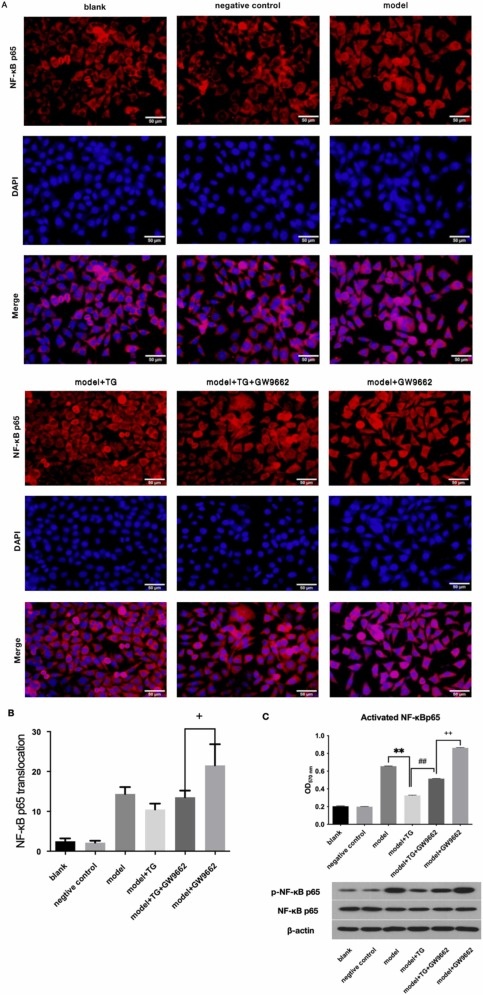
图11 TG抑制了抑制了N2a/APP695细胞中NF-κB的活性
结论
TG可通过抑制NF-κB p65的核转入,激活PPARγ的表达,减少海马和皮层中Aβ的沉积,进而发挥治疗作用,这一结果为AD的治疗提供了新的支持。
参考文献:
Shan He, Junhe Shi, Lina Ma, Hui Pei, Ping Zhang, Dazhuo Shi, Hao Li,Total ginsenosides decrease Aβ production through activating PPARγ,Biomedicine & Pharmacotherapy,Volume 174,2024,116577,ISSN 0753-3322,https://doi.org/10.1016/j.biopha.2024.116577


